XiaoMi-AI文件搜索系统
World File Search System通过 RNA 引导转座对 Anabaena sp. PCC 7120 进行基因组工程改造
摘要:在基因组工程中,传入 DNA 的整合依赖于分裂细胞产生的酶,这一直是提高 DNA 插入频率和准确性的瓶颈。最近,据报道,使用 CRISPR 相关转座酶 (CAST) 的 RNA 引导转座在大肠杆菌中非常有效且具有特异性。在这里,我们开发了 Golden Gate 载体来在丝状蓝藻中测试 CAST,并证明它在鱼腥藻属菌株 PCC 7120 中有效。含有 CAST 和工程转座子的相对较大的质粒通过使用自杀或复制质粒的结合成功转移到鱼腥藻中。编码靶标前导链但不编码反向补体链的单向导 (sg) RNA 与 sgRNA 中包含的原间隔子相关基序 (PAM) 序列有效。在对两个不同靶位点进行分析的六种病例中,有四种的插入位点位于 PAM 之后正好 63 个碱基处。复制质粒上的 CAST 具有毒性,可用于治愈质粒。在分析的所有六种情况下,只有由从左到右元素的序列定义的转座子货物被插入目标位点;因此,RNA 引导的转座是由剪切和粘贴引起的。没有内源转座子通过暴露于 CAST 酶而重新动员。这项工作为通过 RNA 引导的转座在丝状蓝藻中进行基因组编辑奠定了基础,无论是在培养中还是在复杂群落中。关键词:鱼腥藻、CRISPR 相关转座子 (CAST)、基因组工程、RNA 引导的转座、minion 测序、从头基因组组装 ■ 简介
功能丧失方法 siRNA 和基因组编辑...
RNA干扰在保护细胞免受寄生核苷酸序列(病毒和转座子)侵害方面发挥着重要作用,而且在指导发育以及一般基因表达方面也发挥着重要作用。
植物生物技术。 23.0525a(2023)[adv.pub。]
抽象的转座子是移动遗传元件,可以移动到基因组或基因组之间的不同位置。长期以来,它们一直用作基因工程的工具,包括在各种生物中的转基因,插入诱变和标记切除术。源自白菜循环飞蛾的Piggybac转座子是有史以来最有前途的转座子工具之一,因为PiggyBac的优势是它可以转置而不会在切除的地点留下足迹。将Piggybac Transoson应用于植物中的精确基因组编辑,我们证明了从集成到水稻基因组中的转基因基因座的有效且精确的Piggybac Transposon切除。此外,只能通过同源重组介导的基因靶向靶靶标的精确基因修饰的结合以及使用PiggyBac Transposion通过大米中的piggyBac转置从靶基因座进行切除,从而实现了仅将所需点突变引入靶基因。此外,我们为piggybac介导的转带系统设计了序列特异性核酸酶的临时表达,以消除从宿主基因组中的转基因,而无需在成功诱导靶向诱变通过序列特异性核酸盐中促进靶向诱变后,在未经不必要的序列中使用。在这篇综述中,我们总结了我们以前的作品以及Piggybac Transposon基因工程的未来前景。
结合遗传多样性进行作物改良
细长的番茄果实 Xiao 等人 (2008) 圆形或皱褶的豌豆(孟德尔) Ellis 等人 (2011) 高等植物之间交换的 2 百万个转座子 El Baidouri 等人 (2014)
生物化学年度评论 利用 CRISPR 相关 Tn7 样转座子进行天然和人工引导 RNA 定向转座
CRISPR-Cas(成簇的规律间隔的短回文重复序列 - CRISPR 相关核酸酶)防御系统已多次自然地用于指导 RNA 定向转座。在所有情况下,转座子 Tn7 相关的各种元件都参与了转座。Tn7 严格控制转座;只有当专用靶位选择蛋白识别特殊靶标时,转座酶才会被激活。Tn7 和与 CRISPR-Cas 系统合作的 Tn7 样元件进化出了互补的靶向途径:一条途径识别染色体中高度保守的位点,另一条途径靶向能够进行细胞间转移的移动质粒。Tn7 和 Tn7 样元件将单一整合传递到它们识别的位点,并控制整合事件的方向,为未来用作可编程基因整合工具提供了潜力。早期研究表明,引导 RNA 介导的转座系统可以适应不同的宿主,甚至在微生物群落内,这表明将这些系统设计为强大的基因编辑工具具有巨大的潜力。
全球动物生物技术应用概览...
微注射预复合逆转录病毒SCNT转座子-基于基因组编辑的DNA进入早期DNA,通过精子递送遗传介导的基因组改变阶段受精卵进入受精卵工程细胞整合(ZFNs,TALENs,CRISPR / Cas9)
RNA 引导的睡美人转座重新定位......
摘要 基因治疗的理想工具是能够在人类基因组的预定位点上实现有效的基因整合。我们在此展示了睡美人 (SB) 转座子与 CRISPR/Cas9 系统的组件相结合而实现的偏向性全基因组整合。我们提供概念证明,通过将 SB 与催化失活的 Cas9 (dCas9) 融合并提供针对人类 Alu 逆转录转座子的单向导 RNA (sgRNA),可以影响 SB 的靶位选择。转座子整合的富集依赖于 sgRNA,并且以不对称模式发生,偏向于 sgRNA 靶标下游相对较窄的 300 bp 窗口内的位点。我们的数据表明,CRISPR/Cas9 指定的靶向机制迫使整合到基因组区域,而这些区域原本是 SB 转座的不良靶标。未来对该技术的改进可能会允许开发用于精确基因工程的特定基因插入方法。
一个多功能的托管病毒衍生的纳米颗粒,其靶向癌细胞并内化为
随着合成生物学的努力变得更加雄心勃勃,活细胞中预定义功能的工程需要越来越准确的工具。此外,遗传构建体的表型性能的表征需要细致的测量和广泛的数据获取,以实现进食数学模型和沿设计构建测试生命周期的匹配预测。在这里,我们开发了一种遗传工具,可以简化高通量转座子插入测序(TNSEQ):携带HIMAR1 Mariner Transposase System的PBLAM1-X质粒载体。这些质粒源自Mini-TN5转座子矢量PBAMD1-2,并按照标准欧洲矢量体系结构(SEVA)格式的模块化标准构建。为了展示它们的功能,我们分析了60个土壤假单胞菌putida kt2440克隆的测序结果。新的PBLAM1-X工具已经包含在最新的SEVA数据库版本中,在这里我们使用实验室自动化工作流程描述其性能。
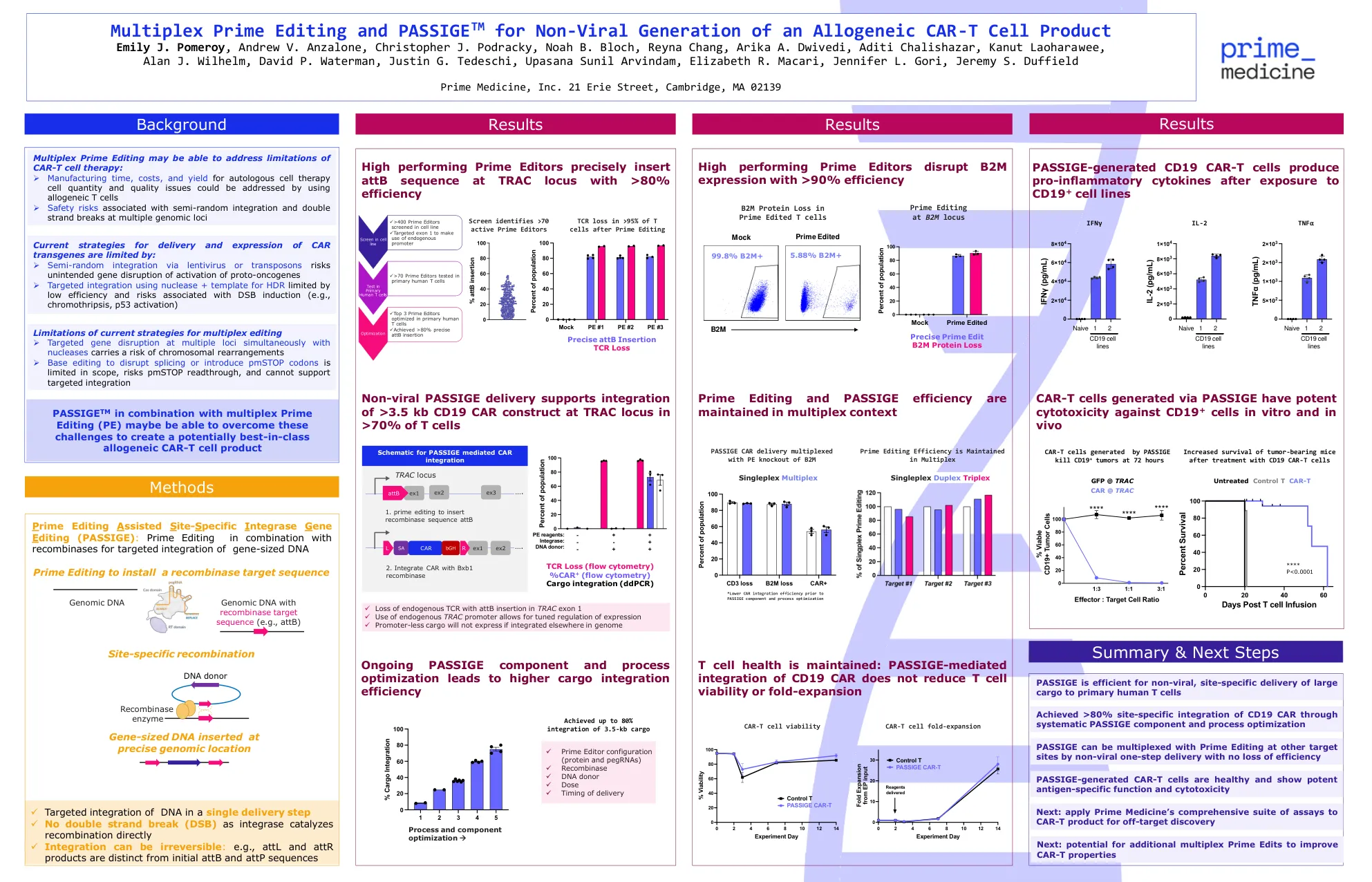
多重素数编辑和非病毒的传递...
当前的CAR转基因输送和表达策略受到以下限制:➢通过慢病毒或转座子通过慢性病毒或转座的半随机整合危险,即在核酸酶 + to ndrate +限制与DSB诱导相关的HDR限制的核酸酶 +模板的核酸酶积分的靶向整合(例如/chromothips)
高通量筛选的标准化转座子工具开发和验证Ammon-Ohe模型,以预测肝硬化门诊患者的明显肝脑病的风险
背景和目的:建议进行神经心理学和心理物理测试,以评估明显的肝病(OHE)的风险,但其准确性是有限的。高莫纳米亚人在OHE的发病机理中是中心的,但其预测效用尚不清楚。在这项研究中,我们旨在确定神经心理学或心理物理测试和氨的作用,并开发一种模型(Ammon-Ohe),以分层持续患有肝硬化的门诊患者的OHE发育风险。方法:这项观察性的前瞻性研究包括426个门诊病人,没有三个肝单元的先前OHE,其中位数为2。5年。心理测量肝病评分(PHES)<-4或临界频率(CFF)<39被认为是异常的。氨将其标准化为正常(AMM-ULN)的上限。多变量脆弱的竞争风险和随机生存的森林分析,以预测未来的OHE并开发Ammon-Ohe模型。使用来自两个独立单位的267和381例患者进行外部验证。结果:根据PHES或CFF和Ammonia在到达时间(log-Rank p <0.001)中存在显着差异,在PHES异常PLUS PLUS PLUS GULL AMM-ULN的患者中,风险最高(危险比4.4; 95%CI 2.4-8.1; p <0.001; p <0.001;与正常的PHES和AMM--uln和AMM--uln相比)。在多变量分析中,AMM-ULN而不是PHE或CFF是OHE发展的独立预测指标(危险比1.4; 95%CI 1.1-1.9; p = 0.015)。Ammon-Ohe模型(性别,糖尿病,白蛋白,肌酐和AMM-ULN)的C-指数为0.844,在两个外部验证队列中预测OHE的第一集,为0.728。结论:在这项研究中,我们开发了和验证了Ammon-Ohe模型,其中包括易于使用的临床和生化变量,可用于鉴定门诊患者,该门诊患者具有开发第一集的最高风险。



![植物生物技术。 23.0525a(2023)[adv.pub。]](/simg/d\d487db999e4f1cf93c146fa75cd24c27419e4718.webp)