XiaoMi-AI文件搜索系统
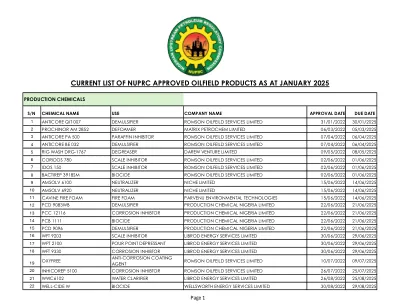
World File Search System截至一月份的 NUPRC 批准油田产品清单……
1 ANTICORE QIT 007 破乳剂 ROMSON OILFEILD SERVICES LIMITED 31/01/2022 30/01/2025 2 PROCHINOR AM 2852 消泡剂 MATRIX PETROCHEM LIMITED 06/03/2022 05/03/2025
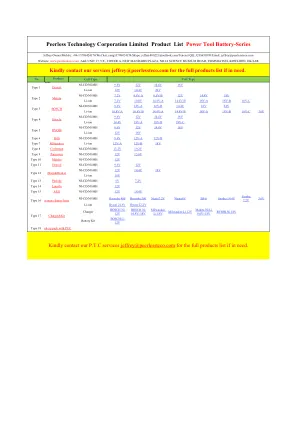
Peerless Technology Corporation Limited产品清单功能...
Jeffrey所有者/移动设备: +86-13798424174/WECHAT:yang13798424174/skype:jeffrey880221@outlook.com/tencenc.com/tencent QQ:3205630599/email:
2024 VOD和数据记录器,用品和配件产品清单
1-02-01 Handitrap II™VOD记录器每个便携式1通道连续爆炸的爆炸速度(VOD)记录器,用于一个蓝鸟和炸药样品中的炸药。分辨率= 12位,4,096中的1个部分。记录速度为1 MHz。131,000个数据点的内存= 131毫秒记录时间。内部和外部触发模式。预触发时间是总记录时间的25%。通过可充电的NICAD电池运行(长达8小时)。Includes HandiTrap II™ VOD Recorder, 120 or 230 VAC Battery Charger (as specified by the Customer), USB Communications Cable, External Trigger Adapter, padded HandiTrap II™ Carry Case, HandiTrap II™ Operations Manual (English), DAS™ Data Acquisition Suite Standard Edition Software for Windows XP™ and later.包括MREL可再生1年综合100%零件和劳动保修(有关更多详细信息,请与MREL联系)。如何为此产品选择正确的配件:在下面确定您的应用程序,然后选择本出版物后面列出的适当兼容的配件。应用程序#1:测量Blastholes中爆炸物的VOD(第8页)应用程序#2:测量炸药样本的VOD(第12页)
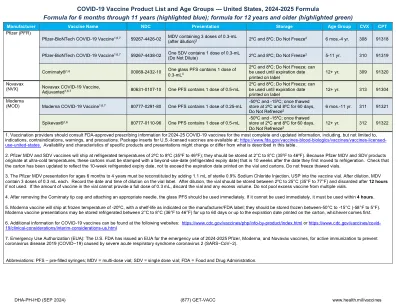
2024 年至 2025 年 COVID-19 疫苗产品清单及年龄组
3. 辉瑞 MDV 适用于 6 个月至 4 岁的儿童,必须将 1.1 mL 无菌 0.9% 氯化钠注射液 (USP) 添加到疫苗瓶中以重新配制。稀释后,MDV 含有 3 剂,每剂 0.3 mL。在疫苗瓶标签上记录稀释的日期和时间。稀释后,疫苗瓶应储存在 2ºC 至 25°C (35°F 至 77°F) 之间,如果未使用,则在 12 小时后丢弃。如果疫苗瓶中的疫苗量不能提供 0.3 mL 的完整剂量,则丢弃疫苗瓶和任何多余的量。不要将多个疫苗瓶中的多余疫苗混合在一起。
NCP产品时间表和NCP吸附产品清单上列出产品的指南
所有先前被确定为获得书面认证的吸附剂的产品,证实了其从EPA中获得的书面认证,直到2025年12月12日至2025年12月12日,所有吸引人的产品都必须已根据第300.955(a)和(b)条提交了修订的信息,并满足任何相关清单要求,并在新的Sorbent产品列表中列出了任何相关清单。EPA将不再在2023年12月11日之后签发吸附产品的书面证书。符合2023 S子部分要求的吸尘器产品将在公开可用的吸令产品列表中列出。不需要为仅由材料或任何组合组合的吸附产品提交技术数据,这些产品在§300.915(g)(g)(1)的定义中确定了材料的任何组合;这些材料自动包含在吸附产品列表中,作为通用吸附剂,无需采取进一步的措施。请参阅第5章吸附剂和此指南的吸附产品清单,以获取更多信息。
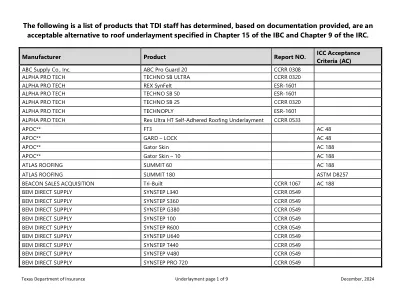
以下是 TDI 工作人员根据提供的文件确定的可接受的屋顶衬垫替代品的产品清单
STARWRAP, Inc. Shingle Whale Shield CCRR 1038 AC 188 STARWRAP, Inc. Shingle Whale Superior CCRR 1038 AC 188 STARWRAP, Inc. Shingle Whale Prime CCRR 1038 AC 188 STARWRAP, Inc. Shingle Whale Platinum CCRR 1038 AC 188 SYSTEM COMPONENTS CORPORATION COVERPRO® 1000、2000 和 3000 CCRR 0310 AC 188 SYSTEM COMPONENTS CORPORATION FELTEX® CCRR 0310 AC 188 SYSTEM COMPONENTS CORPORATION FELTEX® SA3000 CCRR 0310 AC 188 TAMKO Building Products LLC TW METAL AND TILE ESR 1252 TAMKO Building Products LLC TW UNDERLAYMENT ESR 1252 TAMKO Building Products LLC SYNTHETICGUARD CCRR 1056 TAMKO 建筑产品 LLC SYNTHETICGUARD PLUS CCRR 1056 TARCO EASYLAY® HPP ESR 2634
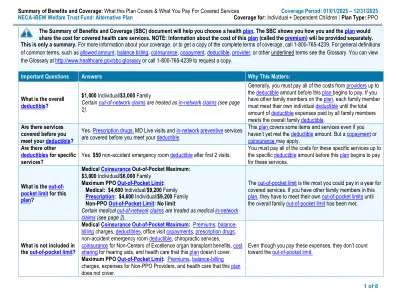
承保范围:个人 + 受抚养子女 | 计划类型
精选药品和产品清单中所列的由医院、诊所或机构内的医疗保健提供者管理的特种药品以及自行管理的药品均需进行医疗必要性的预先认证并参与精选药品和产品计划。基因和细胞治疗产品不在本计划的承保范围内。Humira、Skyrizi 和 Rinvoq 不在本计划的承保范围内。所有接受精选药品和产品清单中所列特种药品的受保人都必须参加精选药品和产品计划。特种药品需经过事先授权、分步疗法和行政审查,可能要求使用特定的药品分销渠道。未能获得事先授权可能会导致成本控制罚款,相当于应付福利减少 100%。
北约推荐的产品列表
目录A.在北约级别批准的Infosec产品清单…………6 B.根据常见标准评估的信息技术产品清单……………………………………。32 C. LISTA PACHETELOR ŞI PROFILELOR DE PROTECŢIE EVALUATE CONFORM CRITERIILOR COMUNE ………………………………………………………………… 215 D. LISTA PRODUCĂTORILOR NAŢIONALI DE ECHIPAMENTE PROTEJATE TEMPEST ………………………………………………………………………………………… 228 E. LISTA PRODUSELOR ŞI MECANISMELOR criptografice证书la nivel na na na na na na na na na na na na na na na n na n na n na n na n na n na n na n na n na n na n na n na n na n na nnaţ .................................................................................................................................................................................................................... 237
EU Monitor - COM(1998) 257 Final 98/0162 (ACC)
出口管制是国际安全的一个贸易方面。直到最近,在欧盟,此类管制仅由国家立法执行。然而,内部市场的完成需要最低限度地协调出口管制,以允许双重用途产品在共同体内自由流动。正是在这种背景下,欧盟理事会于 1994 年 12 月 19 日通过了现行的共同体双重用途产品出口管制制度:由理事会条例 (EC) No 3381/94 1 和理事会决定 94/942/CFSP 2 组成的双支柱体系。前者主要处理许可方面和行政合作;后者包含受控产品清单和成员国可适用简化许可程序的国家/地区指示性清单。概括起来,现行制度的两大要素是:一是共同产品清单;二是出口许可证相互承认原则。
NSF 提案和奖励政策更新 EPSCoR PI 会议
• 增加了机构、专业和学术职位和任命的定义(包含在更新的定义文件中)。 • 修改了认证语言以解决问题,但是,每个联邦研究资助机构都有责任提供有关该机构具体适用的认证要求的详细说明。还增加了规定签名必须与提交的提案在同一日历年的语言。 • 增加了关于恶意外国人才招聘计划的新认证(这两项变化也适用于当前和待定的(其他)支持)。 • 增加了有关专业任命的参数:“关于专业任命,高级/关键人员必须仅识别其主要组织之外的所有当前国内外专业任命。” • 修订了有关产品清单的指导:“所提供的产品清单应由高级/关键人员以最能展示其开展拟议研究的能力的方式进行组织。每个联邦研究资助机构都有责任就允许的产品数量的任何具体限制发布指导。”