XiaoMi-AI文件搜索系统
World File Search System质子泵抑制剂药物在……中的应用
质子泵抑制剂(PPI)是一种对患有各种疾病的患者具有良好安全性和有效性的药物,因此在世界各地均被常规使用,其中之一就是日惹北大穆罕默迪亚甘平医院。本研究旨在评估住院患者PPI药物的使用情况。所采用的研究方法是描述性观察和横断面设计。通过二手资料收集数据,即治疗第一天接受PPI治疗的住院患者200份病历。研究结果显示,PPI 药物使用诊断最高的是胃肠道疾病(60.50%)和非胃肠道疾病(39.50%)。使用的PPI类型为泮托拉唑注射液40mg/ml(97%)、兰索拉唑片30mg(2.5%)、兰索拉唑注射液30mg/ml(0.5%)。 PPI使用的正确剂量依从性为100%。
干货:如何利用EN 脚设计出好电源?
1.以 ZL6205 为例,先简单介绍一下 ........................................................................ 1 2.直接上拉使能 ........................................................................................................... 2 3.电阻分压使能 ........................................................................................................... 3 4.其他使能应用 ........................................................................................................... 4 5.免责声明 ................................................................................................................... 6
Nysdoh AI资源:艺术药物互动|表25:降低酸性剂
ppis:如果可以使用替代酸还原剂,替代PI或增强的ATV,请勿将其与未升高的ATV共同辅助。•时机:在RTV-或COBI增强的ATV之前管理≥12小时。•Art-Neive:如果无法避免使用,则每天不超过奥美拉唑20毫克或同等用途(例如,pantoprazole 40 mg;兰索拉唑30毫克;埃索美拉唑20毫克)。•经验丰富:咨询经验丰富的艾滋病毒护理提供者或GI专家。H2RAS:•艺术:在至少2小时前或10小时前用食物施用ATV 400毫克(未增强)。•经验丰富:请勿将Unboosted ATV + Famotidine组合使用。•不超过任何H2RA的20毫克的剂量。每日总剂量不得超过40 mg Famotidine或同等剂量,例如Ranitidine或Nizatidine 150 mg(每天300毫克)。atazanavir(ATV),增强•ATV需要吸收酸性胃pH,酸 -
Vismaya Babu KK,国际。药学杂志。 《科学》,2025 年,第 3 卷,第 2 期,3521-3527
药物再利用是一种新兴策略,用于确定已在临床用于治疗不同疾病的药物的新靶点。这是一种既经济又省时的替代方法,因为药理学、安全性和毒性特征已经确定。质子泵抑制剂泮托拉唑在针对癌细胞系进行的几项研究中显示出抗癌活性,还表明它在抗血管生成机制中发挥作用。为了确定抗癌特征,进行了 MTT 试验。结果表明泮托拉唑对癌细胞系具有细胞毒性。对绿豆进行了细胞毒性的初步评估,并评估了其发芽反应。发芽抑制也揭示了该药物的细胞毒性潜力。进行了绒毛尿囊膜试验以评估该药物的血管生成潜力。浓度为 50 微克/毫升的泮托拉唑破坏了受精卵中的血管形成。
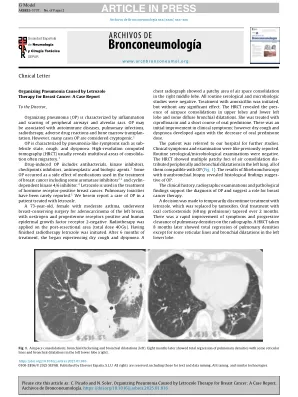
来曲唑治疗引起的肺炎的治疗...
没有任何显著影响。HRCT 显示上叶和左下叶存在气腔实变,以及一些弥漫性支气管扩张。她接受了环丙沙星和短期口服泼尼松治疗。临床症状最初有所改善;然而干咳和呼吸困难
Esopreze(Esomeprazole镁三水合物)多重...
单中心,随机,单盲,双臂平行的,重复的剂量研究检查了埃索美拉唑的药代动力学及其在控制1-24个月的婴儿中控制胃内pH值的功效。患者每天每天口服每天口服0.25 mg/kg或1.0 mg/kg的患者,持续7或8天。五十名患者被随机分配,其中43例≤12个月大,7岁> 12个月大。四十五名患者完成了39个≤12个月大的研究,> 12个月大。达到最大血浆浓度(T MAX)的中位时间为0.25 mg/kg剂量约2小时,而1.0 mg/kg剂量组的中位时间为3小时。平均AUCτ为1.0 mg/kg剂量的3.51μmol.H/L,0.25 mg/kg剂量的剂量为0.65μmol.h/l。分别为1.0 mg/kg和0.25 mg/kg剂量获得了0.85μmol/L和0.17μmol/L的平均C最大值。ssmax ssmax ssmax 。 无法得出关于剂量比例的结论。 胃内pH> 4的平均时间百分比从基线时的30.5%增加到0.25 mg/kg剂量组的47.9%,在1.0 mg/kg剂量组中的平均时间从28.6%增加到28.6%到69.3%。 从统计学上讲,与相比,埃索美拉唑的增加明显更高ssmax ssmax ssmax 。 无法得出关于剂量比例的结论。 胃内pH> 4的平均时间百分比从基线时的30.5%增加到0.25 mg/kg剂量组的47.9%,在1.0 mg/kg剂量组中的平均时间从28.6%增加到28.6%到69.3%。 从统计学上讲,与相比,埃索美拉唑的增加明显更高ssmax ssmax 。 无法得出关于剂量比例的结论。 胃内pH> 4的平均时间百分比从基线时的30.5%增加到0.25 mg/kg剂量组的47.9%,在1.0 mg/kg剂量组中的平均时间从28.6%增加到28.6%到69.3%。 从统计学上讲,与相比,埃索美拉唑的增加明显更高ssmax ssmax 。 无法得出关于剂量比例的结论。 胃内pH> 4的平均时间百分比从基线时的30.5%增加到0.25 mg/kg剂量组的47.9%,在1.0 mg/kg剂量组中的平均时间从28.6%增加到28.6%到69.3%。 从统计学上讲,与相比,埃索美拉唑的增加明显更高ssmax ssmax 。 无法得出关于剂量比例的结论。 胃内pH> 4的平均时间百分比从基线时的30.5%增加到0.25 mg/kg剂量组的47.9%,在1.0 mg/kg剂量组中的平均时间从28.6%增加到28.6%到69.3%。 从统计学上讲,与相比,埃索美拉唑的增加明显更高ssmax ssmax 。 无法得出关于剂量比例的结论。 胃内pH> 4的平均时间百分比从基线时的30.5%增加到0.25 mg/kg剂量组的47.9%,在1.0 mg/kg剂量组中的平均时间从28.6%增加到28.6%到69.3%。 从统计学上讲,与相比,埃索美拉唑的增加明显更高ssmax ssmax 。 无法得出关于剂量比例的结论。 胃内pH> 4的平均时间百分比从基线时的30.5%增加到0.25 mg/kg剂量组的47.9%,在1.0 mg/kg剂量组中的平均时间从28.6%增加到28.6%到69.3%。 从统计学上讲,与相比,埃索美拉唑的增加明显更高ssmax ssmax 。 无法得出关于剂量比例的结论。 胃内pH> 4的平均时间百分比从基线时的30.5%增加到0.25 mg/kg剂量组的47.9%,在1.0 mg/kg剂量组中的平均时间从28.6%增加到28.6%到69.3%。 从统计学上讲,与相比,埃索美拉唑的增加明显更高ssmax ssmax 。 无法得出关于剂量比例的结论。 胃内pH> 4的平均时间百分比从基线时的30.5%增加到0.25 mg/kg剂量组的47.9%,在1.0 mg/kg剂量组中的平均时间从28.6%增加到28.6%到69.3%。 从统计学上讲,与相比,埃索美拉唑的增加明显更高ssmax ssmax 。 无法得出关于剂量比例的结论。 胃内pH> 4的平均时间百分比从基线时的30.5%增加到0.25 mg/kg剂量组的47.9%,在1.0 mg/kg剂量组中的平均时间从28.6%增加到28.6%到69.3%。 从统计学上讲,与相比,埃索美拉唑的增加明显更高ssmax ssmax 。 无法得出关于剂量比例的结论。 胃内pH> 4的平均时间百分比从基线时的30.5%增加到0.25 mg/kg剂量组的47.9%,在1.0 mg/kg剂量组中的平均时间从28.6%增加到28.6%到69.3%。 从统计学上讲,与相比,埃索美拉唑的增加明显更高ssmax ssmax 。 无法得出关于剂量比例的结论。 胃内pH> 4的平均时间百分比从基线时的30.5%增加到0.25 mg/kg剂量组的47.9%,在1.0 mg/kg剂量组中的平均时间从28.6%增加到28.6%到69.3%。 从统计学上讲,与相比,埃索美拉唑的增加明显更高ssmax ssmax 。 无法得出关于剂量比例的结论。 胃内pH> 4的平均时间百分比从基线时的30.5%增加到0.25 mg/kg剂量组的47.9%,在1.0 mg/kg剂量组中的平均时间从28.6%增加到28.6%到69.3%。 从统计学上讲,与相比,埃索美拉唑的增加明显更高ssmax ssmax 。 无法得出关于剂量比例的结论。 胃内pH> 4的平均时间百分比从基线时的30.5%增加到0.25 mg/kg剂量组的47.9%,在1.0 mg/kg剂量组中的平均时间从28.6%增加到28.6%到69.3%。 从统计学上讲,与相比,埃索美拉唑的增加明显更高ssmax ssmax 。 无法得出关于剂量比例的结论。 胃内pH> 4的平均时间百分比从基线时的30.5%增加到0.25 mg/kg剂量组的47.9%,在1.0 mg/kg剂量组中的平均时间从28.6%增加到28.6%到69.3%。 从统计学上讲,与相比,埃索美拉唑的增加明显更高ssmax ssmax 。 无法得出关于剂量比例的结论。 胃内pH> 4的平均时间百分比从基线时的30.5%增加到0.25 mg/kg剂量组的47.9%,在1.0 mg/kg剂量组中的平均时间从28.6%增加到28.6%到69.3%。 从统计学上讲,与相比,埃索美拉唑的增加明显更高ssmax ssmax 。 无法得出关于剂量比例的结论。 胃内pH> 4的平均时间百分比从基线时的30.5%增加到0.25 mg/kg剂量组的47.9%,在1.0 mg/kg剂量组中的平均时间从28.6%增加到28.6%到69.3%。 从统计学上讲,与相比,埃索美拉唑的增加明显更高ssmax ssmax 。 无法得出关于剂量比例的结论。 胃内pH> 4的平均时间百分比从基线时的30.5%增加到0.25 mg/kg剂量组的47.9%,在1.0 mg/kg剂量组中的平均时间从28.6%增加到28.6%到69.3%。 从统计学上讲,与相比,埃索美拉唑的增加明显更高ssmax ssmax 。 无法得出关于剂量比例的结论。 胃内pH> 4的平均时间百分比从基线时的30.5%增加到0.25 mg/kg剂量组的47.9%,在1.0 mg/kg剂量组中的平均时间从28.6%增加到28.6%到69.3%。 从统计学上讲,与相比,埃索美拉唑的增加明显更高ssmax ssmax 。 无法得出关于剂量比例的结论。 胃内pH> 4的平均时间百分比从基线时的30.5%增加到0.25 mg/kg剂量组的47.9%,在1.0 mg/kg剂量组中的平均时间从28.6%增加到28.6%到69.3%。 从统计学上讲,与相比,埃索美拉唑的增加明显更高ssmax ssmax 。 无法得出关于剂量比例的结论。 胃内pH> 4的平均时间百分比从基线时的30.5%增加到0.25 mg/kg剂量组的47.9%,在1.0 mg/kg剂量组中的平均时间从28.6%增加到28.6%到69.3%。 从统计学上讲,与相比,埃索美拉唑的增加明显更高ssmax ssmax 。 无法得出关于剂量比例的结论。 胃内pH> 4的平均时间百分比从基线时的30.5%增加到0.25 mg/kg剂量组的47.9%,在1.0 mg/kg剂量组中的平均时间从28.6%增加到28.6%到69.3%。 从统计学上讲,与相比,埃索美拉唑的增加明显更高ssmax ssmax 。 无法得出关于剂量比例的结论。 胃内pH> 4的平均时间百分比从基线时的30.5%增加到0.25 mg/kg剂量组的47.9%,在1.0 mg/kg剂量组中的平均时间从28.6%增加到28.6%到69.3%。 从统计学上讲,与相比,埃索美拉唑的增加明显更高ssmax 。 无法得出关于剂量比例的结论。 胃内pH> 4的平均时间百分比从基线时的30.5%增加到0.25 mg/kg剂量组的47.9%,在1.0 mg/kg剂量组中的平均时间从28.6%增加到28.6%到69.3%。 从统计学上讲,与相比,埃索美拉唑的增加明显更高。无法得出关于剂量比例的结论。胃内pH> 4的平均时间百分比从基线时的30.5%增加到0.25 mg/kg剂量组的47.9%,在1.0 mg/kg剂量组中的平均时间从28.6%增加到28.6%到69.3%。从统计学上讲,与