XiaoMi-AI文件搜索系统
World File Search System疫苗存储和处理表
他们”在Immunize.org。2 Rotarix和Menveo疫苗可作为不需要稀释的液体配方,或者是需要重新构成的冻干疫苗。3如果您对交货时疫苗的状况有疑问,请立即将疫苗放在建议的存储单元中,标签“不使用”并与制造商联系。如果您对儿童疫苗(VFC)疫苗的状况有疑问,请联系您的当地卫生部门。4如果疫苗被冷冻(仅冷冻疫苗)或融化后重新冻结,请标记疫苗“不使用”,在制造商建议的温度下存储并与制造商联系以确定可行性,除非受影响的疫苗为VFC,否则请与LHD联系以进行LHD。5有关如何安全处理干冰的信息,请参阅“医疗保健专业人员的干冰安全性(CDC.GOV)。” 6 U.S. Covid-19-19始终使用最早的日期。在
疫苗储存及处理表
DTaP、DTaP-HepB-IPV (Pediarix ® )、DTaP-IPV-Hib-HepB (Vaxelis ® )、DTaP-IPV (Quadracel ® 、Kinrix ® )、DTaP-IPV/Hib (Pentacel ® ) 1 、Td、Tdap、HepA、HepB (Engerix-B ® 、 Recombivax HB ® 、Heplisav-B ® 、PreHevbrio ® )、HepA-HepB (Twinrix ® )、Hib (PedvaxHIB ® 、ActHIB ®1 、Hiberix ®1 )、9vHPV、IPV、MenACWY (Menveo ®1,2 、MenQuadfi ® )、MenB (Bexsero ®、特鲁门巴®)、MenABCWY (Penbraya™)、肺炎球菌(PCV13、PCV15、PCV20、PPSV23)、aIIV4(Fluad®)、HD-IIV4(Fluzone® High-Dose)、IIV4、ccIIV4(Flucelvax®)、RIV4(Flublok®)、LAIV4、重组带状疱疹疫苗(RZV、Shingrix)1、呼吸道合胞病毒(RSV、Abrysvo™、Arexvy)1
GSR 案件处理表 - 法医
- 对于手,这将是手背。 - 对于从其他物品中收集的套件,这将是根据提供的信息具有最大证明价值的两个样本。 • 提交的服装或其他物品调查使用每件包装物品的单个存根进行抽样,除非另有指示。
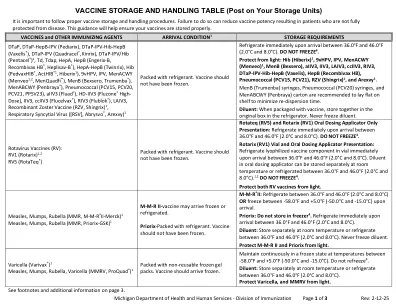
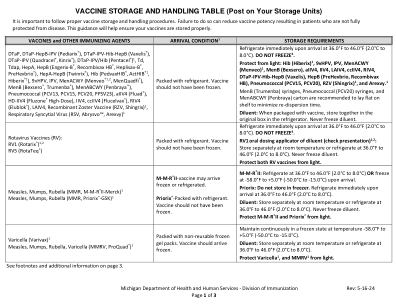
疫苗储存和处理表(张贴在您的储存单元上)
疫苗到达条件 3 储存要求 DTaP、DTaP-HepB-IPV(Pediarix ®)、DTaP-IPV-Hib- HepB(Vaxelis ®)、DTaP-IPV(Quadracel ®、Kinrix ®)、DTaP-IPV/Hib(Pentacel ®)1、Td、Tdap、HepA、HepB(Engerix-B ®、Recombivax HB ®、Heplisav-B ®、PreHevbrio ®)、HepA-HepB(Twinrix ®)、Hib(PedvaxHIB ®、ActHIB ®1、Hiberix ®1)、9vHPV、IPV、MenACWY(Menveo ®1,2、MenQuadfi ®)、MenB(Bexsero ®、Trumenba ®)、肺炎球菌(PCV13、PCV15、PCV20、PPSV23)、aIIV4(Fluad ®)、HD-IIV4(Fluzone ® High-Dose)、IIV4、ccIIV4(Flucelvax ®)、RIV4(Flublok ®)、LAIV4、重组带状疱疹疫苗(RZV、Shingrix)1、呼吸道合胞病毒(RSV、Abrysvo TM1、Arexvy 1)
快速链接 - 创意VA
协议是指由预订,条款和数据处理表的合法约束合同。预订是指预订表格(设置我们两个组织的详细信息;我们将为您做的工作;以及有关我们之间特别安排的其他条款和条件)。预订表可以通过我们的商定项目管理渠道进行修改或更新,我们俩都同意以书面形式进行更改;当我们一个人未遵守协议下的任何义务时,违反违规就会发生。机密信息是指我们中一个人通过连接发现对方的所有信息,以及与对方的业务有关或与对方有关的信息(包括财务信息,产品,服务,服务水平,客户满意度,提议的服务和产品,定价和利润率),或者(包括董事或合作伙伴或合作伙伴,投资者,员工,员工,员工,供应商,客户,客户,客户,客户,客户,客户,客户,客户,客户和承包商)。但是,机密信息不包含当事方公开发布的信息,也不包含在不违反我们各自的机密义务的情况下公开获得的信息。数据隐私法是指2018年《数据保护法》将2016/679的欧盟一般数据保护条例纳入英国法律,以及2003年的隐私和电子通信(EC指令)法规,并不时修改或替换。付款,付款仅在我们在帐户中收到清算资金时才发生。个人数据是指有关可识别活人的信息。数据处理表是指您签发并由我们同意的数据处理协议,或者您填写的数据处理表格,设置了预订所需的个人和其他数据处理的框架,以及我们决定在我们之间讨论后决定实施的任何抵押数据处理协议。材料是指在或支持提供服务的过程中使用或生产的书面,音频和视觉材料,包括讲义,视频,问卷,游戏,案例研究,解释性材料,注释,计算,规格,报告,设计,设计,图纸,流程图,计划,计划,计划,计划,计划,参考材料,参考材料,原型。
最终场地/分区规划/修订清单
a. 一份已盖章的已批准的报价声明和分析的副本(如适用)(平面图); b. 一份已盖章的已批准的特殊用途许可条件和分析的副本(平面图); c. 一份并行处理表(如果申请在提交时属于豁免请求、重新分区、报价修订和/或特殊用途申请的主题)(平面图) d. 一份规划委员会决议或规划总监的合规性决定的副本(如果申请需要公共设施审查)(平面图) e. 任何已批准的与申请有关的变更、豁免或协议书的副本(平面图); f. 已批准的 GDP 的副本; g. 一份单价表的副本(平面图); h. 已签名并盖章的交通影响分析(小册子); i. 岩土报告(小册子)
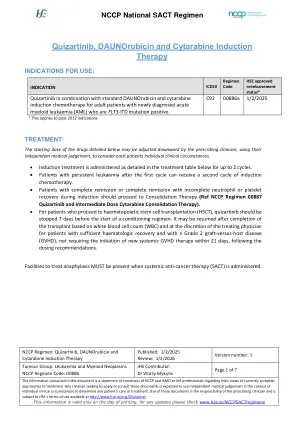
886-quizartinib-daunorubicin and-cytarabine诱导 -
诱导治疗是在下面的处理表中详细介绍的,最多2个周期。第一个周期后患有持续性白血病的患者可以接受第二个诱导化疗周期。在诱导过程中,患有完全缓解或完全缓解的患者应进行巩固治疗(参考NCCP方案00887 Quizartinib和中等剂量的细胞蛋白滨固结疗法)。对于继续进行造血干细胞移植(HSCT)的患者,应在调节方案开始前7天停止Quizartinib。 可以根据白细胞计数(WBC)完成移植后恢复,并由治疗医师自行决定,患有足够的血液恢复并患有≤2级移植物 - 主疾病(GVHD)的患者,不需要在21天内进行新的全身GVHD治疗,并不需要在21天内进行启动。对于继续进行造血干细胞移植(HSCT)的患者,应在调节方案开始前7天停止Quizartinib。可以根据白细胞计数(WBC)完成移植后恢复,并由治疗医师自行决定,患有足够的血液恢复并患有≤2级移植物 - 主疾病(GVHD)的患者,不需要在21天内进行新的全身GVHD治疗,并不需要在21天内进行启动。
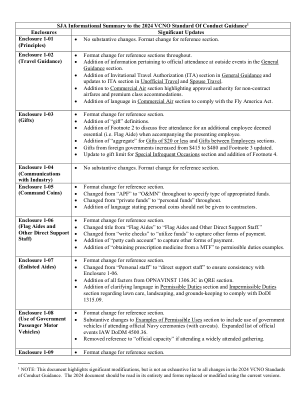
SJA 摘要表 2024 VCNO 行为标准。......
• 更改参考部分的格式。 • 在关键概念部分添加有关正式出席外部活动的信息。 附录 AH • 附录 A(旅行工作表):修改表格格式和所需信息,包括会议文件、与国旗事务的协调以及在国家首都地区使用租车的理由。 • 附录 B(礼品处理表):修改表格格式。外国政府礼品从 415 美元更改为 480 美元。将道德顾问签名移到最终礼品处理部分之前,并增加了一个评论框。 • 附录 C(事件审查表):修改表格格式。将名称从“协议事件审查表”更改为“事件审查表”,以鼓励在更多活动中使用。自动计算 100% ORF 事件以确定表格内的比率。 • 附录 D(日程审查表):修改表格格式。 • 附录 E(外国事件的法律审查):无变化。 • 附录 F(外部会议申请表):无变化。 • 附录 G(备案备忘录):无变化。• 附录 H(年度道德审计清单):在演讲活动/对非联邦实体 (NFE) 的支持部分下添加了与 NFE 进行官方活动的标记事项/DNS 通知或 JS 批准。
COVID 19 疫苗实施工作组诊所参考标题:COVID-19 疫苗辉瑞 COMIRNATY™ 免疫者快速参考领域:参考
COVID 19 疫苗实施工作组诊所参考标题:COVID-19 疫苗辉瑞 COMIRNATY™ 免疫者快速参考领域:免疫者参考生效日期:2021 年 11 月 25 日(儿科制剂)、2022 年 10 月 7 日(二价制剂)、2022 年 10 月 21 日(婴儿制剂)、2022 年 12 月 1 日(12+ 单价制剂)12 月 9 日(儿科二价)修订日期:2022 年 12 月 12 日批准人:FINAL 辉瑞 COMIRNATY TM 疫苗适用于主动免疫 2019 冠状病毒病 (COVID-19) 免责声明:本快速参考并非旨在取代其他产品特定疫苗参考。该文件旨在提供经常参考信息的快速参考。有关所有当前和完整的信息,请参阅产品专论和其他辉瑞 COMIRNATY TM 特定资源。其他资源: 产品专论:https://www.gov.mb.ca/asset_library/en/covidvaccine/pfizer-biontech-pm.pdf 二价产品专论:https://www.gov.mb.ca/asset_library/en/covidvaccine/pfizer-cominarty-bivalent-ba4-5-pm.pdf 资格标准:有关基础系列和加强剂量资格标准的最新信息,请参阅马尼托巴省 | 资格标准 (gov.mb.ca)。 加拿大免疫指南:有关特殊人群的指导,请参阅加拿大免疫指南。 情况说明书:有关疫苗风险和预期收益的信息,请参阅省级 COVID-19 情况说明书 文件表格摘要: 表 1:额外剂量建议:免疫功能低下 表 2:额外剂量建议:未经加拿大卫生部批准 表 3:马尼托巴省卫生部根据年龄推荐的 mRNA 免疫接种时间表。表 4:马尼托巴省批准的 COVID-19 疫苗的储存和处理表 5:双价疫苗注意事项