XiaoMi-AI文件搜索系统
World File Search SystemComirnaty® Original/Omicron BA.4-5 (托齐纳曼/...
Comirnaty 加强剂量对 65 岁及以上人群的安全性基于研究 C4591001 中 12 名 65 至 85 岁加强剂量接受者、研究 C4591001 中 306 名 18 至 55 岁加强剂量接受者以及研究 C4591031 中 1,175 名 65 岁及以上加强剂量接受者的安全性数据。Comirnaty Original/Omicron BA.4- 5 作为 65 岁及以上人群的第二次加强剂量的安全性基于 C4591044 中 159 名 65 岁及以上加强剂量接受者和 35 名 75 岁及以上加强剂量接受者的安全性数据。 Comirnaty 加强剂量对 65 岁及以上人群的有效性基于研究 C4591001 中 306 名 18 至 55 岁加强剂量接受者的有效性数据,以及研究 C4591031 中 9,945 名 16 岁及以上参与者的功效分析。
JAYPIRCA(吡托替尼):首个用于治疗复发/复发性套细胞淋巴瘤的非共价布鲁顿酪氨酸激酶抑制剂
产品特性简要概述 ▼ 该药品尚需进一步监测。这将允许快速获取新的安全信息。我们要求医疗保健专业人员报告任何疑似不良反应。有关报告不良反应的详细信息,请参阅产品特性完整摘要的第 4.8 节。 JAYPIRCA 100 毫克和 50 毫克薄膜包衣片:Jaypirca(吡托替尼)是一种抗癌药物,是布鲁顿酪氨酸激酶的非共价抑制剂。成分:每片薄膜包衣片含100毫克或50毫克吡托替尼(辅料为乳糖一水合物)。适应症:作为单一疗法,用于治疗既往接受过布鲁顿酪氨酸激酶抑制剂治疗的复发或难治性套细胞淋巴瘤成年患者。剂量和用法:建议剂量为每天一次 200 毫克,每天大约同一时间服用。应将药片整个吞下,无论是否进食。治疗应持续至病情进展或出现不可接受的毒性。如果患者呕吐或漏服药物,应按预定时间服用下一剂,而不要服用额外剂量。如果出现以下任何一种情况,应暂停使用 Jaypirca,直至症状缓解至 1 级或恢复至基线水平:伴有发烧和/或感染的 3 级中性粒细胞减少症、持续 ≥7 天的 4 级中性粒细胞减少症、伴有出血的 3 级血小板减少症、4 级血小板减少症、3 级或 4 级非血液学毒性。无症状淋巴细胞增多症不被视为不良反应,患者应继续服用 Jaypirca。在一项临床研究中,有限数量的患者通过减少剂量来控制不良事件。无需根据年龄以及轻度、中度或重度肾功能或肝功能不全患者调整剂量。目前尚无关于该产品对儿童和青少年(<18岁)的安全性和有效性的数据。吡托替尼过量服用的症状尚未确定,且无针对吡托替尼过量服用的特定治疗方法。若发生药物过量的情况,应密切监测患者并给予适当的支持治疗。禁忌症:对活性物质或任何赋形剂过敏。特别警告:接受治疗的患者中曾出现严重感染,包括死亡病例。对于机会性感染风险较高的患者,应考虑进行预防性抗菌治疗。根据感染的严重程度以及是否伴有中性粒细胞减少症,可能需要中断产品的给药。接受治疗的患者,无论是否伴有血小板减少症,都曾发生过出血事件,包括致命病例。应监测患者是否出现出血的体征和症状。与 Jaypirca 共同使用时,应权衡抗凝或抗血小板治疗的风险和益处,并应考虑额外监测出血迹象。尚未评估 Jaypirca 与华法林或其他维生素 K 拮抗剂的使用效果。如果发生 3 级或 4 级出血事件,应停止使用该产品。根据手术类型和出血风险,应考虑手术前后 3 至 5 天暂停使用 Jaypirca 的利益风险平衡。接受治疗的患者出现过 3 级或 4 级血细胞减少症,包括中性粒细胞减少症、贫血和血小板减少症;治疗期间应根据临床指征监测全血细胞计数。根据血细胞减少的程度,可能需要中断产品的给药。在接受治疗的患者中观察到心房颤动/扑动,特别是有心房颤动病史和/或多种心血管合并症的患者。应监测心房颤动和心房扑动的症状,并根据临床指征进行心电图检查。根据心房颤动/扑动的程度,可能需要停用该药物。接受治疗的患者中经常观察到其他原发性恶性肿瘤,最常见的是非黑色素瘤皮肤肿瘤。应监测患者是否患有皮肤癌,并建议他们保护自己避免日晒。罕见的是,Jaypirca 治疗期间曾报告出现肿瘤溶解综合征 (TLS)。罹患 TLS 风险较高的患者是治疗前肿瘤负担较高的患者。应评估患者是否有潜在的 TLS,并根据临床指征进行密切监测。患有半乳糖不耐症、完全乳糖酶缺乏症或葡萄糖-半乳糖吸收不良的患者不应服用此药。该产品1片含钠量少于1mmol。相互作用:与 CYP3A 抑制剂一起使用时,Jaypirca 无需调整剂量;如果可能,避免同时使用强 CYP3A 诱导剂(例如利福平、卡马西平、苯妥英)。当与质子泵抑制剂共同使用时,吡托替尼的药代动力学没有临床显著差异。吡托替尼可能会增加 CYP2C8 底物、BCRP 底物、P-gp 底物、CYP2C19 底物和 CYP3A 底物的血浆浓度。如果无法避免与 CYP2C8 底物(例如瑞格列奈、达塞布韦、司来帕、罗格列酮、吡格列酮和孟鲁司特)、治疗指数较窄的 BCRP 底物(例如高剂量甲氨蝶呤、米托蒽醌)、治疗指数较窄的 P-gp 底物(例如达比加群酯和地高辛)、治疗指数较窄的 CYP2C19 底物(例如苯巴比妥和美芬妥英)和治疗指数较窄的 CYP3A 底物(例如阿芬太尼、咪达唑仑、他克莫司)共同给药,则应考虑进行仔细的临床监测。生育能力、妊娠和哺乳:目前还没有关于吡托替尼对人类生育能力影响的数据。吡托替尼给孕妇服用可能会对胎儿造成伤害。怀孕期间不应使用 Jaypirca。育龄妇女在治疗期间以及服用最后一剂 Jaypirca 后 5 周内必须使用可靠的避孕方法。建议男性采取有效的避孕措施,并且在治疗期间以及服用最后一次 Jaypirca 后 3 个月内不要生育孩子。在治疗期间以及服用最后一剂 Jaypirca 后一周内应停止母乳喂养。对驾驶和使用机器能力的影响:Jaypirca 对驾驶或使用机器的能力有轻微影响。一些患者在使用 Jaypirca 治疗期间报告出现疲劳、头晕和乏力等症状,在评估驾驶和使用机器的能力时应考虑到这些情况。不良反应:各级别最常见的不良反应是疲劳(26.3%)、中性粒细胞减少症(22.8%)、腹泻(22.1%)和挫伤(19.0%)。最常见的严重(≥3级)不良反应是:中性粒细胞减少症(19.7%)、贫血(7.9%)和血小板减少症(6.6%)。 11.3% 的患者出现了与 Jaypirca 相关的严重不良反应,最常见的严重不良反应(发生在 ≥1% 的患者中)是肺炎(4.7%)、中性粒细胞减少症(2.2%)、贫血(1.7%)和泌尿道感染(1.0%)。 0.3% 的患者(2 名患者)因肺炎出现致命不良反应,0.1% 的患者(1 名患者)因出血出现致命不良反应。包装、调剂和付款:每包28、30或84片50毫克薄膜包衣片,或每包28、30、56、60、84或168片100毫克薄膜包衣片(PCTFE/PVC泡罩包装,铝箔密封)。市场上有售 28 片 100 毫克片剂的包装。该产品仅凭处方购买,不属于公共医疗保险覆盖范围。储存条件:不需要任何特殊的储存条件。营销授权持有人:Eli Lilly Nederland BV,Papendorpseweg 83, 3528 BJ Utrecht,荷兰。营销授权号及文本最后修订日期:EU/1/23/1738/001-009; 8.10. 2024 在开具产品处方前,请仔细阅读完整的产品特性摘要。产品特性概要的全文可从 VPOIS spol 网站获得。 Lilly:https://www.lilly.cz/cs/produkty/vpois.aspx 或地址:ELI LILLY ČR, sro, Pobřežní 394/12, 186 00 Prague 8,电话:234 664 111中性粒细胞减少症(22.8%)、腹泻(22.1%)和挫伤(19.0%)。最常见的严重(≥3级)不良反应是:中性粒细胞减少症(19.7%)、贫血(7.9%)和血小板减少症(6.6%)。 11.3% 的患者出现了与 Jaypirca 相关的严重不良反应,最常见的严重不良反应(发生在 ≥1% 的患者中)是肺炎(4.7%)、中性粒细胞减少症(2.2%)、贫血(1.7%)和泌尿道感染(1.0%)。 0.3% 的患者(2 名患者)因肺炎出现致命不良反应,0.1% 的患者(1 名患者)因出血出现致命不良反应。包装、调剂和付款:每包28、30或84片50毫克薄膜包衣片,或每包28、30、56、60、84或168片100毫克薄膜包衣片(PCTFE/PVC泡罩包装,铝箔密封)。市场上有售 28 片 100 毫克片剂的包装。该产品仅凭处方购买,不属于公共医疗保险覆盖范围。储存条件:不需要任何特殊的储存条件。营销授权持有人:Eli Lilly Nederland BV,Papendorpseweg 83, 3528 BJ Utrecht,荷兰。营销授权号及文本最后修订日期:EU/1/23/1738/001-009; 8.10. 2024 在开具产品处方前,请仔细阅读完整的产品特性摘要。产品特性概要的全文可从 VPOIS spol 网站获得。 Lilly:https://www.lilly.cz/cs/produkty/vpois.aspx 或地址:ELI LILLY ČR, sro, Pobřežní 394/12, 186 00 Prague 8,电话:234 664 111中性粒细胞减少症(22.8%)、腹泻(22.1%)和挫伤(19.0%)。最常见的严重(≥3级)不良反应是:中性粒细胞减少症(19.7%)、贫血(7.9%)和血小板减少症(6.6%)。 11.3% 的患者出现了与 Jaypirca 相关的严重不良反应,最常见的严重不良反应(发生在 ≥1% 的患者中)是肺炎(4.7%)、中性粒细胞减少症(2.2%)、贫血(1.7%)和泌尿道感染(1.0%)。 0.3% 的患者(2 名患者)因肺炎出现致命不良反应,0.1% 的患者(1 名患者)因出血出现致命不良反应。包装、调剂和付款:每包28、30或84片50毫克薄膜包衣片,或每包28、30、56、60、84或168片100毫克薄膜包衣片(PCTFE/PVC泡罩包装,铝箔密封)。市场上有售 28 片 100 毫克片剂的包装。该产品仅凭处方购买,不属于公共医疗保险覆盖范围。储存条件:不需要任何特殊的储存条件。营销授权持有人:Eli Lilly Nederland BV,Papendorpseweg 83, 3528 BJ Utrecht,荷兰。营销授权号及文本最后修订日期:EU/1/23/1738/001-009; 8.10. 2024 在开具产品处方前,请仔细阅读完整的产品特性摘要。产品特性概要的全文可从 VPOIS spol 网站获得。 Lilly:https://www.lilly.cz/cs/produkty/vpois.aspx 或地址:ELI LILLY ČR, sro, Pobřežní 394/12, 186 00 Prague 8,电话:234 664 111cz/cs/produkty/vpois.aspx 或联系地址:ELI LILLY ČR, sro, Pobřežní 394/12, 186 00 Prague 8,电话:234 664 111cz/cs/produkty/vpois.aspx 或联系地址:ELI LILLY ČR, sro, Pobřežní 394/12, 186 00 Prague 8,电话:234 664 111
OPM 7300 T23 G05 Parsons Winter 2024.pdf
领土承认 曼尼托巴大学的校园和设施位于阿尼希那贝格人、克里人、奥吉克里人、达科他人和德内人的原始土地上,也是梅蒂斯民族的故土。我们尊重在这些领土上签订的条约,我们承认过去的伤害和错误,我们致力于本着和解与合作的精神,与土著社区合作前进。 曼尼托巴大学要求对领土进行普遍承认,但在许多课程中,比如这门课程,讨论与课程的直接联系更为重要。 曼尼托巴省的一个重要特点是其土著公民比例在加拿大所有省份中最高,接近五分之一的曼尼托巴人。因此,土著公民对整个曼尼托巴省的经济未来至关重要。具体来说,关于这门课程,在过去大约 350 年的时间里,原住民和梅蒂斯人构成了世界上最重要的供应链之一的核心部分,这个供应链对于后来的马尼托巴省也具有重要意义。这个供应链也导致了各种重大的不利影响。所有学生都应该提前考虑的问题是,这个供应链是什么,它涉及什么?我们将在课堂上讨论这些有趣的观点。
我们塑造清洁空气的未来 - 尼的曼集团
Nederman 的 MCP 过滤器是我们 SmartFilter 系列的最新成员。与此同时,我们正在逐步淘汰我们忠实的产品之一 FMC。这也标志着一项大型能力和物流计划的开始,以波兰 Marki 的制造部门为中心。通过将 MCP 生产集中在那里,我们不仅获得了规模经济,而且还获得了额外的竞争力。通过重组物流链,我们同时减少了二氧化碳排放量并加强了我们在运输领域的可持续发展。Marki 也将成为我们自动化能力中心的所在地。经过此次变更,德国弗里森海姆将成为 FS 过滤器的 EMEA 制造中心,并具有相应的效率和环境效益。
圣塔曼尼教区幼儿网络
*hwv wr d vlwlqj srvllrrq e \ khuvhoi 0ryhv wklqv iurp rqh rqh kdqg wr khu rwkhu rwkhu kdqg 8vhv i ilqjjuv wr w wr wr w w w w w w w w wr 6lwv zlwkrxw vxssruw,w¶vw¶vwlphiru ghyhorsphwdo vuhqlqjj $ wqwkv \ rxu ede \ lv gxh iru jhqudo jhqudo ghyhorsqwdo vfuhqlqj dv uhfrpphqggggggg iru doo fkloguhq e \ wkh $ phulldq $ fdghp \ ri 3hgldwoulfv $ vn wkh grfru derxw \ rxu derxu \ rxu ede \ rxu ede \〜 div>
马尼托巴司法中心:温尼伯法院编号 CI24-01-...
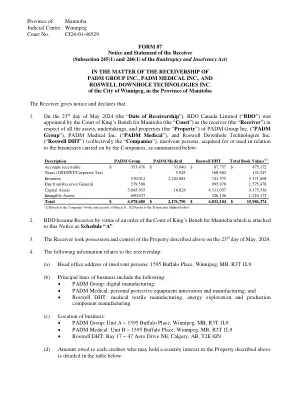
2. 根据马尼托巴省王座法院的命令,BDO 成为接管人,该命令作为附表“A”附于本通知后。 3. 接管人于 2024 年 5 月 23 日占有并控制上述财产。 4. 以下信息涉及接管: (a) 破产人员总部地址:1595 Buffalo Place, Winnipeg, MB, R3T 1L9。 (b) 主要业务包括: • PADM Group:数字制造; • PADM Medical:个人防护设备创新与制造;以及 • Roswell DHT:医用纺织品制造、能源勘探和生产部件制造。
省级处方法规摘要图表-M3P-...
您可以在此处找到 M3P 药物清单。请注意,阿片类药物处方的实践标准如下: • 曼尼托巴省医师和外科医生学院 (CPSM) 《开具阿片类药物处方的实践标准》;以及, • 曼尼托巴省注册护士学院 (CRNM) RN(NP) 《开具治疗非癌症疼痛的阿片类药物处方》;以及, • 曼尼托巴省兽医协会 (MVMA) 章程第 1 号 (4-6-10 和 4-6-11) ,只允许开具最长三个月的处方,并且每次授权的调药量不得超过一个月。有关更多信息,请参阅 CPhM 配套文件。必须写在由授权医疗从业人员(医生、执业护士、牙医或曼尼托巴省执业兽医)签字并注明日期的 M3P 表格上。必须在 3 天内(除开具处方当天外)向药房出示 M3P 表格。不接受口头命令。
旅行者或“候鸟族”的注意事项:阿片类药物、苯二氮卓类药物/Z 类药物和虚拟医学实践标准
在患者旅行期间,曼尼托巴省的处方人员不能通过虚拟护理/电话为身在其他国家的曼尼托巴省患者提供医疗服务以更新或调整处方。CPSM 注册并不扩展到在该国提供医疗服务。同样,医疗责任保险可能不涵盖在另一个国家为患者提供护理的曼尼托巴省医师或 RN(执业护士)。同样,CPSM 注册也不扩展到在其他省提供医疗服务。想要在其他省提供医疗服务的曼尼托巴省执业医师需要了解并遵守该加拿大司法管辖区的许可和责任要求。RN(NP)应联系客户所在省/地区的监管机构,以确定他们是否需要在该司法管辖区注册,然后才能在该地为客户提供医疗保健服务。
新省无家可归战略的概述
•建立一个部门间工作组,以改善服务提供服务•温尼伯的协调访问和曼尼托巴省的住房应用程序•支持HIFI在曼尼托巴省的集成和扩展•开发沟通运动以解决污名•扩展住房的资金,为住房提供资金。