XiaoMi-AI文件搜索系统
World File Search System微生物类胡萝卜素生产:菌株、条件和产量影响因素
摘要:类胡萝卜素生产的研究和开发历史悠久,人们对这组色素的兴趣至今未减。现有的六种类胡萝卜素被认为具有工业重要性:虾青素、β-胡萝卜素、叶黄素、玉米黄质、角黄素和番茄红素。这些类胡萝卜素具有广泛的应用范围,由于其生物活性和着色特性,被用作食品和饮料、饲料、营养保健品、药品和化妆品中的添加剂。目前,全球色素市场以化学合成的类胡萝卜素为主。来自植物和微生物等天然来源的类胡萝卜素不那么受欢迎或普及。目前,天然类胡萝卜素市场主要由微藻雨生红球藻、盐生杜氏藻、布朗葡萄藻、真菌三孢布拉氏菌、红法夫酵母和细菌胡萝卜素副球菌代表。这些微生物产生虾青素、β-胡萝卜素、角黄素和番茄红素。红酵母、掷孢酵母、弹球酵母、戈登酵母和迪茨酵母属的几种酵母和细菌可能成为工业规模的类胡萝卜素来源,但现有技术仍需改进。本文综述了提高真菌和细菌类胡萝卜素生产竞争力的策略。考虑的策略包括选择产胡萝卜素菌株、使用低成本底物、通过添加微量元素、TCA中间体、NaCl、H 2 O 2 、光照来刺激类胡萝卜素的合成,以及优化pH、温度和通气等发酵条件。
儿童和青少年饮食补充剂的使用
抽象目标:评估儿童和青少年饮食补充剂的叙述性评论。数据来源:2000年至2023年之间,使用了PubMed,Medline和Scielo数据库中的“饮食补充剂”,“儿童”和“青少年”术语,该术语在PubMed,Medline和Scielo数据库中使用,评估了人类的研究,该研究发表在Portuguese,英语,法语,法语和西班牙语中。数据综合:近几十年来,儿童和青少年饮食补充剂的使用有所增加。最常用的补充剂是维生素,矿物质,微量元素,蛋白质,氨基酸,褪黑激素,脂肪酸,益生菌和能量饮料。结论:尽管有特定的指示,但大多数情况下,医疗保健专业人员没有开处方。使用的原因有所不同。在儿童中,主要原因是针对感染,刺激生长和食物摄入量不佳,多种维生素和矿物质是最常用的补充剂。在青少年中,它们用于改善运动表现并获得“理想的身体”,蛋白质和氨基酸是最常使用的营养素。由于它们不受卫生机构的监管,并且在没有预先措施的情况下出售,因此他们的无监督使用可能导致剂量不足,不耐用或过量的风险。至于复合配方,或者在有多种营养素的制剂中可用时,错误的机会会增加。至关重要的是,儿科医生向父母和患者提供有关适应症,风险和收益的建议,并在必要时开处方。©2023由Elsevier Editora Ltda发布。代表Sociedade Brasileira de Pediatria。这是CC BY-NC-ND许可证(http://creativecommons.org/licenses/by-nc-nd/4.0/)下的开放访问文章。
阿尔茨海默氏病的循环痕量元素变化
循环中的抽象痕量元素水平(血液,血清,血浆)被认为在阿尔茨海默氏病的病理生理过程(AD)中起作用;但是,可用发现中存在异质性。This study conducted a systematic review and meta-analysis of trace elements (including: copper (Cu), iron (Fe), zinc (Zn), selenium (Se), lead (Pb), cadmium (Cd), mercury (Hg), manganese (Mn), aluminum (Al), arsenic (As), and magnesium (Mg)) in AD patients and controls to assess the variation of trace AD患者循环中的元素。通过系统地筛选病例 - 对照研究对2000年至今的AD循环痕量元素水平在PubMed,Web of Science和Medline数据库中,最终荟萃分析中包括52项研究。随机效应模型的结果表明,CD的循环水平显着升高(SMD = 0.79,95%CI:0.35,1.24),Hg(SMD = 0.59,95%CI:0.03,1.16)和CU(SMD = 0.70,95%CI:0.37:0.37,1.37,1.04),同时,pec:0.37,1.0 r级别。 CI: - 1.03, - 0.13),SE(SMD = - 0.53,95%CI: - 0.85, - 0.21)和Zn(SMD = - 0.99,95%CI: - 1.52,-0.46)显着降低。本研究中形成的数据库为探索AD患者循环元素水平的变化提供了可靠的基于人群的研究证据。对老年人的循环痕量元素水平的监测和稳定可能是AD的潜在预防靶标。关键词阿尔茨海默氏病,病例对照研究,微量元素,循环系统
Aphanizomenon flos -aquae的商业潜力,A ...
摘要Aphanizomenon flos-aquae(AFA)是一种革兰氏阴性氮固定的淡水淡水丝状蓝细菌,具有丰富的营养概况,可通过食品和药物管理局和欧洲食品和安全当局批准人类消费。它具有较高的蛋白质含量(60-70%),并含有许多维生素,矿物质和微量元素,以及具有营养特性的几种高价值化合物,例如C-磷酸和β-苯基乙胺。AFA干生物量的500-1000吨目前是从季节性在美国俄勒冈州克拉马斯湖季节性出现的自然花朵收获的,并在全球范围内作为营养补充剂分发。由于AFA增长对环境条件的依赖性和微囊藻毒素毒素的潜在污染,野生收获的要求和不可靠性威胁到生物质供应的可用性并限制了商业扩张。在这篇综述中,我们建议在开放池或封闭的光生反应器中培养AFA培养,以获得可靠的Unialgal生物量生产以解决供应问题并增强AFA作为特定高价值副产品的原料。此外,我们通过使用耕种和野生收获的协同组合来探索最大化总体产量和季节性鲁棒性的潜在策略。受控的AFA培养还将促进使用遗传操纵来产生具有改善商业应用的定制菌株,例如增加氰基杆菌的氮固定速率,以提高其作为生物肥料的价值。最终,实现AFA的未开发的生物技术潜力,需要更好地了解其基本生物学,实验室和大规模培养的强大方法以及AFA特异性基因工程技术的发展。
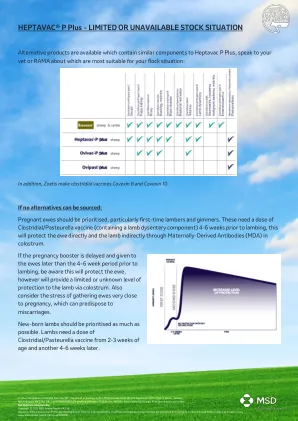
HEPTAVAC® P Plus – 库存有限或缺货情况
• 减少压力——压力会导致梭菌病和巴氏杆菌病。压力可能由聚集、处理、施用产品或药物、混合群体、移动、天气突然变化、担心狗等引起。 • 营养充足——动物应保持良好的身体状况,但不能肥胖。营养突然变化会导致患病,因此应逐步进行任何变化。 • 避免过去绵羊曾患过梭菌病或巴氏杆菌病的田地/环境——一些梭菌细菌生活在土壤中,似乎与某些田地更相关。被扰动的土壤会增加风险,因此避免在田地中进行地基工程等。秋季将绵羊转移到甜菜或其他饲料作物上也会增加患病风险。 • 确保动物健康——确保它们没有蠕虫,跛行得到控制,在有风险的地方控制吸虫,并且它们没有患有任何其他可能降低其免疫力的疾病(例如 MV、Johnes、CLA、Orf、OPA)。• 良好的卫生条件——在产羔时,所有设备和人员都应一丝不苟地清洁,羔羊肚脐必须浸湿,标记、断尾和阉割必须按照最高标准进行。• 良好的初乳管理——羔羊在出生后的前 24 小时内必须接受 200ml/kg 的初乳,并且在出生后的 2-4 小时内必须喂食 200ml。• 管理环境——如果动物在室内;干净的垫料,定期更换,充足干净的淡水,充足的营养且易于获取,不拥挤,通风良好,脚下干燥。如果羊在室外;确保围栏符合良好标准,并且草不会被吃掉,只剩下裸露的土壤 - 如果需要,提供补充营养。 • 管理微量元素 - 可以进行血液测试以确定缺陷并提供补充剂。
含 Triton X-100 的李氏肉汤
20 世纪 40 年代早期,Weber 和 Black 建议使用卵磷脂和聚山梨醇酯来中和季铵化合物的抗菌作用 (6)。1965 年,AOAC 认可该方法用于抗菌测定,并将其应用扩展到所有阳离子洗涤剂。1978 年,FDA 将其作为每次化妆品微生物检查的预增菌培养基。化妆品的化学成分很有可能通过生物体的新陈代谢而改变,从而导致化妆品变质并对使用者造成伤害 (1,5,7)。直接菌落计数和增菌培养是从化妆品中分离微生物的首选方法。Letheen 这个词代表卵磷脂和聚山梨醇酯 (tween) 80 的组合。建议使用含有 Triton X-100 的 Letheen 肉汤来检测酵母和霉菌,因为这种肉汤可以让大多数生物大量生长。 Triton X-100 是非离子型的,可分散微生物,使计数更容易。蛋白胨、HM 蛋白胨 B 为微生物提供含氮营养物质、碳化合物和微量元素。在培养基中加入卵磷脂和聚山梨醇酯 80 可以从含有化妆品中使用的消毒剂或防腐剂残留物的材料中回收细菌。加入聚山梨醇酯 80 可消除酚类化合物、六氯酚和福尔马林,并与卵磷脂一起中和乙醇 ( 2 )。卵磷脂还可以中和化妆品中的季铵化合物。氯化钠可维持培养基的渗透平衡。Triton X-100 可用作表面活性剂。化妆品中含有防腐剂,在接种过程中应至少部分灭活,而该培养基有助于稀释和中和。
应用土壤生态学
将覆盖作物实施到农作物轮作中可以有助于更可持续的土壤管理。为了改善覆盖作物残留物的分解,越来越多地应用了商业接种剂有效的微生物®(EM)。尽管有广泛的应用,但缺乏对EM应用对土壤过程的影响的全面研究,因为很少有效应(直接直接通过EM诱导)或底物效应(由随附的EM底物引起的)清晰的区分。为了确定覆盖土壤覆盖作物融合后EM应用的潜在影响,我们在温带气候下在类似春季的条件下进行了实验室孵育实验,并在建议的裸露土壤或覆盖作物上施加了EM在建议的土壤掺入之前,并在建议的100倍的剂量上施加。对照组包括没有EM添加的治疗方法,并以建议剂量的100倍施用了无菌EM溶液。在28天的监测期内,EM在建议的剂量上的应用对土壤呼吸,微生物结合的碳或氮,土壤pH,大陆基糖氧化氧化碳或可萃取的养分和微量元素没有一致的影响。在接受100倍推荐剂量的100倍的治疗中观察到的效果归因于EM溶液引入的底物,而不是活着的EM本身。扩增子测序表明,在施用后,可以在低丰度中在土壤中检测到某些EM分类单元,但只有在推荐剂量的100倍施用EM时。我们得出的结论是,EM的应用不会对土壤生物学或化学特性产生明显的影响,也没有影响覆盖作物的分解过程。
紫色红胆葡萄糖琼脂板(统一)
紫罗兰色胆汁葡萄糖琼脂板(统一的)预期用途紫罗兰红胆汁葡萄糖琼脂板(统一)用于根据usp/ep/ep/ep/bp/jp/jp/jp/jp/ip/anconized方法来隔离和培养药物的肠杆菌科。摘要肠杆菌科包括乳糖发酵大肠菌菌,大肠杆菌的非乳糖发酵菌株以及其他参与食物损坏的沙门氏菌和志贺氏菌的非乳糖发酵物种。由于食品和乳制品的潜在污染,很重要的是检测肠杆菌科的成员而不是传统的大肠菌菌细菌。紫色红胆葡萄糖琼脂板(统一)是紫罗兰色琼脂的修饰。mossel等人,通过添加葡萄糖,修饰含有紫罗兰色胆汁琼脂的乳糖。Mossel等人的进一步工作表明,可以省略乳糖,从而导致紫罗兰色胆汁葡萄糖琼脂的制定。在培养基中,葡萄糖均由肠杆菌科的所有成员发酵,因此紫罗兰色胆汁葡萄糖琼脂(VRBGA)具有假定的肠杆菌科。VRBGA用于列举食品样品中的肠杆菌科。酪蛋白和酵母提取物的原理胰腺消化物提供营养,氨基酸,碳化合物,维生素B复合物,矿物质和微量元素。葡萄糖是一种能源。胆汁盐和晶体紫抑制革兰氏阳性细菌。中性红色是pH指示器。琼脂是固化。其他材料所需的细菌孵化器。使用指令配方 *成分G/L明胶7.0酵母提取物的胰腺摘要3.0葡萄糖一水合物10.0胆汁盐1.5氯化钠5.0中性红色0.03 Crystal Viret 0.002 Crystal Violet 0.002琼脂15.0 *调整以适应适合性能参数。
肠道菌群和甲状腺疾病的最新进展
本综述综合了过去五年实验文献中的关键发现,阐明了肠道微生物组对甲状腺疾病发病机理的重要影响。一直观察到肠道菌群组成的明显转移,细菌(例如双杆菌,芽孢杆菌,芽孢杆菌,巨蛋白酶和梭状芽胞杆菌)的细菌显着降低,细菌的显着增加,包括细菌,包括细菌,proteebacteria,proteeabacteria,actacinobacteria,blebactia,kle and kle and kle and kle and kle and kle and kle and kle and and and anderaTia and kle。这些改变与包括胆汁酸和细胞因子的产生在内的代谢途径(包括降低短链脂肪酸(SCFA)(SCFA),这对于免疫调节和甲状腺激素稳态至关重要,这与甲状腺疾病的发展和进展有关。该评论还强调了益生菌在管理甲状腺条件中的治疗意义。证据表明,益生菌辅助治疗可以调节肠道菌群,从而改善甲状腺功能和患者结局。使用特异性益生菌菌株(例如lactiplantibacillus plantarum 299V和双杆菌长杆菌)在增强传统治疗的作用方面表现出了潜力,并可能恢复了平衡的肠肌菌群。值得注意的是,粪便菌群移植(FMT)已成为对Graves疾病(GD)的有前途的干预,证明了重新校准肠道菌群的潜力,从而通过gut-Brain-brain-Brain and Gut-thyroid-ater-thyroid Axes侵蚀神经递质和微量元素。将基于微生物组的疗法与传统疗法的整合可以吸引个性化甲状腺疾病管理的新时代,从而提供了更细微的患者护理方法。通过整合这项工作,该评论对肠道微生物组对甲状腺疾病的广泛影响和益生菌的治疗应用提供了创新的观点。
国家现状和采样与分析方法...
3.2.3.1.3.现场收集变化............................................... I.26 3.2.3.2.包装 .............................................................................. I.27 3.2.3.2.1.东海岸和西海岸 ........................................................ I.27 3.2.3.2.1.1.有机样品............................................. I.27 3.2.3.2.1.2.主要和微量元素样品 ......... I.27 3.2.3.2.2.墨西哥湾沿岸............................................................. I.27 3.2.4.辅助测量......................................................................... I.28 3.2.4.1.潮汐水平线...................................................................... I.28 3.2.4.2.深度............................................................................... I.29 3.2.4.3.海洋帕金斯虫............................................................. I.29 3.2.4.4.贝壳大小....................................................................... I.29 3.2.4.5.放射性核素样本....................................................... I.29 3.2.4.6.粪甾烷醇和产气荚膜梭菌............................................. I.29 3.2.4.7.性腺指数....................................................................... I.29 3.2.4.8.温度....................................................................... I.30 3.2.4.9.盐度 ................................................................................ I.30 4.质量保证 ................................................................................................ I.30 4.1.方法............................................................................................. I.30 4.1.1.方法论 .................................................................................... I.30 4.1.2.标准参考和控制材料............................................................. I.30 4.1.3.程序和标准............................................................................. I.31 4.1.4.仪器校准............................................................................. I.31 4.1.5.样品定量 ............................................................................. I.31 4.1.6.方法检测限................................................................................. I.31 4.1.7.精度............................................................................................... I.31 4.1.8.准确性................................................................................................ I.32 4.2.对照样品............................................................................................... I.32 4.3.数据可接受性标准和存档........................................................................ I.33 4.4.比对练习............................................................................................. I.33 4.5.质量保证研讨会......................................................................................... I.33 4.6.标准参考材料的开发............................................................................. I.33 4.7.NIST 痕量有机练习............................................................................. I.33 4.8.NRC 痕量元素练习............................................................................. I.34 5.分析程序............................................................................................. I.34 5.1.介绍................................................................................................................ I.34 5.1.1.痕量有机物............................................................................................... I.34 5.1.2.常量和痕量元素............................................................................... I.34 5.2.分析物限制讨论................................................................................. I.34 5.2.1.有机分析物....................................................................................... I.34 5.2.1.1.PCB............................................................................. I.34 5.2.1.1.1.PCB 定量....................................................... I.34 5.2.1.1.2.PCB 选择............................................................. I.35 5.2.1.1.3.PCB 共洗脱物............................................................... I.36 5.2.1.2.PAHs............................................................................... I.36 5.2.2.无机分析物............................................................................... I.39 5.2.2.1.铊 ............................................................................. I.39 5.2.2.2.锑............................................................................. I.39 5.2.2.3.硒............................................................................. I.40 5.2.2.4.NEFSC 沉积物元素分析............................. I.41锡 .................................................................................... I.40 5.3.分析物添加............................................................................................... I.40 5.4.国家底栖生物监测项目分析方法............................................... I.41 5.4.1.无机分析................................................................................. I.41 5.4.1.1 沉积物............................................................................... I.41 5.4.1.1.1.