XiaoMi-AI文件搜索系统
World File Search System总统特布布恩接待了非洲的指挥官
军队将军说,国防部长的代表Chanegriha昨天在ANP总参谋部总部总部收到了国防部总部的总部,美国非洲司令部(US-AFRICOM)司令官迈克尔·兰格利(Michael Lan-Gley)表示,美国国防部的一份声明。接待仪式是由国旗的救赎开始的,随后是军事荣誉,由ANP的各种力量形成给了Armee Michael Langley。在这次会议上参加了国防部秘书长,部队指挥官,部门负责人,国防部的中央董事和ANP的主要主任以及美国代表团的成员以及两个政党的成员,“检查了双边武器合作的国家,并交换了同一点。随后,陆军将军发表讲话,他欢迎他“欢迎对非洲的指挥官和伴随他的代表团,以及在美国第47任总统安装后向美国人民朋友表示祝贺”。“首先,欢迎您来到阿尔及利亚并抓住这个机会表达我的梅尔 -
利妥昔单抗超敏反应:从临床表现到管理
利妥昔单抗是一种针对在人B细胞上表达的CD20分子的嵌合单克隆抗体(MAB)。它已用于治疗各种淋巴恶性肿瘤,淋巴增生性疾病和风湿病。利妥昔单抗通常耐受性良好。然而,利妥昔单抗的使用增加与超敏反应(HSR)有关,可以将其分类为输注相关,细胞因子释放,I型(IGE/非IgE),混合,III型和IV型反应。对利妥昔单抗的直接输注反应非常普遍,随后输注频率下降。然而,在约10%的患者中,出现了严重的输注反应,从而阻止了其使用。某些直接输注反应是由于细胞因子释放引起的,但某些反应引起了对I型(IgE/非IgE)超敏反应的关注。最近的研究表明,以IgG或IgE同型为代表的血清抗利妥昔单抗抗体存在。在某些情况下,IgE介导的反应和细胞因子释放反应的临床表现部分重叠,这称为混合反应。分类为III型反应,在自身免疫性疾病和血液学恶性肿瘤患者中已经报道了利妥昔单抗诱导的血清疾病反应。在主要具有潜在的风湿病状态的患者中,已经观察到经典的血清疾病三合会(发烧,皮疹和关节痛)。涉及利妥昔单抗引起的HSR的全面评论很少。严重的延迟IV型超敏反应,包括对史蒂文斯(Stevens)等严重反应的非严重性皮疹 - 约翰逊综合征和有毒的表皮坏死术后,rituximab注射后很少报道。我们旨在审查利妥昔单抗超敏反应的临床表现,潜在的机制以及包括快速药物脱敏的管理。
明智之选:利妥昔单抗、来那度胺和依鲁替尼治疗新诊断大 B 细胞淋巴瘤患者
方法 我们招募了 60 名新诊断的非生发中心 B 细胞样 DLBCL 患者,参与这项由研究者发起的单组 II 期临床试验,研究利妥昔单抗、来那度胺和伊布替尼 (RLI) 联合序贯化疗 (ClinicalTrials.gov 标识符:NCT02636322)。患者在每个 21 天周期 (RLI) 中接受利妥昔单抗 375 mg/m 2 静脉注射一次(第 1 天)、来那度胺 25 mg 每日一次(第 1-10 天)和伊布替尼 560 mg 每日一次连续治疗。两个周期后,在 RLI 中添加标准化疗,再进行六个周期。主要终点是两个周期单独 RLI 后的总体缓解率 (ORR) 和完成 RLI 联合化疗后的完全缓解率。在可评估样本中,进行了循环肿瘤 DNA 和 DLBCL90 检测。
维奈克拉和阿沃昔布均对耐阿糖胞苷和氯法拉滨的急性髓系白血病细胞具有细胞毒性
结果:新建立了 10 倍 ara-C 抗性的 HL-60 变异株、4 倍 CAFdA 抗性的 HL-60 变异株和 30 倍 CAFdA 抗性的 HL-60 变异株。这些变异株显示脱氧胞苷激酶和脱氧鸟苷激酶表达降低,但表面转运蛋白(hENT1、hENT2、hCNT3)表达完整。与非变异 HL-60 细胞相比,这些变异株细胞内核苷类似物三磷酸盐表达较低。这些变异株还过度表达 Bcl-2 和 Mcl-1。维奈克拉单药对耐药变异株无细胞毒性。然而,维奈克拉与核苷类似物联合使用对变异株有协同细胞毒性。Alvocidib 单药对细胞有细胞毒性。然而,alvocidib 诱导 G1 停滞并抑制同时给药的核苷类似物的细胞毒性。
Zanubrutinib 1 / 4
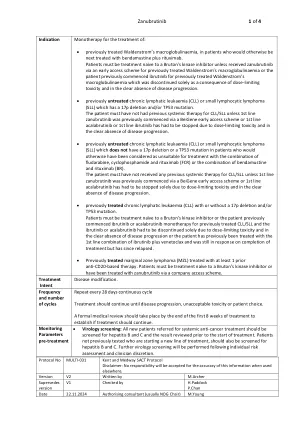
• 之前接受过治疗的华氏巨球蛋白血症患者,如果接受治疗,下一步将接受苯达莫司汀联合利妥昔单抗治疗。患者必须未接受过布鲁顿激酶抑制剂治疗,除非患者通过早期使用计划接受了赞布替尼治疗之前接受过治疗的华氏巨球蛋白血症,或之前开始使用伊布替尼治疗之前接受过治疗的华氏巨球蛋白血症,但停药仅是因为剂量限制性毒性,且疾病明显没有进展。• 之前未接受过治疗的慢性淋巴白血病 (CLL) 或小淋巴细胞淋巴瘤 (SLL),存在 17p 缺失和/或 TP53 突变。患者先前必须未接受过 CLL/SLL 的全身治疗,除非先前通过百济神州早期使用计划开始使用一线 zanubrutinib,或者由于剂量限制性毒性并且明显没有病情进展而必须停止使用一线 acalabrutinib 或一线 ibrutinib。• 先前未接受过治疗的慢性淋巴细胞白血病 (CLL) 或小淋巴细胞淋巴瘤 (SLL),没有 17p 缺失或 TP53 突变,这些患者原本被认为不适合使用氟达拉滨、环磷酰胺和利妥昔单抗 (FCR) 联合治疗或苯达莫司汀和利妥昔单抗 (BR) 联合治疗。患者既往未接受过任何针对 CLL/SLL 的全身治疗,除非之前通过 BeiGene 早期使用计划开始使用一线 zanubrutinib,或一线 acalabrutinib 仅因剂量限制性毒性且在明显无疾病进展的情况下必须停用。• 先前接受过治疗的慢性淋巴细胞白血病 (CLL),无论是否存在 17p 缺失和/或 TP53 突变。患者必须是未接受过布鲁顿激酶抑制剂治疗的患者,或患者之前已开始使用伊布替尼或阿卡替尼单药治疗先前接受过治疗的 CLL/SLL,并且仅因剂量限制性毒性且在明显无疾病进展的情况下必须停用伊布替尼或阿卡替尼,或患者之前曾接受过伊布替尼加维奈克拉的一线组合治疗,并且在完成治疗时仍有反应,但此后复发。 • 曾接受过至少 1 种抗 CD20 疗法治疗的边缘区淋巴瘤 (MZL)。患者必须未接受过布鲁顿激酶抑制剂治疗,或已通过公司准入计划接受过 zanubrutinib 治疗。治疗意向
替布索沃(ivosidenib)
北欧联合 HTA 机构 (JNHB) 前身为 FINOSE,最初是由芬兰、挪威和瑞典 HTA 当局自下而上发起的,于 2018 年在斯德哥尔摩启动。该合作将于 2023 年扩大到丹麦,2024 年扩大到冰岛。2024 年 6 月,FINOSE 更名,变为北欧联合 HTA 机构 (JNHB)。JNHB 为五个北欧国家提供高效透明的药品联合卫生技术评估。评估包括相对有效性和卫生经济学。价格和报销决定以及使用建议在每个国家的国家层面做出。通过合作和共享知识,JNHB 旨在制作高质量的评估报告,为国家决策提供坚实支持。合作的基础在 2024 年 4 月由合作 HTA 机构签署的谅解备忘录中概述;
巴布亚银行新几内亚
巴布亚银行新几内亚外汇交易商许可申请申请申请旨在协助申请人根据“许可要求”(第2部分)列出的外汇交易经销商许可证要求1的形式和详细信息准备和提交完整的申请。The Checklist is not a substitute for the requirements of the BFIA 2 .将tick放在每个项目旁边的空间(____)中。1。外汇业务计划(第2.1部分)(____)外汇业务计划的完整详细信息,包括要进行交易的货币(____)组织结构的全部详细信息(____),结合了外汇业务(____)管理结构,结合了外汇交易业务管理结构(____),显示了贸易,和解和信息交易所以及外汇企业的分离,并显示信息和会计系统(第2.2部分)(____)政策,显示有关要采用的信息类型和会计系统的足够详细信息3。通讯银行(第2.3)(____)外国记者银行的名称(____)与外国通讯银行(____)有关建立Nostro帐户的文献证据的交易安排的副本和详细信息的完整详细信息4。其他(____)申请费(第2.4部分)