XiaoMi-AI文件搜索系统
World File Search System基因组DNA提取试剂盒
•所有样品必须视为潜在的生物危害。戴上适当的防护眼镜,衣服和手套。•避免与套件试剂直接接触皮肤。如果接触,请立即用水彻底洗涤。•最小化化学物质的吸入。请勿打开化学容器。•出于安全原因,应在设备齐全的设施中进行所有工作(即物理控制设备)。•在使用潜在的传染性材料之前,应根据公司/机构的相关法规和要求对个人进行培训。
Roche无细胞DNA收集管
警告和预防措施●在6.5毫升血液加防腐剂溶液的最小填充线以下不应填充管。●在到期日期后不要使用产品。●请勿冷藏或冷冻。●避免将试剂与皮肤和粘膜接触。如果眼睛接触,请至少15分钟彻底用大量水冲洗。如果皮肤接触,请用肥皂和大量的水洗净。●将所有与它们接触的生物标本和材料视为生物危害。按照适当的谨慎操作,并根据您的设施的政策和程序处置。●练习通用预防措施。使用保护性个人设备和其他工程控制,以防止血液溅出,血液泄漏以及潜在暴露于血液传播病原体。●处理时要谨慎,以免掉落或破裂Roche无细胞的DNA收集管。●如果内容有多云或存在异物,请勿使用Roche无细胞的DNA收集管。●请勿使用Roche无细胞的DNA收集管来收集用于注射的材料。●由于未在Roche无细胞的DNA收集管上验证试样将样品转移到无针和注射器的无Roche细胞收集管中,因此请勿使用针和注射器将收集的样品转移到Roche无细胞收集管中。对尖锐的额外操纵会增加受伤的风险。●确保按照生物危害材料运输的所有要求,将收集的标本包装和标记。●安全数据表(SDS)可应要求提供。●将使用此设备时可能发生的任何严重事件通知您当地的主管当局和制造商。
生物风险管理政策(MPFXXX)草案
(a) 机构生物安全委员会 (IBC)(及任何相关小组委员会)通过审查、监督和监测对 IBC 监管活动进行内部监管;以及 (b) 为确保大学对生物风险管理计划进行适当监督而认为必要或可取的其他报告、治理和监督机构或职责,这些将在辅助要求中记录。 4.4. 大学采用合规方法来管理生物风险,符合更广泛的机构风险管理框架。根据本政策和辅助要求,识别和评估与生物危害相关的特定风险,并定义、授权、实施和监测控制措施。 4.5. 在大学与 RBM 合作的所有人员将:
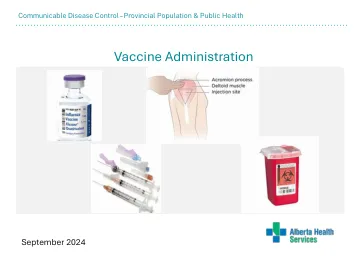
COVID-19疫苗:
尽管生化药物中使用的微生物不太可能引起健康个体感染,但它们确实有可能引起免疫功能低下的个体感染。bCG与免疫功能低下的患者引起的医院感染有关。已经假设,BCG医院医院传播的可能原因是在无菌药物制备过程中未正确使用使用的设备。从理论上讲,当其他生物危害药物与化学疗法相同的生物安全柜(BSC)制备时,可能会导致免疫功能低下的患者中的化学疗法,交叉污染和医生感染。因此,需要特殊的处理程序。
2021 PAF&DENSSTION.PDF
3。i/我们已提交给该项目的SPGA执行的FCOI披露表。4。i/我们已经阅读并同意遵守当前的知识产权政策(OIT-24-10),在研究中使用人类和动物受试者的机构审查委员会(OIT-25-010)以及其他适当的研究政策。5。所有提出的实验,程序等。涉及人类/动物受试者或在拟议项目中的生物危害措施包含在上述IRB批准的法规协议中或待定的批准中,或者根据大学在研究中使用人类和动物受试者的政策(OIT-25-010),不需要监管方案。*由NSF定义的“调查员”是任何人,无论标题或职位如何,负责研究,进行或报告研究。
宾夕法尼亚大学全球肿瘤学研究中心资助试点...
该项目是否涉及以下任何一项(如果是,则必须在研究启动前获得监管部门的批准函): 人类受试者?¨ 否 ¨ 是 IRB 协议号:______________ 批准日期:______________ 动物受试者?¨ 否 ¨ 是 IACUC 协议号:_____________ 批准日期:_______________ 生物危害或重组 DNA?¨ 否 ¨ 是 协议号:__________________ 批准日期:______________ 项目类别(选择一个): o 基础科学/实验室研究(例如,细胞培养、动物模型) o 转化研究(例如,从基础到临床、从临床到社区) o 临床研究(例如,临床预防或治疗试验) o 基于人群/癌症控制研究(例如,流行病学/遗传学、实施科学、行为科学、卫生服务、基于社区的研究)