XiaoMi-AI文件搜索系统
World File Search System氧化石墨烯大量修饰的屏幕打印电极提供有益的电分析感应能力
摘要:我们展示了一种简便的方法,用于批量生产氧化石墨烯(GO)散装修饰的屏幕打印电极(GO-SPE),这些电极(GO-SPE)是经济的,高度可重现的,并提供了分析有用的输出。通过制造具有不同百分比质量掺入(2.5、5、7.5和10%)的GO-SPE,观察到对所选的电分析探针的电催化作用,与裸露的/石墨SPE相比,随着更大的GO掺杂而增加。最佳质量比为10%,达到90%的碳墨水显示出朝向多巴胺(DA)和尿酸(UA)(ua)的电分析信号。×10的幅度比在裸露/未修改的石墨SPE上可实现的大小要大。此外,10%的GO-SPE表现出竞争性低的检测极限(3σ)对DA的DA。81 nm,它优于Ca的裸露/未修饰的石墨SP。780 nm。改进的分析响应归因于居住在GO纳米片的边缘和缺陷位点的大量氧化物种,可用于对内晶的电化学分析物表现出电催化反应。我们报道的方法简单,可扩展性且具有成本效益,可用于制造GO-SPE,该方法表现出竞争激烈的LOD,并且在商业和药用应用中具有重大兴趣。
,Fisli,H,NACEF,M,AFFOUNE,AM和PONTIUR,M(2024)用低内容PT – Ni微结构装饰的屏幕打印电极用于敏感检测
In this study, we report for the first time, a method for simultaneous detection of paracetamol (PA) and its toxic impurities, 4-aminophenol (4-AP), as well as commonly co-formulated drugs, ascorbic acid and zinc (AA and Zn (II)), using screen-printed electrodes (SPEs) as a sensing platform.为了改善SPE的电化学性能,使用简单的电极位置技术装饰了铂和镍微结构(PT - Ni)。通过Fe - SEM,TEM,EDX,XRD和AFM测量结果证实了合成的PT - Ni/SPE电极的结构和形态。此外,使用环状伏安法和电化学阻抗光谱法研究了AS制备传感器的电化学表征。在最佳条件下,使用环状体积量,差分脉冲伏安法和方波伏安法技术对4 AP,PA,AA和Zn(II)的含量进行定量。设计的传感器可以提出双重效应,利用Pt的Zn(II)检测效率和PT - Ni检测4-AP,AA和PA。一方面,应准备的PT - Ni/SPE传感器表现出对4-AP和PA的线性响应,两者的范围为0.5至200μm,对于4-AP和
相关的光学 - 电化学测量结果揭示了在超密机电极上石墨烯纳米骨骼碰撞的双向电流步骤
摘要:纳米颗粒形成的合成方法产生了异质种群的纳米颗粒,在研究反应性时,可以研究单纳米颗粒的化学植物学特性的技术。虽然单一实体电化学实验已被充分记录在包括球形金属纳米颗粒,乳液液滴和细胞在内的对称对象的,但由于碰撞过程中物体方向的自由度增强,因此不对称物体为额外的挑战提供了额外的挑战。最近,由于高电荷密度能力,机械稳定性和生物相容性的结合,石墨烯已成为一种突出的电极材料,其应用范围从体内感应到工业能量转换反应。石墨烯纳米片(GNP)是一种准二维导电纳米材料,其在微米尺度上具有两个尺寸,而在纳米尺度上有一个,在功能上充当平面材料。在与铁甲醇(外球氧化还原介体)存在下与电极表面碰撞后,观察到广泛的电流响应,这些反应被观察到对称对象的广泛电流响应。在这里,我们介绍了相关的电化学和光学显微镜,以同时在单个实体级别探测化学和空间信息,以完全了解石墨烯纳米片的纳米级的碰撞动力学。此外,这种相关的技术允许对复杂电流响应的反卷积,从而揭示了数十秒范围内耦合的瞬态事件。从这些测量值中,稳态电流的变化用于氧化亚甲醇的氧化可能与GNP碰撞时电极表面积的变化直接相关,从而深入了解了单一实体的几何形状|没有两种组合技术的电极界面,否则将无法访问。
通过气溶胶喷射打印的三维电极
是作者/资助者,他已授予Medrxiv的许可证,以永久显示预印本。(未通过同行评审证明)预先印刷此版本的版权持有人于2020年9月14日发布。 https://doi.org/10.1101/2020.09.13.13.20193722 doi:medrxiv preprint
电化学能源存储中有机电极的机会和挑战快速高保真量子量子量Qubit通过非扰动交叉kerr耦合
Qubit读数是任何量子信息处理器中必不可少的元素。在这项工作中,我们在实验中证明了transmon和Polarmon模式之间的非扰动交叉kerr耦合底,该模式可以改善量子非态度(QND)读数,用于超导速度。新机制使用与分散近似中的标准QND量子读数相同的实验技术,但由于其非扰动性质,它最大化了速度,单发忠诚度和读取的QND属性。此外,它可以最大程度地减少不需要的衰减通道的影响,例如purcell效应。我们观察到短50 ns脉冲的单次读数保真度为97.4%,并且对长度测量脉冲的QND度为99%,并具有重复的单发读数。
从不完整心脏MRI的标准12铅ECG电极位置的个性化拓扑信息定位,可有效心脏数字双胞胎
心脏数字双胞胎(CDTS)of er个性化的内部心脏表示,以推断与心脏机制相关的多尺度特性。CDT的创建需要有关躯干上电极位置的精确信息,特别是对于个性化心电图(ECG)校准。然而,当前的研究通常依赖于对ECG电极定位的躯干成像和手动 /半自动方法的额外获取。在这项研究中,我们提出了一种新颖和E FFI Cient拓扑知识模型,以完全自动从2D临床标准心脏MRIS中提取个性化的ECG标准电极。具体来说,我们从心脏MRI中获得稀疏的躯干轮廓,然后从轮廓中定位12铅ECG的标准电极。心脏MRI旨在成像心脏而不是躯干,从而导致成像中不完整的躯干几何形状。为了解决错过的拓扑结构,我们将电极合并为关键点的子集,可以将其与3D躯干拓扑明确对齐。实验结果表明,所提出的模型优于耗时的常规模型投影方法(Euclidean距离:1。24±0。293厘米与1。48±0。362 cm)和E FFI效率(2 S vs. 30-35分钟)。我们进一步证明了使用检测到的电极进行硅内ECG模拟的e FF具有效果,从而突出了它们创建准确和E ffi cient CDT模型的潜力。该代码可在https://github.com/lileitech/12Lead_ecg_electrode_localizer上获得。©2025 Elsevier B. V.保留所有权利。
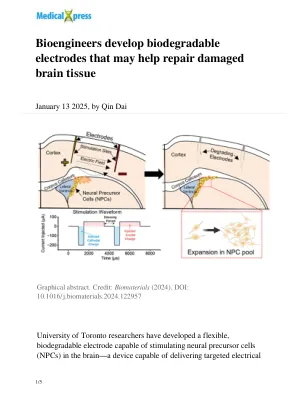
生物工程会开发可生物降解的电极,这些电极可能有助于修复受损的脑组织
通过利用人体的先天修复机制,研究人员的方法代表了治疗神经系统疾病的潜在一步,这是全球残疾的主要原因。虽然神经系统疾病通常会导致不可逆的细胞损失,刺激NPC(能够修复神经组织的可培养细胞)在扩大有限的治疗方案时表现出了希望。
在原位/操作电学技术研究的纳米多孔还原石墨烯电极的电化学激活上
由于电解质很难进入纳米多孔还原石墨烯(RGO)电极的纳米构固定空间,因此实现了这些设备的最佳电化学性能是一个挑战。在这项工作中,在电压控制的纳米孔RGO电极的电化学激活过程中研究了界面州现象的动力学,该电化学激活在人体能力和电化学障碍方面导致电化学性能增强。原位/操作表征技术用于揭示激活过程中引入的不可逆材料变化的动力学,包括纳米孔内的离子差异和水的构成,以及含氧组的还原和RGO Interlayer距离的减少。此外,操作技术用于揭示RGO电极的复杂极化依赖性动态响应的起源。研究表明,石墨烯基平面中剩余官能团的可逆质子化/去质子化和阳离子电吸附/解吸过程控制纳米孔RGO电极的假能性能。这项工作为纳米多孔RGO电极的电化学循环过程中发生的表面化学,离子实现和脱染过程之间的复杂相互作用带来了新的了解,从而为设计基于Nanoporor rgo的高强度电极设计了新的见解。
柔软的弹力电极使用电信号模拟触摸感觉
聚合物电极将激光切割成弹簧形的同心设计,并连接到硅基板上。“此设计可增强电极的可伸缩性,并确保电流靶向皮肤上的特定位置,从而提供局部刺激以防止任何疼痛。” Abdulhameed Abdal博士说。加州大学圣地亚哥分校的机械和航空航天工程系的学生和该研究的另一位联合首先作者。Abdal和Blau与UC San Diego Nano Engineering本科生Yi Qie,Anthony Navarro和Jason Chin合成电极的合成和制造。