XiaoMi-AI文件搜索系统
World File Search System基于 NaNi 0.7 Co 0.3 O 2 、Na 2 MnO 3 和 NaCoO 2 组合的新型钠离子电池正极材料:合成与表征
摘要:通过溶胶-凝胶法制备了几种组合,包括 (1-xy) NaNi 0.7 Co 0.3 O 2 、xNa 2 MnO 3 和 yNaCoO 2 体系。已经应用化学计量的 NaNO 3 、Mn (Ac) 2 ∙4H 2 O、Co (Ac) 2 ⋅ 4H 2 O 和 Ni(NO 3 ) 2 ⋅ 6H 2 O 对 28 个样品进行了测试。我们证明,包括掺杂 Al 的 Na 1.5 Ni 0.117 Co 0.366 Al 0.017 Mn 0.5 O 2 在内的样品是 NIBT 中正极材料的最佳组成,因为该组合中的钴 (Co) 含量低于 NiCoO 2 。从 Co 使用成本和毒性的角度来看,这一点很重要。通过在2.0-4.0V范围内进行循环测试,分析了正极材料的充放电行为。结果表明,此类样品可以高效地消除Co不适合的缺点,也可以替代比Li更便宜的Na。
DNR Capital澳大利亚股票对社会负责的投资组合的表现使S&P/ASX 200总回报指数在一月份下降了0.37%。
在此期间,S&P/ASX 200总回报指数上涨了4.57%。消费者自由支配( +7.1%)是表现最佳的行业,对2月份的降低降低前景的信心越来越有信心,对消费者的积极影响可能会随之而来(Wesfarmers(Wes) +7.1%,贵族休闲(Alistocrat Leisure(All) +10.6%)。财务( +6.1%)也表现出色,同样对宽松的财务状况的影响(澳大利亚联邦银行(CBA) +4.8%,Macquarie Group(MQG) +8.6%)。公用事业(-2.4%)是表现最差的部门,此前降级到弱气产量的原产能指南(ORG)(org -4.1%,AGL Energy(AGL)-2.0%)。消费者主食( +0.7%)的表现也不足,因为在Rick -On Rally中留下了防御性暴露(Woolworths Group(WOW)-0.1%,Coles Group(COL) +3.2%)。
抑制ULK1/2介导的自噬增强抗原加工和表现 ARC-9:一项评估基于伊特鲁马德的治疗组合的随机研究
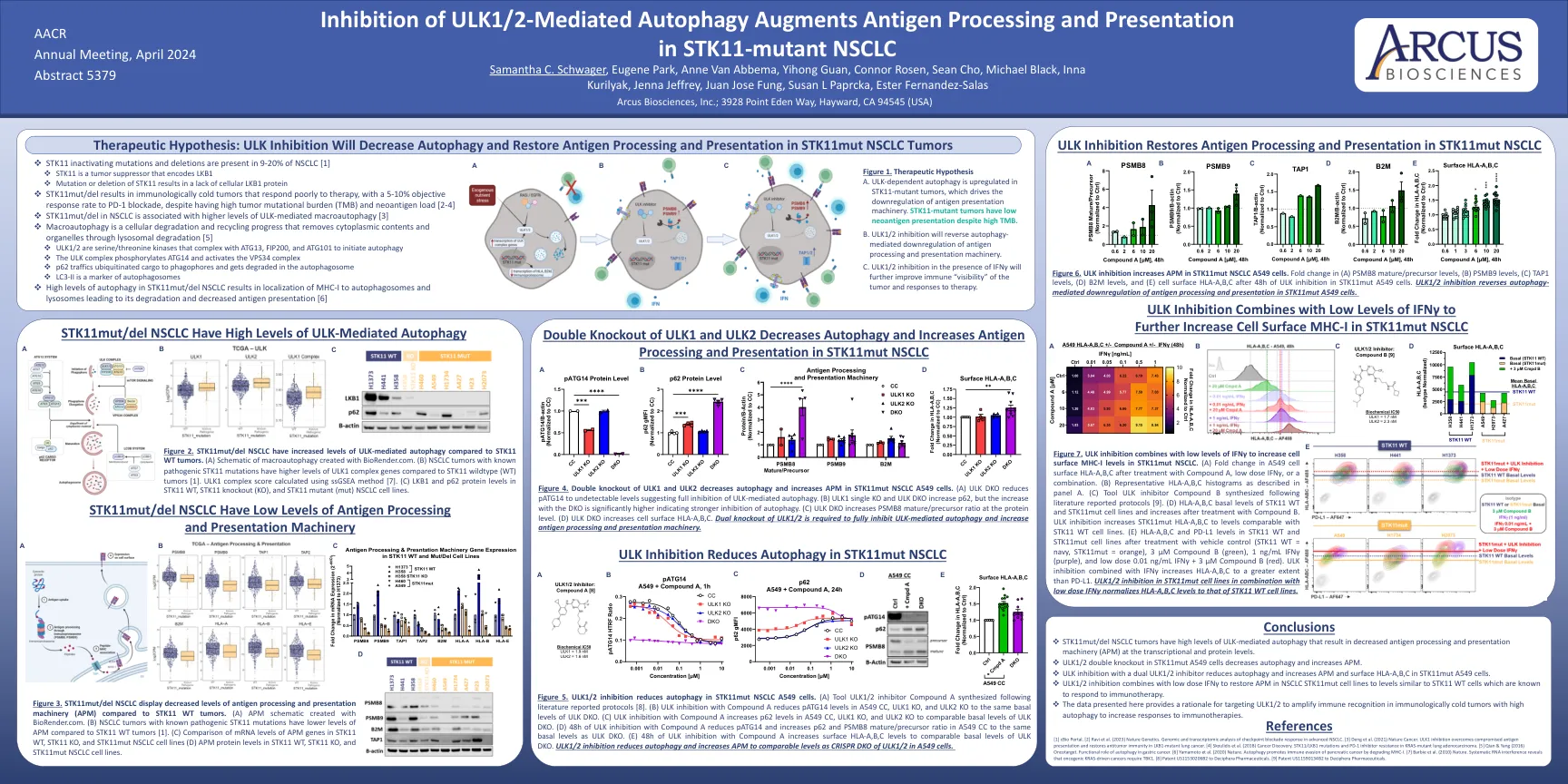
图2。与STK11 WT肿瘤相比, STK11MUT/DEL NSCLC具有ULK介导的自噬水平升高。 (a)用biorender.com创建的大噬细胞的示意图。 与STK11野生型(WT)肿瘤相比,具有已知致病性STK11突变的NSCLC肿瘤具有更高水平的ULK1复合基因[1]。 ULK1复合分数使用SSGSEA方法计算[7]。 (C)STK11 WT,STK11敲除(KO)和STK11突变体(MUT)NSCLC细胞系中的LKB1和P62蛋白水平。 图4。 ULK1和ULK2的双重敲除可降低自噬并增加STK11MUT NSCLC A549细胞中的APM。 (a)ULK DKO将PATG14降低至无法检测的水平,表明对ULK介导的自噬完全抑制。 (b)ULK1单个KO和ULK DKO增加了p62,但随着DKO的增加,dKO的增加表明自噬抑制更强。 (c)ULK DKO在蛋白质水平上增加了PSMB8成熟/前体比率。 (d)ULK DKO增加了细胞表面HLA-A,b,c。 需要ULK1/2的双重敲除以完全抑制ULK介导的自噬并增加抗原加工和表现机制。STK11MUT/DEL NSCLC具有ULK介导的自噬水平升高。(a)用biorender.com创建的大噬细胞的示意图。与STK11野生型(WT)肿瘤相比,具有已知致病性STK11突变的NSCLC肿瘤具有更高水平的ULK1复合基因[1]。ULK1复合分数使用SSGSEA方法计算[7]。 (C)STK11 WT,STK11敲除(KO)和STK11突变体(MUT)NSCLC细胞系中的LKB1和P62蛋白水平。 图4。 ULK1和ULK2的双重敲除可降低自噬并增加STK11MUT NSCLC A549细胞中的APM。 (a)ULK DKO将PATG14降低至无法检测的水平,表明对ULK介导的自噬完全抑制。 (b)ULK1单个KO和ULK DKO增加了p62,但随着DKO的增加,dKO的增加表明自噬抑制更强。 (c)ULK DKO在蛋白质水平上增加了PSMB8成熟/前体比率。 (d)ULK DKO增加了细胞表面HLA-A,b,c。 需要ULK1/2的双重敲除以完全抑制ULK介导的自噬并增加抗原加工和表现机制。ULK1复合分数使用SSGSEA方法计算[7]。(C)STK11 WT,STK11敲除(KO)和STK11突变体(MUT)NSCLC细胞系中的LKB1和P62蛋白水平。图4。ULK1和ULK2的双重敲除可降低自噬并增加STK11MUT NSCLC A549细胞中的APM。(a)ULK DKO将PATG14降低至无法检测的水平,表明对ULK介导的自噬完全抑制。(b)ULK1单个KO和ULK DKO增加了p62,但随着DKO的增加,dKO的增加表明自噬抑制更强。(c)ULK DKO在蛋白质水平上增加了PSMB8成熟/前体比率。(d)ULK DKO增加了细胞表面HLA-A,b,c。需要ULK1/2的双重敲除以完全抑制ULK介导的自噬并增加抗原加工和表现机制。
俄罗斯海事船舶登记处
rs-class.org › Industry › getIndustry Jun 29, 2015 — Jun 29, 2015 N 4.0xPR,用作“poka-gas”组合的一部分。用于“焊丝/气体”组合的铝合金焊丝,商品名 V.CvAMg61 ...
2023气候报告 - 有关TCFD和进度的更新...
在2021年,我们设定了与我们的运营和融资活动相关的净零温室气体(GHG)排放。2我们正在取得进步,以实现我们的油气和天然气和发电组合的2030年临时排放量。截至2022年,与2020年的基线相比,我们的运营油和天然气组合的排放强度累计下降了22%。此进度主要归因于活动组合管理。我们最终使用油气组合的排放强度在2020年至2022年之间没有变化,因为技术,地缘政治和宏观经济环境继续为排放强度的变化率提供了信息。截至2022年,与我们的2020年基线相比,我们发电组合的排放强度累计下降了14%。除了我们继续专注于向客户和基于可再生能源的项目提供贷款外,还可以归因于客户转移到较低发射一代混音的客户。
2035 年情景下的输电组合和运营
国家输电规划研究 (NTP 研究) 评估了输电对美国本土的作用和价值。输电组合的开发和验证是分析的一个关键方面,它可以根据网络和运营约束测试转型方案。本章介绍了开发输电组合的方法、美国本土的最终组合以及第 4 章和第 5 章重点研究中使用的西部互联的替代组合,以及关于这些输电组合如何用于未来 2035 年模型年的小时运营的其他见解。本章还描述了对替代西部互联组合的输电效益和成本的评估。
抑制ULK1/2介导的自噬增强抗原加工和表现ARC-9:一项评估基于伊特鲁马德的治疗组合的随机研究
如果没有禁忌使用贝伐单抗。hr,危险比; ORR,客观响应率; OS,整体生存; PFS,无进展的生存; TEAE,治疗紧急不良事件
量子 BCI 管理基金 (C)
投资政策 为实现目标,投资组合中应包含的投资包括本地和全球股票证券、非股票证券、货币市场工具、计息工具和证券、债券、债权证、公司债务、股票证券、房地产证券、优先股、可转换股票和流动资产。投资组合的最大股票敞口为其资产价值的 75%。风险将通过在可接受的风险承受范围内管理投资组合的波动性和长期回报来管理,重点是实现长期实际回报。经理可以投资于集体投资计划投资组合的参与权益或任何其他形式的参与。投资组合可能不时投资于上市和非上市金融工具。