XiaoMi-AI文件搜索系统
World File Search SystemMüller等。 - Aurora -A通过CDK12 1 阻止TRC JAX动物行为系统(JABS) 混合猪中等位基因特异性调节变化的多摩尼克表征1 质膜修复需要Septin细胞骨架 RNA-Seq基因融合检测工具的荟萃分析 量表,新颖壁ches的高分辨率微生物分析 壳聚糖金纳米颗粒基于敏感的视觉检测组氨酸标记的重组蛋白 强化学习和工作记忆系统的双重过程障碍是生理焦虑中学习缺陷的基础 合成PPR蛋白的翻译激活阐明了拟南芥叶绿体中PSBA翻译的控制 在某些选定的白色念珠菌基因中对镜面重复序列的内部评估 生成人工智能执行基本的结构生物学建模 研究了模拟的两组分凝胶系统的组织再生 动物和机器人建模和模拟框架
预印本(未通过同行评审认证)是作者/资助者。保留所有权利。未经许可就不允许重复使用。该版本的版权持有人于2025年1月19日发布。 https://doi.org/10.1101/2025.01.15.633177 doi:biorxiv preprint
将金纳米颗粒的潜力解锁为游戏 -
根据研究,肝细胞癌(HCC)在死亡原因方面在全球排名第三,并且是总体上第五大常见的癌症类型。 因此,寻找新颖的诊断和治疗方法至关重要。 使用纳米技术作为一种癌症治疗,最近引起了很大的兴趣。 尽管在检测和治疗方面取得了重大进展,但在完全消除这种疾病之前还有很长的路要走。 因此,寻找诊断和治愈疾病的创新方法至关重要。 尤其是,具有与许多生物分子相当的大小相当的金属纳米颗粒(NP)及其纳米级结构的实质惰性引起了极大的兴趣。 由于其特殊的光学质量,通过各种配体的附着,生物相容性(生物启动性和低细胞毒性)以及出色的光学特性,金NP(AUNP)获得了重大兴趣。 当前的评论讨论了各种领域中AuNP的效率,包括成像,免疫疗法和用于治疗肝癌的光热疗法。 最后,本综述总结了AUNPS前景的局限性。根据研究,肝细胞癌(HCC)在死亡原因方面在全球排名第三,并且是总体上第五大常见的癌症类型。因此,寻找新颖的诊断和治疗方法至关重要。使用纳米技术作为一种癌症治疗,最近引起了很大的兴趣。尽管在检测和治疗方面取得了重大进展,但在完全消除这种疾病之前还有很长的路要走。因此,寻找诊断和治愈疾病的创新方法至关重要。尤其是,具有与许多生物分子相当的大小相当的金属纳米颗粒(NP)及其纳米级结构的实质惰性引起了极大的兴趣。由于其特殊的光学质量,通过各种配体的附着,生物相容性(生物启动性和低细胞毒性)以及出色的光学特性,金NP(AUNP)获得了重大兴趣。当前的评论讨论了各种领域中AuNP的效率,包括成像,免疫疗法和用于治疗肝癌的光热疗法。最后,本综述总结了AUNPS前景的局限性。
仙人掌提取物金纳米粒子的生物合成及伊红染料的环境污染处理
在纳米尺度(1 纳米至 100 纳米 (10-9 米))上对结构、电子和系统进行操控被称为纳米技术 [ 1, 2]。金属纳米粒子,尤其是金纳米粒子 (AuNP),因其与入射光的奇妙相互作用而备受关注 [ 3]。在所有金属纳米粒子中,金纳米粒子因具有电、磁、生物传感、等离子体、光子、催化和生物医学特性,在近几十年来引起了最多的关注 [ 4 ]。金纳米粒子对生物医学应用做出了重大贡献,如免疫色谱病原体识别、药物输送、生物标记、光热疗法和癌症光诊断 [ 5 ]。AuNP 在尺寸、形状、溶解度、稳定性和功能方面的可控合成一直是人们研究的课题。合成 AuNPs 的方法通常可分为三类:化学方法、物理方法和生物方法 [6]。化学方法、物理方法和生物方法。合成 AuNPs 的另一种环保方法是通过称为“绿色合成”的生物技术。为了最大限度地减少传统 AuNPs 合成过程中产生的有害化学物质和有毒副产物,生物合成至关重要。目前,不同的 AuNPs 是使用绿色材料生产的,如植物、真菌、藻类、酶和生物聚合物 [7-9]。由于生物合成产生的 AuNPs 高度稳定且特征明确,因此在生物医学应用中使用它们通常更安全,因为这些化合物来自天然材料 [10]。已经采用了几种经济、环保且实用的技术来从微生物 [11]、植物提取物 [12] 中生产纳米颗粒。这些植物提取物在将金转化为纳米颗粒时充当封端剂和还原剂
植物介导的金纳米粒子在癌症治疗中的应用
金纳米粒子 (AuNPs) 因其独特的物理化学性质而在癌症治疗和药物输送方面表现出巨大的前景。利用植物提取物和植物化学物质合成 AuNPs 是一种简单、快速、环保且经济高效的替代方法。本综述深入分析了植物介导的 AuNPs 在癌症治疗中的作用,重点介绍了其核心机制、药物输送应用和未来潜力。它强调了绿色合成方法对癌症治疗的优势,详细介绍了所涉及的过程,并重点介绍了用于纳米粒子生物合成的各种植物。本综述还探讨了植物介导的 AuNPs 的抗癌作用,例如它们选择性靶向癌细胞和诱导细胞凋亡的能力,这得到了体外和体内研究的支持。此外,还研究了这些纳米粒子在癌症治疗的靶向药物输送中的应用。本综述解决了生物相容性和毒性问题,为这些纳米粒子的安全性提供了见解。讨论了未来的研究方向和挑战,以克服当前的局限性并最大限度地提高其临床适用性。总之,植物介导的 AuNP 为癌症治疗和药物输送提供了一种可持续且有效的方法,其绿色合成和多种抗癌特性凸显了其潜力。进一步的研究对于充分发挥其临床益处至关重要。
DNA折纸指导的金纳米球的自组装
等离子纳米结构经常用于创建具有多种光学效应的元整形面积。控制纳米结构的形状和定位是这种等离子跨面功能的关键。在光刻均值旁边,定向自组装是一条可行的途径,可在表面上以必要的精度在表面上创建等离子结构。在这里,提出了DNA折纸自组装和电子束光刻的组合方法,用于确定金纳米球在SIO 2表面上的定位。首先,DNA折纸结构与电子束图案的底物结合,然后通过DNA杂交连接到DNA折纸结构上定义的结合位点上的金纳米颗粒。然后使用溶胶 - 凝胶反应在DNA周围生长二氧化硅层,从而增加了自组装跨表面的稳定性。平均产量为74%的单金纳米球,位于确定位置,空间位置精度为9 nm。金纳米球二聚体和三聚体的速度分别为65%和60%。这种结构方法的适用性是通过制造的元张面积来证明的,其光学响应可以通过传入和散射光的极化来调节。
唾液酸官能化的金纳米颗粒,用于敏感和选择性比色测定5-羟色胺
摘要:我们提出了一种受自然复杂机制启发的新型比色方法,能够选择性地确定具有高灵敏度的5-羟色胺。此方法利用了链接到金纳米颗粒(SA-Aunps)的唾液酸(SA)分子的固有结合亲和力。在5-羟色胺结合,sa-aunps骨料和Sa-unps吸光度的特征性红移后,也会发生剧烈的色彩变化(红色至蓝色),即使没有仪器也很容易观察到。提出的方法有效地消除了潜在干扰物种(例如多巴胺,肾上腺素,L-酪氨酸,葡萄糖胺,半乳糖,甘露糖和草酸)的干预措施。缺乏与5-羟色胺相关的与结构相关的前体L- tryptophan的变化,进一步证实了这种方法检测方法的高选择性。比色法具有宽的线性动态范围(0.05 - 1.0μm),检测的低极限(0.02μm)和快速响应时间(5分钟)。该方法的检测极限低于到目前为止报道的其他比色性羟色胺传感器。通过在处理后血浆中采用5-羟色胺回收测定法评估了所提出的方法在生物样品分析中的使用。回收率为90.5%至104.2%,显示出有希望的临床应用潜力。
CSM 罗纳德·E·金纳德
CSM Ronald E. Kinard 是南卡罗来纳州查尔斯顿人。他于 2001 年加入美国陆军,并在肯塔基州诺克斯堡参加单站单位训练,在那里他获得了骑兵侦察兵(19D)军事职业特长。CSM Kinard 担任过从团队领导到指挥军士长的每个领导职务,还担任过联合战备训练中心的观察员控制员和普罗维登斯学院预备役军官训练司令部的高级军事科学教官。他曾任职于路易斯安那州波尔克堡第 2/2 装甲骑兵团;路易斯安那州波尔克堡第 89 骑兵团第 3 中队;路易斯安那州波尔克堡 TF3 联合战备训练中心;北卡罗来纳州布拉格堡第 73 骑兵团第 3 中队;罗德岛普罗维登斯普罗维登斯学院;他曾在德国格拉芬沃尔第 91 骑兵团第 1 中队、德克萨斯州布利斯堡军士长学院、阿拉斯加州埃尔门多夫理查森联合基地和夏威夷州斯科菲尔德兵营第 4 骑兵团第 3 中队服役。他曾被派往伊拉克和阿富汗参加多次作战行动。CSM Kinard 的军事教育包括美国陆军军士长学院的所有 NCOES、游骑兵课程、空降课程、探路者课程、跳伞长课程、侦察排长课程、骑兵领导课程、JRTC 观察员控制员课程、夏普基础课程、SOCC 教官培训课程、发展教官课程、指挥官/一级军士长课程、营和旅级预指挥课程以及指挥军士长发展课程。他的平民教育包括西阿什利高中的高中文凭、普罗维登斯学院的领导力研究与发展文学学士学位以及德克萨斯大学埃尔帕索分校的公共管理硕士学位。 CSM Kinard 获得的奖项和勋章包括铜星勋章(二级)、功绩服务勋章(四级)、陆军表彰勋章(五级)、陆军成就奖(四级)、总统单位嘉奖(二级)、英勇单位嘉奖、功绩单位嘉奖、陆军优良品行勋章(七级)、国防服役勋带、阿富汗战役勋章(带星星)、伊拉克战役勋章(三星)、全球反恐战争服役勋章、全球反恐战争远征勋章、士官专业发展勋章(五级)、陆军服役勋章、海外服役勋章(三级)、北约勋章、游骑兵勋章、探路者徽章、跳伞大师徽章以及荷兰、德国和拉脱维亚外国跳伞翼。 CSM Kinard 还获得了圣乔治铜质勋章。CSM Kinard 与来自南卡罗来纳州查尔斯顿的 Amy Kinard 结婚 18 年。他们有一个女儿 Marissa 和一个儿子 Brady。
211At 在金纳米粒子上的靶向放射性核素治疗应用
外束放射治疗 (EBRT) 使用外部来源的准直 X 射线或伽马射线、电子或质子发射到受影响区域。2 最近的迭代被称为重离子疗法,使用重离子代替电子或质子进行治疗。3,4 这种方法的优点是不需要手术,这可能会使患者的健康复杂化。此外,随着机器的进步,可以非常准确地识别目标细胞,从而可以更准确地输送剂量。另一方面,近距离放射治疗使用放射性物质并将其植入目标细胞附近的密封容器中。该程序适用于特定癌症,例如乳腺癌或前列腺癌,在这些癌症中,将更高剂量应用于集中区域是有利的。这两种治疗方法可以结合起来:通过使用 EBRT 瞄准大癌症肿块,近距离放射治疗将剂量输送到较小的癌症区域,可以提高整体治疗的有效性。内部治疗的另一种形式是放射性核素治疗或非密封源放射治疗。它使用化学和生物化合物与癌细胞结合或利用人体将其吸收到体内的倾向,因此是一种靶向放射治疗。早期的例子是使用放射性碘(131 I)治疗甲状腺癌。5 由于甲状腺会自然吸收碘进行自我调节,因此当摄入 131 I 时,甲状腺会吸收放射性碘,治疗就会顺利进行。
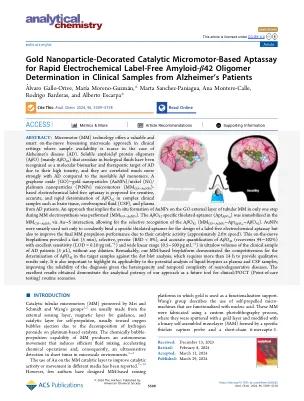
金纳米颗粒装饰的基于催化微动物的催化剂,用于快速电化学无标记的无淀粉样蛋白β42临床
摘要:微型运动(MM)技术在临床环境中提供了一种有价值且智能的自动生物传感微观方法,在阿尔茨海默氏病(AD)的情况下,样本可用性稀缺。可溶性淀粉样蛋白β蛋白低聚物(AβO)(AβO)(主要是AβO42),在生物流体中循环的循环已被认为是AD的分子生物标志物和AD的分子生物标志物和治疗靶标,因为它们的高毒性,并且与AD相比,它们与AD的相关性更强。基于电化学标记的氧化纳米颗粒(AUNP)/镍(Ni)/铂(Ni)/铂纳米颗粒(PTNPS)微型颗粒(MM GO - go-aunps) - 基于电化学标记的无电化学aptassay被提出,以进行敏感,准确的,临床的临床范围,例如,βO 42的临床范围较快,以下(CSF)和AD患者的血浆。 一种表示在MM电气合成期间仅在一个步骤中仅在一个步骤中的a unp的原位形成的方法(mm go -aunps)。 AβO42特异性硫醇化调子剂(APTAβOD 42)通过Au-s的相互作用固定在MM GO-AUNP中,从而可以选择性地识别AβO42(mm aunps-aunps-aunps-aunps-aunps-apt-apt app-app-apt aβoβoβob d 42-aβo d 42-aβoβo 42)。 aunps不仅被智能地用于共价结合特定的硫醇化运动剂,以设计无标签的电化学插图,而且还可以改善由于其催化活性(大约2.0×速度)而提高最终的MM推进性能。 值得注意的是,我们基于MM的Bioplatform证明了针对DOT印迹分析在目标样品中确定AβO42的竞争力,该分析需要超过14小时才能提供定性结果。基于电化学标记的氧化纳米颗粒(AUNP)/镍(Ni)/铂(Ni)/铂纳米颗粒(PTNPS)微型颗粒(MM GO - go-aunps) - 基于电化学标记的无电化学aptassay被提出,以进行敏感,准确的,临床的临床范围,例如,βO 42的临床范围较快,以下(CSF)和AD患者的血浆。一种表示在MM电气合成期间仅在一个步骤中仅在一个步骤中的a unp的原位形成的方法(mm go -aunps)。AβO42特异性硫醇化调子剂(APTAβOD 42)通过Au-s的相互作用固定在MM GO-AUNP中,从而可以选择性地识别AβO42(mm aunps-aunps-aunps-aunps-aunps-apt-apt app-app-apt aβoβoβob d 42-aβo d 42-aβoβo 42)。aunps不仅被智能地用于共价结合特定的硫醇化运动剂,以设计无标签的电化学插图,而且还可以改善由于其催化活性(大约2.0×速度)而提高最终的MM推进性能。值得注意的是,我们基于MM的Bioplatform证明了针对DOT印迹分析在目标样品中确定AβO42的竞争力,该分析需要超过14小时才能提供定性结果。这种移动的生物术提供了快速(5分钟),选择性,精确(RSD <8%),并准确地定量βO42(回收率94 - 102%)具有出色的敏感性(LOD = 0.10 Pg ml - 1)和宽线性(0.5-500 pg ml-ml-inflof flastial flastial flastial flastial flastice) l),没有任何稀释。也重要的是要强调其对液体活检的潜在分析(作为等离子体和CSF样品的潜在分析),从而提高了诊断的可靠性,因为神经退行性疾病的异质性和时间复杂性。获得的出色结果证明了我们的方法作为临床/POCT(护理点测试)常规场景的未来工具的分析效力。■简介
在金纳米颗粒上的电容性免疫传感,用一步激光纳米结构制造的还原石墨烯氧化石墨烯电极
纳米结构的电化学生物传感器已经迎来了诊断精度的新时代,从而增强了临床生物标志物检测的敏感性和特异性。中,电容性生物传感可实现多个分子靶标的超灵敏标签检测。但是,与纳米结构平台的常规制造方法相关的复杂性和成本阻碍了这些设备的广泛采用。这项研究引入了一个电容式生物传感器,该生物传感器利用激光磨碎的还原氧化石墨烯(RGO)ELEC TRODE,该Elec Trodes装饰有金纳米颗粒(Aunps)。制造涉及激光标记的GO-AU 3 +膜,产生RGO-AUNP电极,通过按压戳面方法无缝传输到PET基板上。这些电极与特定生物受体功能化后,对生物分子识别具有显着的亲和力。例如,使用人IgG抗体的初步研究证实了使用电化学电容光谱学的生物传感器的检测能力。此外,生物传感器可以量化临床癌症生物标志物Ca-19-9糖蛋白。生物传感器的动态范围在0到300 u ml -1,检测极限为8.9 u ml -1。对人体液体预处理的CA-19-9抗原的已知浓度进行严格测试证实了它们在检测糖蛋白方面的准确性和可靠性。这项研究表示临床生物标志物的电容式生物传感方面的显着进展,可能导致更容易获得和成本效益的护理解决方案。