XiaoMi-AI文件搜索系统
World File Search System闪烁的抗抗性气传感器测量器...
摘要:我们讨论了基于化学主义传感器的低频噪声测量的气体传感系统的实施挑战。在各种气体传感材料中的电阻波动通常在频率范围内,通常至几个kHz,可以通过考虑其强度和功率频谱密度的斜率来增强气体感测。考虑了电阻气体传感器中低频噪声测量的问题,特别是在具有二维材料中表现出气体感应性能的问题。我们提出了用于气体检测的测量设置和噪声处理方法。化学传感器显示了需要不同闪烁噪声测量方法的各种直流电阻。单独的噪声测量设置用于高达几百kΩ的电阻,并用于具有更高值的电阻。高度电阻材料(例如MOS 2,WS 2和ZRS 3)中的噪声测量值易于外部干扰,但可以使用温度或光照射来调节以增强感应。因此,这种材料引起了气体传感的极大兴趣。
使用眼睛闪烁的虚拟键盘
Kaushal Gawas,三位一体工程与研究摘要学生 - 口头交流认为是大多数人的主要互动方式,但是某些情况可能会抑制其使用。这提示了探索替代通信方法。本文为问题引入了一种新颖的解决方案:使用眼眨眼检测输入的虚拟键盘系统。利用网络摄像头,系统通过面部特征点标识眼睛闪烁,特别是“ 68分”方法。通过采用机器学习算法和图像处理技术的混合物,例如定向梯度(HOG)的直方图和卷积神经网络(CNN),该系统可实现实时和准确的眼睛闪烁检测。虚拟键盘的用户界面是直觉设计的,使用户能够无缝输入文本而无需物理键盘或其他设备。此外,眼睛闪烁是“ Enter”键的功能等效物。使用多种数据集对系统的评估表明了其在不同的照明条件和用户配置文件中的稳健性。所提出的系统对辅助技术,虚拟现实和人类计算机互动的应用有望。关键术语:虚拟键盘,眼睛眨眼检测,OpenCV,Python,Dlib库,人机交互(HCI)。I.我的研究论文介绍了一个虚拟键盘系统的创建,该系统引入了一种新颖的输入方法:眼眨眼检测。主要目的是开发一个不仅有效而且直观且易于使用的系统。这种系统的潜在应用是广泛的,跨越了各个领域,包括辅助技术,虚拟现实和人类计算机的互动。该虚拟键盘系统的一个值得注意的方面是它对传统输入设备(例如物理键盘之类的环境)的适应性。例如,在诸如核电站的高风险环境中,污染潜力很大,利用传统的输入设备可能会对操作员构成挑战甚至风险。在这种情况下,使用眼眨眼检测的虚拟键盘系统的实现可能会非常有益。通过消除与输入设备进行物理接触的需求,可以大大降低污染的风险。此外,系统对眼睛眨眼检测的依赖确保了操作员可以与界面进行交互,而不会损害其安全性或环境的完整性。因此,通过提供传统输入方法的更安全,更实用的替代方案,提出的虚拟键盘系统有可能极大地提高核电站等关键环境中的运营效率和安全性。动机传统输入设备(如键盘和小鼠)长期以来一直是计算机交互的基石。但是,这些工具对运动障碍或伤害的个体面临着重大挑战,从而限制了他们对技术的可及性。Eye Blink检测是一种有前途的解决方案,利用了用户眼睛的自然运动,以提供非侵入性和直观的输入机制。此外,在诸如虚拟现实危险工作场所之类的环境中,使用传统输入设备是不切实际的或有风险的,替代方法。本研究论文是出于需要探索眼睛眨眼检测的潜力作为虚拟键盘的可行输入方法的可能性。目的是开发一个能够准确检测眼睛并翻译它们
存在散斑和弱闪烁的闭环自适应光学
散斑是一种干涉现象,由相干照明从物体平面的光学粗糙表面散射而产生。传播到光瞳平面后,背向散射的光线自干涉形成亮斑和暗斑,这些斑块被称为“散斑”。假设照明为准单色,且表面高度变化超过光波长的一半,则散斑图案将“完全显现”,对比度趋于一致。在非合作定向能应用中,散斑充当乘性噪声,对图像质量[2]和轨迹质量[3]产生有害影响。给定一个扩展信标,自适应光学系统必须分别感测和校正大气引起的相位像差(导致闪烁)和物体引起的相位像差(导致散斑)。然而,波前传感器(在自适应光学系统内)实际测量和重建的是来自两个相位像差源的路径积分贡献的总和。例如,夏克-哈特曼波前传感器 (SHWFS) 使用单独的小透镜将接收器孔径划分为子孔径,这些子孔径对入射波前进行采样,并将样本聚焦到探测器阵列上。
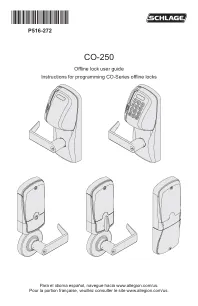
Schlage CO-250用户指南 - 英语
条件灯访问被拒绝2红闪烁访问被拒绝,外部时间区域4眨眼闪烁的工厂默认重置一秒钟的固体绿色带有一秒钟的蜂鸣型低电池指示灯,AA电池9左红色闪烁的电池电池灯光指示灯9右红色指示器9右红色闪烁的红色闪烁瞬间无固定的固定闪光1绿色闪烁,然后固定固定的绿色闪烁,旋转2固定闪光2固定闪烁的闪光2固定闪烁的闪光,闪烁的2个固定的闪光,闪烁的2个闪光(左绿色固体USB活动,没有物理连接左绿色闪烁
在60 Hz处闪烁的白光刺激会引起健康受试者的强烈,广泛的神经夹带和同步
神经调节是旨在调节弥漫性神经元活性以实现治疗作用的技术的集合。通过在大脑中应用外部能量(例如电流,磁场,光或超声)来获得调制时,它被称为神经刺激1。非侵入性脑刺激(NIBSS)技术,例如电击疗法(ECT),经颅磁刺激(TMS)和经颅电刺激(TES),对大脑发挥可测量的结构和功能作用。这些影响包括增加神经可塑性2,大脑结构3和连通性4的变化以及脑衍生的神经营养因子(BDNF)水平5的恢复。某些NIBSS溶液是FDA批准的,用于治疗各种脑部疾病,包括抑郁症6和强迫症7(OCD),强调了神经调节的治疗潜力。
ITU-R P.618-8 建议书 - 设计地球空间电信系统所需的传播数据和预测方法
m) 电离层闪烁:电离层中电子密度的不均匀性导致无线电波的折射聚焦或散焦,并导致称为闪烁的幅度波动。电离层闪烁在地磁赤道附近最大,在中纬度地区最小。极光区也是闪烁较大的区域。强闪烁的幅度呈瑞利分布;较弱的闪烁几乎呈对数正态分布。这些波动随着频率的增加而减小,并且取决于路径几何形状、位置、季节、太阳活动和当地时间。表 2 根据 ITU-R P.531 建议书中的数据,列出了中纬度地区 VHF 和 UHF 的衰落深度数据。
基于稳定闪烁动作视频的开发......
摘要。背景:本研究重点是开发上肢康复计划。为此,设计了一个基于稳态视觉诱发电位 (SSVEP) 触发的脑机接口 (BCI)-功能性电刺激 (FES) 的动作观察游戏,该游戏以闪烁的动作视频为特色。目的:特别是,通过将动作观察范式与基于 BCI 的 FES 相结合来研究游戏的协同效应。方法:在两种条件下对比 BCI-FES 系统:闪烁的动作视频和闪烁的噪声视频。为此,招募了 11 名年龄在 22-27 岁之间的右利手受试者。检查了对这两种情况的大脑激活差异。结果:结果表明,T3 和 P3 通道在动作视频中表现出 8-13 Hz 的 Mu 抑制比噪声视频更大。此外,与噪声视频相比,T4、C4 和 P4 通道对动作的增强高 beta(21-30 Hz)。最后,T4 表明与噪声视频相比,动作视频的低 beta(14-20 Hz)受到抑制。结论:基于闪烁动作视频的 BCI-FES 系统比基于闪烁噪声的系统对皮质激活产生了更大的协同效应。