XiaoMi-AI文件搜索系统
World File Search System远程监控手册
RNS® 神经刺激器型号 RNS-320:您必须咨询医生以确定您是否可以进行 MRI 扫描。RNS® 系统(带 RNS 神经刺激器型号 RNS-320)是 MR 条件性的,这意味着可以在特定条件下安全地进行 MRI 扫描。如果您的神经刺激器已被移除,也可能进行 MRI 扫描。如果您的医生确定您可以进行 MRI 扫描,他或她必须确保遵守安全 MRI 扫描的条件。这些条件包括将您的神经刺激器置于 MRI 模式,这会消耗更多电量并可能影响电池寿命。在 MRI 模式下,神经刺激器不会检测或向患者提供治疗。因此,您应该与医生合作,尽量减少神经刺激器处于 MRI 模式的时间。
刺激丘脑核的刺激显示出改变的GL
摘要:丘脑下核(STN)的深脑刺激(DB)是减轻帕金森氏病(PD)运动症状的手术程序。DBS的模式(例如,所使用的电极对和刺激强度)通常通过基于运动功能的主观评估来优化试验和误差。我们测试了DBS在选定的基底神经节核中释放谷氨酸的假设,并创建了6-羟基羟基胺(6-OHDA)诱导的nigrostriatal病变会在这些基础神经节核中的DBS释放中改变谷氨酸。我们研究了在麻醉,对照和6-OHDA治疗的大鼠中,STN本身或Globus Pallidus(GP)中DBS的伪随机二进制序列与谷氨酸(GP)之间的关系。我们使用使用系统识别估算的转移函数表征了DBS和谷氨酸水平之间的刺激 - 反应关系。刺激GP和STN中STN升高的谷氨酸水平。 尽管6-OHDA处理不会影响DBS在STN期间STN中的谷氨酸动力学,但由于存在或不存在6-OHHDA诱导的病变,DBS在STN中的DBS和GP中DBS之间的DBS之间的转移功能显着改变。 因此,在6-OHDA处理的动物中GP中的谷氨酸反应(但不在STN中)取决于多巴胺能输入。 因此,在DBS患者中,测量GP中的谷氨酸水平可能会在闭环DBS设备中提供有用的反馈目标,因为DBS期间GP中谷氨酸释放的动力学似乎反映了SNC中多巴胺能神经元的丧失。刺激GP和STN中STN升高的谷氨酸水平。尽管6-OHDA处理不会影响DBS在STN期间STN中的谷氨酸动力学,但由于存在或不存在6-OHHDA诱导的病变,DBS在STN中的DBS和GP中DBS之间的DBS之间的转移功能显着改变。因此,在6-OHDA处理的动物中GP中的谷氨酸反应(但不在STN中)取决于多巴胺能输入。因此,在DBS患者中,测量GP中的谷氨酸水平可能会在闭环DBS设备中提供有用的反馈目标,因为DBS期间GP中谷氨酸释放的动力学似乎反映了SNC中多巴胺能神经元的丧失。
用于双向脑机接口 (BD-BCI) 的完全植入式电荷平衡人工感官刺激器原型
Biopac 摘要 — 用于恢复运动和感觉的双向脑机接口 (BD-BCI) 必须实现同时记录和解码来自大脑的运动命令以及通过体感反馈刺激大脑。之前,我们开发并验证了一种用于运动解码的完全植入式 BCI 系统的台式原型。在这里,原型人工感觉刺激器被集成到台式系统中,以开发完全植入式 BD-BCI 的原型。人工感觉刺激器采用基于脉冲宽度调制的主动电荷平衡机制,以确保对长期接口电极的安全刺激,防止损伤脑组织和电极。在幻影脑组织中测试了 BD-BCI 系统的主动电荷平衡的可行性。通过电荷平衡,可以明显去除电极上的残留电荷。这是迈向完全植入式 BD-BCI 系统的关键里程碑。
脊髓的植入电刺激器
国家政策/指南印第安纳州没有肯塔基州为脊髓(仅适用于肯塔基州)植入电气刺激器(仅适用于肯塔基州)路易斯安那州植入脊髓的电刺激器(仅适用于路易斯安那州的新泽西州),新泽西州植入了脊髓的脊髓(仅适用于新墨西哥的新墨西哥植入式电气刺激器(仅适用于新墨西哥)的脊髓(仅)用于脊髓的电刺激器(仅适用于北卡罗来纳州),将电刺激器植入脊髓(仅对于俄亥俄州)(仅适用于俄亥俄州)宾夕法尼亚州植入脊髓的电刺激器,用于脊髓(仅宾夕法尼亚州,仅用于宾夕法尼亚州(仅适用于田纳西州)田纳西州的田纳西州植入电气刺激器,用于刺激器的刺激器(仅用于固定的),刺激范围是刺激范围的散文范围(用于覆盖范围)。根据美国食品和药物管理局(FDA)进行标记为适应症,禁忌症,警告和预防措施的某些情况下的以下条件:
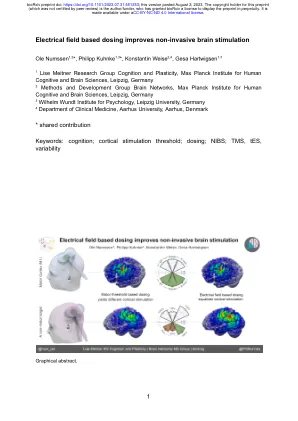
基于电场的给药可改善非侵入性脑刺激
图1。e-field剂量在主题一级优于其他给药策略。(a)选择所有线圈位置以最大化皮质靶刺激。(b)基于电动机阈值(MT)(上排)的剂量在不同的皮质靶区域(柱)施加相同的刺激器强度,从而产生高度可变的皮质刺激强度(以每米的电压为单位; V/m)。“ Stokes”方法(中行)线性地调节了线圈到目标距离的刺激器强度,但仍会导致跨靶标的皮质刺激的次优匹配。e-field的给药(底行)为所有靶标提供相同的皮质刺激强度。颜色:| e |。百分比:MT刺激器强度的百分比。所有电子场均在灰质表面可视化,以示例性主题。(c)刺激器强度(上排)与皮质刺激暴露(底行)之间的关系在皮质靶标之间有很大不同。在皮质靶标上提取刺激暴露,并与MT强度下的M1暴露有关(“ 100%”)。
使用人工智能(AI)编程的医疗设备
1. Hagiwara, H.、Yamashita, Y.、Yagi, S. 等人。经鼻内镜在多中心个体胃癌筛查中的现状及准确性。 J Cancer Screening 2009;47:683-92。2. Menon S、Trudgill N。内镜检查漏诊上消化道癌的可能性有多大?一项荟萃分析。Endosc Int Open 2014;2:E46-50。3. Kumar S、Thosani N、Ladabaum U 等人。3 分钟与 6 分钟结肠镜检查停药时间相关的腺瘤漏诊率:一项前瞻性随机试验。Gastrointest Endosc 2017;85:1273-80。4. Robertson DJ、Lieberman DA、Winawer SJ 等人。结肠镜检查后不久发现的结直肠癌:一项汇总多队列分析。Gut 2014;63:949-56。5. Ladabaum U、Fioritto A、Mitani A 等人。社区实践中窄带图像老化的结肠息肉实时光学活检尚未达到临床决策的关键阈值。胃肠病学 2013;144:81-91。6. 下一代医疗器械评估指标公布(药品上市通知第 0523-2 号,2019 年 5 月 23 日)。 7.《关于修订《药品、医疗器械等质量、功效和安全保障法》的法案》(2019年第63号法案)。 8. 有关程序对医疗器械的适用性的基本原则(2014年11月14日役所官发第1114-5号) 9. Takemura Y, Yoshida S, Tanaka S 等. 定量分析及开发计算机辅助系统以识别结直肠病变的规则小凹模式. Gastrointest Endosc 2010;72:1047-51. 10. Kominami Y, Yoshida S, Tanaka S 等. 利用实时图像识别系统和窄带成像放大结肠镜对结直肠息肉组织学进行计算机辅助诊断. Gastrointest Endosc 2015;83:643-9. 11. Byrne MF, Chapados N, Soudan F 等. 利用深部增强扫描对标准结肠镜检查未改变的视频进行分析以实时区分腺瘤性和增生性小结直肠息肉
国防部标准 NDS Y 7101C 轻武器弹药测试枪械
说明··········································································································································································································· 59
Viper 内存加载器/验证器 (MLV) 和 Viper MLV II
Viper MLV / MLV II 在严苛的航线环境中拥有 20 年的可靠性和耐用性。BAE Systems 不断开发和集成新功能,以支持 F-16 的所有 Block/版本,包括新型 F-16V 和 Block 70 F-16。Viper MLV / MLV II 支持 100 多个 F-16 航空电子系统,为整个 FMS 和美国空军 F-16 用户社区提供功能更新,而开发成本仅为独立系统的一小部分。我们通过识别复杂需求和开发独特的软件和硬件解决方案来满足客户需求。新型 Viper MLV II 提供网络强化硬件架构,确保长期的 F-16 航空电子设备支持。
ECL 15B驱动的堆叠器ECL 15B驱动的堆叠器
电池深部排放保护设备,电压放电指示器,具有低压自动切割和效力功能,可用于更高的电池寿命。证明的紧急开关和电压放电指示器,使其更耐用和可靠。指示器通过CAN-BUS显示故障,无需删除指示外壳。
我的物资追踪器 - GCSS-Army
1.输入材料编号:无通配符 (*) 2.输入 LIN:全部大写,无通配符 (*) 3.输入材料描述:全部大写,建议在输入的文本前后使用通配符 (*)。例如,*TANK* 4.输入 ACOM:全部大写,可选的辅助排序标准 5.输入工厂:(2000 或 2001) 6.输入城市:全部大写,可选的辅助排序标准 7.输入州:两个字符的缩写。全部大写,可选的次要排序标准 8。输入供应类别:单个数字,可选的次要排序标准 9。如果不确定输入 4、5、6、7 的可选搜索标准的正确方法,请在此处输入并单击 ,此搜索功能将创建正确格式的匹配列表 10。单击按钮呈现报告