XiaoMi-AI文件搜索系统
World File Search System剂量和管理指南 | PHESGO®(帕妥珠单抗/曲妥珠单抗/透明质酸酶-zzfx)
黑框警告:心肌病、胚胎-胎儿毒性和肺毒性 • PHESGO 给药可导致亚临床和临床心力衰竭。在接受含蒽环类化疗方案的 PHESGO 患者中,发病率和严重程度最高。在使用 PHESGO 治疗之前和治疗期间应评估心脏功能。对于接受辅助治疗的患者,应停止使用 PHESGO 治疗;对于转移性疾病患者,如果左心室功能出现临床显著下降,应停止使用 PHESGO • 接触 PHESGO 可导致胚胎-胎儿死亡和出生缺陷,包括羊水过少和羊水过少序列,表现为肺发育不全、骨骼异常和新生儿死亡。告知患者这些风险和有效避孕的必要性 • PHESGO 给药可导致严重和致命的肺毒性。出现过敏反应、血管性水肿、间质性肺炎或急性呼吸窘迫综合征时,应停止使用 PHESGO。监测患者直至症状完全消退
苯妥英里 - Negeri Semarang大学
抽象苯妥英是一种源自一种称为Hydantoin的有机化合物的抗癫痫药。苯妥英钠是一种抗癫痫药,主要用于治疗癫痫患者的癫痫发作。苯可以通过靶向和阻断神经系统中电压门控钠通道的作用,这有助于减少导致癫痫发作的大脑中异常的电活动。苯妥英钠也可用于治疗三叉神经痛和心室心动过速。苯妥英的吸收取决于给药途径。苯妥英钠的分布受到血浆蛋白结合的影响。苯妥英钠主要由肝酶,尤其是细胞色素P450酶系统代谢。苯妥英钠排泄受尿液中pH的影响。Side effects of phenytoin use that can occur are sedation, fever, sedation, confusion, hallucinations, peripheral neuropathy, Stevens-Johnson syndrome, cardiovascular collapse, hypotension, purple glove syndrome, nystagmus, ataxia, nausea, coma, seizures, vomiting, hyperactivity, lethargy, fetal hydantoin syndrome (FHS)和巨大贫血。苯妥英钠是在苯妥英钠或其他羟托因,孕妇和哺乳期妇女过敏的患者中禁忌的。口服苯妥英,过量会引起神经毒性,而肠胃外苯甲酸苯甲酸过量会导致心血管毒性。 没有特定的解毒剂对苯妥毒素毒性,治疗通常是支持的。 有多种药物可以与苯妥英相互作用以降低或增加苯妥英水平。 关键字:苯妥英钠,临床用途,药代动力学,药效学,毒理学口服苯妥英,过量会引起神经毒性,而肠胃外苯甲酸苯甲酸过量会导致心血管毒性。没有特定的解毒剂对苯妥毒素毒性,治疗通常是支持的。有多种药物可以与苯妥英相互作用以降低或增加苯妥英水平。关键字:苯妥英钠,临床用途,药代动力学,药效学,毒理学
Enhertu, INN-曲妥珠单抗
此药品需要接受额外监控。这将允许快速识别新的安全信息。请医疗保健专业人员报告任何疑似不良反应。有关如何报告不良反应,请参阅第 4.8 节。 1. 药品名称 Enhertu 100 mg 浓缩粉末,用于输液溶液 2. 定性和定量组成 一瓶浓缩粉末,用于输液溶液,含有 100 mg trastuzumab deruxtecan。配制后,一瓶 5 mL 溶液含有 20 mg/mL trastuzumab deruxtecan(请参阅第 6.6 节)。曲妥珠单抗 deruxtecan 是一种抗体-药物偶联物 (ADC),含有人源化抗 HER2 IgG1 单克隆抗体 (mAb),其氨基酸序列与曲妥珠单抗相同,由哺乳动物 (中国仓鼠卵巢) 细胞产生,通过基于四肽的可裂解接头与 DXd (一种依沙替康衍生物和一种拓扑异构酶 I 抑制剂) 共价连接。每个抗体分子上附着约 8 个 deruxtecan 分子。有关辅料的完整列表,请参阅第 6.1 节。3. 药物形式用于输液溶液的浓缩粉末。白色至黄白色冻干粉末。 4. 临床特点 4.1 治疗适应症 乳腺癌 HER2 阳性乳腺癌 Enhertu 单药疗法适用于治疗已接受过一种或多种抗 HER2 方案的不可切除或转移性 HER2 阳性乳腺癌成年患者。 HER2 低乳腺癌 Enhertu 单药疗法适用于治疗已接受过转移性化疗或在完成辅助化疗期间或后 6 个月内出现疾病复发的不可切除或转移性 HER2 低乳腺癌成年患者(见第 4.2 节)。 非小细胞肺癌 (NSCLC) Enhertu 单药疗法适用于治疗肿瘤具有激活 HER2 (ERBB2) 突变且需要在铂类化疗(联合或不联合免疫疗法)后进行全身治疗的晚期 NSCLC 成年患者。
1665-布伦妥昔单抗
剂量调整的证据有限,eviQ 上的建议仅供参考。他们通常是保守的,强调安全。任何剂量调整都应基于临床判断和个体患者的情况,包括但不限于治疗意图(治愈性与姑息性)、抗癌方案(单一疗法与联合疗法与化疗与免疫疗法)、癌症生物学(部位、大小、突变、转移)、其他治疗相关副作用、其他合并症、体能状态和患者偏好。建议的剂量调整基于临床试验结果、产品信息、已发布的指南和参考委员会共识。除非另有说明,否则剂量减少适用于每个单独的剂量,而不适用于总天数或治疗周期持续时间。除非另有说明,否则非血液学分级基于不良事件通用术语标准 (CTCAE)。肾脏和肝脏的剂量调整已尽可能标准化。有关更多信息,请参阅剂量注意事项和免责声明。
米哚妥林治疗 AML
急性髓细胞白血病 (AML) 是一种快速生长的血癌,与白细胞有关。AML 的治疗可分为三个阶段:诱导治疗(控制 AML)、巩固治疗(控制 AML)和维持治疗(降低 AML 复发风险)。米哚妥林可与化疗一起用于诱导和巩固治疗,或单独用于维持治疗。我们将介绍米哚妥林是什么、哪些人可能服用该药以及如何服用。我们还介绍了其主要副作用以及服用期间可能需要采取的任何特殊预防措施。
监管技术发展计划 钠快堆
免责声明 本报告是作为美国政府机构赞助的工作的记录而编写的。美国政府及其任何机构、芝加哥大学阿贡分校有限责任公司及其任何员工或官员均不对所披露的任何信息、设备、产品或流程的准确性、完整性或实用性做任何明示或暗示的保证,也不承担任何法律责任或义务,也不表示其使用不会侵犯私有权利。本文以商品名、商标、制造商或其他方式提及任何特定商业产品、流程或服务并不一定构成或暗示美国政府或其任何机构对其的认可、推荐或支持。本文表达的文档作者的观点和意见不一定代表或反映美国政府或其任何机构、阿贡国家实验室或芝加哥大学阿贡分校有限责任公司的观点和意见。
钠通道抑制药物和抗癌药物...
摘要 目的 抗癫痫和抗心律失常药物抑制电压门控钠 (Na +) 通道 (VGSC),临床前研究表明这些药物可减少肿瘤生长、侵袭和转移。我们研究了乳腺癌、肠癌和前列腺癌患者使用 VGSC 抑制剂与生存期之间的关联。设计回顾性队列研究。设置从临床实践研究数据链接中提取的个人电子初级医疗保健记录。参与者 132 996 名被诊断为乳腺癌、肠癌或前列腺癌的患者的记录。结果测量调整后的 Cox 比例风险回归用于分析与接触 VGSC 抑制剂相关的癌症特异性生存期。还考虑了非 VGSC 抑制抗癫痫药物和其他非 VGSC 阻滞剂的暴露。药物暴露被视为时变协变量,以解释永恒时间偏差。结果 在 1 002 225 人年的随访中,共有 42 037 人死于癌症。53 724 名(40.4%)癌症患者至少开过一次 VGSC 抑制剂处方。癌症死亡风险的增加与接触此类药物有关(HR 1.59,95% CI 1.56 至 1.63,p<0.001)。这适用于 VGSC 抑制三环抗抑郁药(HR 1.61,95% CI 1.50 至 1.65,p<0.001)、局部麻醉药(HR 1.49,95% CI 1.43 至 1.55,p<0.001)和抗惊厥药(HR 1.40,95% CI 1.34 至 1.48,p<0.001),并且在敏感性分析中持续存在。相反,暴露于 VGSC 抑制 1c 类和 1d 类抗心律失常药物与癌症特异性生存率显著提高相关(分别为 HR 0.75,95% CI 0.64 至 0.88,p<0.001 和 HR 0.54,95% CI 0.33 至 0.88,p=0.01)。结论 VGSC 抑制剂的使用与癌症患者死亡率之间的关联因适应症而异。使用 VGSC 抑制性抗心律失常药物(而非抗惊厥药物)支持了临床前数据的结果,即生存率有所提高。然而,这些关联可能还存在其他混杂因素,这凸显了进一步研究的必要性。
Invanz(Ertapenem钠)1 g粉末注射
•RCTS(总共28,873例患者):肌腱炎和脊髓炎炎很常见(<1%),肌腱破裂很少见(<0.1%)。•病例报告(10例肌腱破裂和15例肌腱炎):报告了所有三种类型的第三代AI病例,并涉及上肢和下肢。存在可能导致不良事件的其他药物和/或疾病。由于这些报告中的信息不足,因此在审查中未包括替索诺伏炎的病例报告。
映射钠诱导的代谢重编程
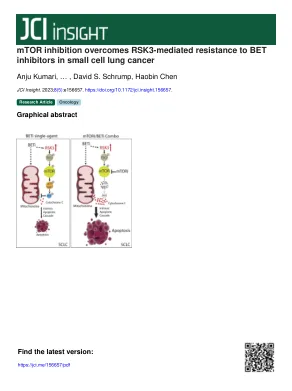
引言小细胞肺癌(SCLC)是一种顽固性恶性肿瘤,治疗方案有限(1)。由于近20年的治疗进展缺乏治疗的进展,其2年生存没有改善(2)。最近批准了几种新的治疗剂,包括免疫检查点抑制剂和lurbinectedin,但只有一部分患者会受益(3)。因此,不需要开发SCLC的新疗法。SCLC的潜在治疗候选者是溴结构域和末端结构域抑制剂(BETIS),它们靶向BET家族蛋白,即BRD2,BRD3,BRD4和BRDT。BET家族蛋白的主要功能是基因转录调节。betis与BET家族蛋白的溴结构域结合,并使它们与活性染色质分离,从而导致基因转录的抑制。由于贝蒂斯仅降低基因的一部分,尤其是与细胞谱系和驱动癌基因相关的基因的表达(4),因此对将此类药物应用于癌症治疗而引起了很大的兴趣。先前的研究报告说,小鼠SCLC非常容易受到贝蒂斯(5)的影响(5),但是人类SCLC系具有更广泛的敏感性(6)。最近我们发现,由于neu-rod1反式激活对BET家族蛋白的依赖,SCLC表达神经1(SCLC-N亚型)的子集特别容易受到BETIS的影响(7)。先前的几项研究报告说,针对PARP,HDAC6或BCL2的抑制剂在SCLC中与BETIS协同作用(8-11)。但是,然而,Beti在体内SCLC-N亚型肿瘤中仅具有适度的抗肿瘤活性(7),这需要一种组合策略来增强其在SCLC和SCLC的其他分子亚型中的抗抗效应。
钠作为电池中锂的绿色替代品
电池101在1980年代开发,并获得2019年诺贝尔化学奖的认可,锂离子电池已成为世界上最常用的电池之一。它为大多数手机和笔记本电脑提供动力,并且驱动了电动汽车生产的激增。与大多数电池一样,锂离子电池由三个主要组件组成:正电极(阴极),负电极(阳极)和两个之间的离子传输介质(电解质)。对于每个组件使用的材料都有多种选择,但是最常见的设计具有石墨制成的阳极(碳);由含锂的金属氧化物制成的阴极,例如氧化锂或锰氧化锂;以及结合锂盐和有机溶剂的电解质。