XiaoMi-AI文件搜索系统
World File Search System帕金森氏病的自主功能障碍研究的进步
缺乏研究,尤其是在英国,它调查了医疗和休闲大麻使用者的个体差异。横断面调查研究设计用于评估目前居住在英国的休闲大麻用户和医用大麻用户。邀请休闲大麻用户通过社交媒体参加。医用大麻使用者是从英国伦敦的Sapphire Medical Clinics招募的,该医疗诊所提供了基于大麻的药用产品的治疗。人口统计数据和大麻使用频率以及创伤后应激障碍症状(PCL-5),抑郁症状(流行病学研究中心抑郁症量表),性状和州焦虑症(州特征焦虑量表)以及大麻使用动机[全面的大麻动机问卷(CMMQ)]。使用卡方和独立样本t检验用于比较分类变量和正态分布的连续变量。使用方差分析(ANOVA)和t检验分析数据。统计显着性在p值<0.05时考虑。 调查由161名参与者完成。 医用大麻使用者年龄较大,经常消耗大麻,在CMMQ上具有更高的“睡眠”动机,并且在自我报告的当前诊断神经系统问题,情绪障碍和焦虑症的诊断中患病率更高(P <0.05)。 娱乐性大麻用户的使用动机得分更高(例如,“享受”,“应对”,“实验”,“无聊”和“庆祝”)和较高的州焦虑得分(p <0.05)。统计显着性在p值<0.05时考虑。调查由161名参与者完成。医用大麻使用者年龄较大,经常消耗大麻,在CMMQ上具有更高的“睡眠”动机,并且在自我报告的当前诊断神经系统问题,情绪障碍和焦虑症的诊断中患病率更高(P <0.05)。娱乐性大麻用户的使用动机得分更高(例如,“享受”,“应对”,“实验”,“无聊”和“庆祝”)和较高的州焦虑得分(p <0.05)。两组使用大麻的最常见动机是“享受”,“低风险”和“睡眠”。群体之间的性别,“低风险”动机,创伤后应激障碍症状,抑郁评分,特质焦虑评分,与药物使用相关疾病的自我报告的患病率以及过去的酒精,烟草或咖啡因的消费率没有差异(P> 0.05)。当前的研究不仅证明了娱乐和医用大麻使用者之间大麻消费的年龄和动机差异,而且还显示了潜在重叠的领域,包括心理健康成果,过去的药物使用和性别。这些特定于英国的发现表明,休闲大麻使用者会感到更高的状态焦虑,强调需要进一步评估大麻的潜在焦虑/抗焦虑特性。这些发现证明了研究大麻使用者中个体差异的重要性,并对未来的研究,临床实践和立法具有重要意义。
帕金森氏病的慢性疼痛:患病率,性别差异,
此预印本版的版权持有人于2025年2月12日发布。 https://doi.org/10.1101/2025.02.09.25321969 doi:medrxiv preprint
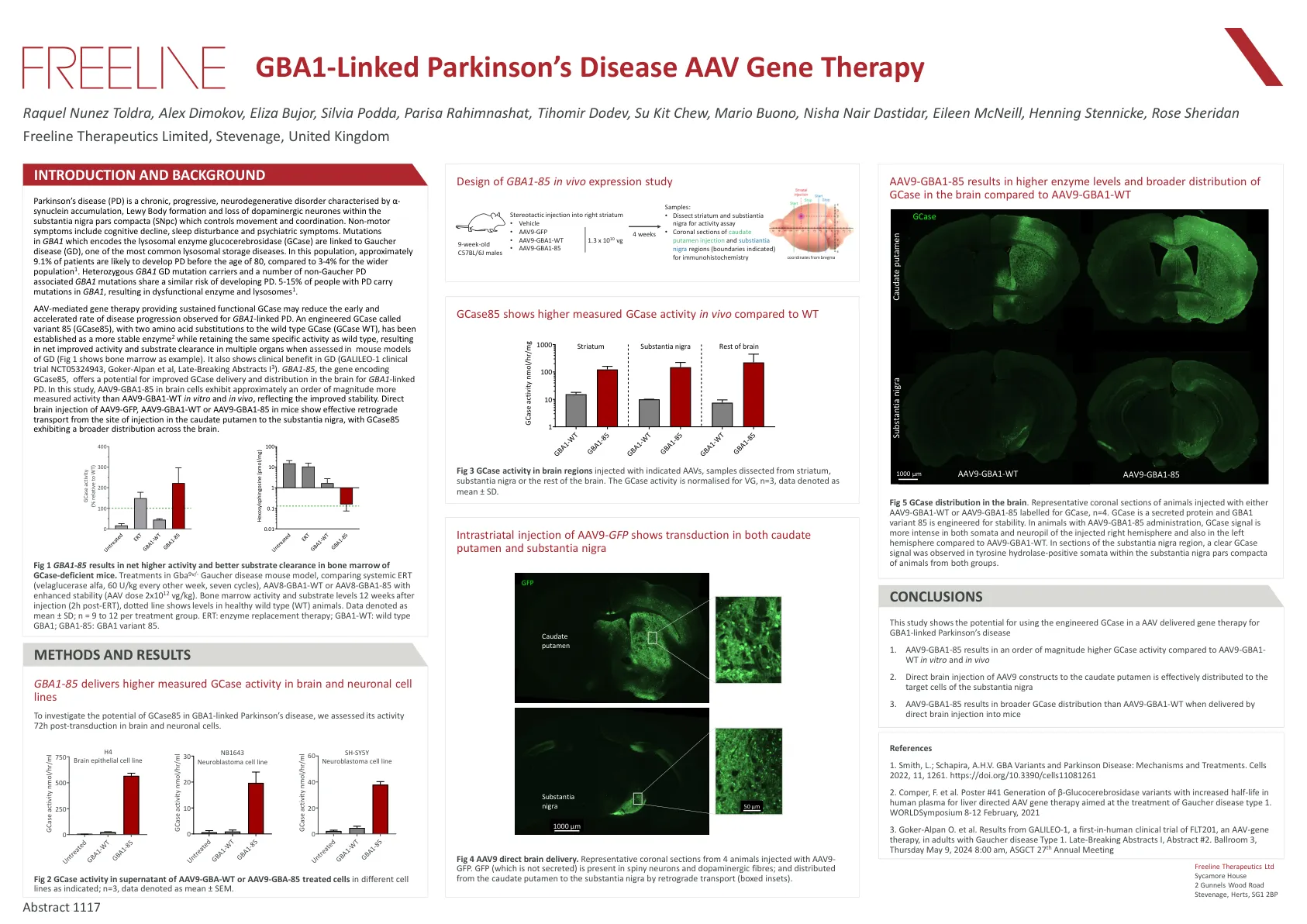
与GBA1连接的帕金森氏病AAV基因治疗
帕金森氏病(PD)是一种慢性,进行性,神经退行性疾病,其特征是α-突触核蛋白积累,Lewy身体形成和质体nigra Pars Compacta(SNPC)中多巴胺能神经元的丧失,控制运动和配位。非运动症状包括认知能力下降,睡眠障碍和精神病症状。GBA1中编码溶酶体酶葡萄糖脑苷酶(GCASE)的突变与Gaucher病(GD)有关,Gaucher病(GD)是最常见的溶酶体储存疾病之一。在这一人群中,大约9.1%的患者可能在80岁之前发展PD,而更广泛的人群为3-4%。杂合GBA1 GD突变携带者和许多非Gaucher PD相关的GBA1突变具有相似的发展PD风险。5-15%的PD患者在GBA1中携带突变,导致功能失调的酶和溶酶体1。
丁酸酯在帕金森氏病中的复杂作用
帕金森氏病(PD)是一种复杂的神经退行性疾病,通常与胃肠道(GI)功能障碍有关。胃肠道是多种微生物的所在地,其中细菌可以通过各种机制影响宿主。可以在肠道中作用,但也可以通过现在确定为微生物群 - 甲状脑轴轴的大脑中发挥作用。在患有PD的人中,肠杆菌组成通常与非PD个体不同。除了组成变化外,PD在PD中还改变了肠道 - 微生物的代谢活性。特别是,经常据报道,短链脂肪酸(SCFA)的关键生产者以及SCFA本身的浓度在粪便和PD患者的血液中被改变。这些SCFA,其中包括丁酸酯是宿主的必需营养素,是胃肠道上皮细胞的主要能源。此外,丁酸酯在调节各种宿主反应方面起着关键作用,尤其是与炎症有关。研究表明,丁酸水平的降低可能在PD的发作和进展中起关键作用。此外,已经表明,通过益生菌,益生元,丁酸钠补充钠和粪便移植能够对患有PD的丁酸酯水平恢复,可以对运动的运动和非运动型疾病产生有益的作用。本评论概述了PD患者中改变的肠杆菌组成和相应的代谢产物产生的证据,特别关注SCFA丁酸。除了在临床和临床前报告中介绍有关SCFA的最新研究外,还讨论了在治疗环境中使用基于微生物组的方法靶向丁酸酯产生的证据。
在帕金森氏病中平衡营养和胃肠道问题
Pasricha TS,Guerrero-Lopez IL,Kuo B.帕金森氏病中胃肠道症状的管理:对临床表现,检查和治疗的全面综述。J Clin胃肠烯醇。2024; 58(3):211-220。出版了2024年3月1日。DOI:10.1097/MCG.000000000000001961
HLA-DRB1与帕金森氏病中吸烟之间的相互作用
1帕里斯 - 萨克莱大学,UVSQ,UNIV。Paris-Sud, Inserm, Team " Exposome, Heredity, Cancer, and Health " , CESP, Villejuif, France 2 Nantes Université, INSERM, Center for Research in Transplantation and Translational Immunology, Nantes, France 3 Centre for Genetic Epidemiology, Institute for Clinical Epidemiology, and Applied Biometry, University of Tubingen, Tübingen, Germany 4 Department for神经退行性疾病,赫尔蒂临床脑研究所,图宾根大学,德国图宾根大学5德国5个神经退行性疾病中心(DZNE),德国Tubingen,德国6转化神经科学,卢克斯堡系统生物医学中心(LCSB),卢克斯堡,卢克斯郡,卢克斯郡, Genetics, Helmholtz Zentrum München, Neuherberg, Germany 8 Molecular Genetics Section, Laboratory of Neurogenetics, NIA, NIH, Bethesda, Maryland, USA 9 Center For Alzheimer ' s and Related Dementias, NIA, NIH, Bethesda, Maryland, USA 10 Grif fi th Institute for Drug Discovery, Grif fi th University, Nathan,昆士兰,澳大利亚昆士兰11号神经病学系,维也纳医科大学,奥地利维也纳12号神经病学系,奥地利维也纳Klinik Ottakring神经病学系13坦兹神经退行性疾病研究中心,多伦多大学多伦多大学,多伦多大学,加拿大多伦多大学,加拿大加拿大的埃德蒙·J·萨弗里亚(Edondond Shother),帕克森(Morton),帕克森(Morton),多伦多,帕克森(Morton),帕克森(Morton)。加拿大安大略省多伦多的UHN 15神经病学系,多伦多大学多伦多大学,加拿大安大略省,加拿大安大略省16克里姆比尔脑研究所,多伦多,多伦多,安大略省,加拿大,加拿大17分子医学和创新疗法中心,
帕金森氏病的临床诊断-Thieme Connect
在1817年,詹姆斯·帕金森(James Parkinson)描述了6例患有神经系统综合征的患者的临床特征,该患者尚未得到很好的特征,他称之为“麻痹脂肪”或“震动麻痹” 1。在他的观察中,帕金森帕金森(Parkinson)捕获了主要的临床特征,例如阴险的发作,具有渐进的残疾课程,存在不对称身体受累的休息震颤,随着躯干,颈部和四肢的流向,姿势变化,异常步态,带有节日,持续性疾病,疾病和droloolloolloolloroollior and droloollorooling。他还描述了便秘和认知保存的存在。对这种新综合征的描述逐渐被逐渐了解当时的医学文献,在19世纪末,两位作者做出了重要的贡献。2 - 4 Trousseau描述了肌肉刚性的存在和重复运动的逐步减慢,还指出患者随着条件的进行而认知能力下降。charcot定义为疾病最重要的表现和运动障碍的主要来源。他建议同名的帕克森病(PD)庆祝原始描述符。charcot还指出,该综合征的临床变异型具有非典型表现,没有震颤,较长的刚度,偏瘫和“惊人的脸”。在20世纪初,即1917年至1926年之间,脑炎脑炎大流行使后帕金森氏症作为后遗症,这是帕金森主义的第一个认可的次要原因。当时,像Critchley这样的作者试图表征各种帕金森氏综合症,例如“动脉粥样硬化帕金森氏症”,已经认识到该综合征的异质性及其可能的病因。4此外,许多作者的研究包括Lewy,Tretiakoff,Marinesco,Foix和Nicolesco,可以确定可以确定的是Nigra nigra compacta的改变以及Lewy Bodies(LBS)的存在是PD的基本病理底物。在1967年,霍恩和雅尔在levodopa时代就撰写了有关帕金森氏症的开创性研究。5他们描述了802例患者的临床特征,“所有接受的基本症状迹象:休息震颤,塑性刚度,稀少或延迟运动,缓慢以及姿势和矫正后的爆发”。pd被定义为疾病的主要或“特发性”形式。对诱导临床症状或存在相关或非典型神经系统异常的存在的基本过程的怀疑,排除了这个特发性诊断类别的给定病例。作者定义了二次帕金森氏症,当该综合征与潜在病因学剂相关时和/或有迹象表明帕金森氏症是影响不参与原型综合征通常不涉及的系统的病理上更广泛的疾病的一部分。这些次要病例被塞在后脑帕金森氏症或“其他”中。最后,一定比例的病例被分类为具有不分散的帕金森氏症,因为它们被认为无法确定临床迹象是否是主要的
帕金森主义改变了基底神经节皮质网络
这篇早期版本的文章已经过同行评审和接受,但尚未通过构图和复制过程。最终版本的样式或格式可能会略有不同,并且将包含指向任何扩展数据的链接。
帕金森主义改变了基底神经节皮质网络
在β带中升高的同步振荡活性已被认为是帕金森氏病(PD)的病理生理标记。最近的研究表明,帕金森氏症与丘脑下核(STN)中β爆发活性的幅度和持续时间的增加密切相关。但是,如何从基底神经节(丘脑皮层(BGTC)运动网络)从正常状态变为帕金森氏症状态。在这项研究中,我们同时记录了三个雌性恒河猕猴中的STN,Globus Pallidus(GPI)(GPI)的内部段(GPI)(GPI)和Primary Motor Cortex(M1)的局部现场潜在活性,并表征了Beta爆发活动如何随着动物从正常而过渡到更严重的parkinsonian状态而变化。帕金森氏症与在STN和GPI的低β频段(8 - 20 Hz)中持续时间更长的β爆发发生率增加,而在M1中却没有。我们观察到Beta爆发活性的更大并发,但是,在PD中的所有记录位点(M1,STN和GPI)中。在BGTC网络的多个节点上同时存在低β爆发活性,而PD电动标志的严重程度增加了令人信服的证据,以支持低Beta同步旋转振荡的假说在PD的潜在病理生理学中起重要作用。鉴于其沉浸在整个电机电路中,我们假设这种升高的β波段活性会干扰BGTC网络中信息流的空间 - 时间处理,从而导致PD中的运动功能受损。
中脑器官 - 帕金森氏病的发展和应用
在这篇综述中,我们讨论了使用脑器官来建模中脑及其相关的神经退行性疾病:PD(图1)。PD的标志是在底骨pars compacta中中脑多巴胺能(MDA)神经元的选择性死亡,导致Nigrostriatal途径退化[2]。这在临床上表现为运动缺陷,包括胸肌,僵化,震颤和姿势不稳定性[3]。PD已使用动物模型进行了广泛的研究;此外,从人类多能干细胞(HPSC)中产生人类神经元的能力使PD机制可以在人类环境中进行建模。患者衍生的诱导多能干细胞(IPSC)的产生使多样化的遗传敏感性和治疗反应以及个性化治疗策略的演变得以研究[4]。