XiaoMi-AI文件搜索系统
World File Search SystemPHH-1V HIPRA 疫苗
1 医疗信息,HIPRA Human Health,西班牙 2 预防医学和公共卫生领域。西班牙巴利亚多利德医学院和大学临床医院 3 西班牙马德里 10 月 12 日大学医院预防医学系 4 西班牙马德里拉巴斯大学医院免疫学系 5 微生物学系。医学院和“里奥奥尔特加”大学医院。西班牙巴利亚多利德 6 预防医学和公共卫生服务。西班牙阿斯图里亚斯 Vital Álvarez Buylla 医院 7 预防医学和公共卫生。西班牙胡安卡洛斯国王大学 8 西班牙莱里达大学(UdL)护理与理疗学院 9 西班牙巴塞罗那儿科医生 10 家庭医学。西班牙阿尔赫西拉斯北部医疗保健中心 11 名誉高级研究员。疫苗研究领域,FISABIO,瓦伦西亚,西班牙 12 卫生领域主任,文塞斯,西班牙 13 IRTA-UAB 动物健康联合研究单位,动物健康研究中心(CReSA),巴塞罗那自治大学校园,贝拉特拉,西班牙 14 IRTA,动物健康计划,CReSA,巴塞罗那自治大学校园,贝拉特拉,西班牙 15 医疗和政府事务。 HIPRA 人类健康,西班牙
缺血性中风中的间充质干细胞(...
摘要引言中风是一个严重的公共卫生问题,因为尽管它传播了再启动疗法,但它是全球残疾的主要原因。用干细胞给药增强大脑可塑性是一种有希望减少这些患者后遗症的创新疗法。方法和分析我们已经开发了IIB期,多中心,随机,双盲,安慰剂控制的临床试验方案,以评估静脉内给予同种异性脂肪组织的安全性和功效。三十名患者将以1:1的方式随机分配,以在中风症状发作后的前4天内尽快接受静脉安慰剂或同种异体AD-MSC。随机分解后24个月的患者将随访。主要目的是通过报告两个治疗组的所有不良事件以及神经或系统并发症的所有不良事件以及同种异体AD-MSC的早期静脉内给药的安全评估。次要目标通过评估改良的Rankin量表和美国国立卫生研究所的变化在整个随访期内评估早期静脉注射AD-MSC治疗在急性缺血性中风中的功效。此外,将在各种访问时测量脑修复生物标志物。研究结果将通过以开放访问格式和会议演示的同行评审出版物进行传播。伦理和传播这项临床试验已获得拉巴斯大学医院(西班牙马德里)临床研究伦理委员会和西班牙药物和健康产品机构的批准,并已在Eudra CT(2019- 001724-35)和临床中注册。
SVCE 特别会议演示 041921
MWh 1 Slate 太阳能 + 储能 (4 小时) Kings Cnty, CA 2021 年 7 月 17 日 93.0 266 6.7% 46.5 4 186 2 Big Beau 太阳能 + 储能 (4 小时) Kern Cnty, CA 2021 年 12 月 70.4 230 5.8% 22 4 88 3 Ormat Casa Diablo Binary Geothermal Mono Cnty, CA 1021 年 12 月 7.0 57 1.4% 4 Coso Geothermal Inyo Cnty, CA 1522 年 1 月 43.8 380 9.6% 5 Rabbitbrush 太阳能 + 储能 (2.5 小时) Kern County, CA 1522 年 6 月 40.0 119 3.0% 8 2.5 20 6 Yellow Pine 太阳能 + 储能 (4 小时) Clark County, NV 20 22年12月 50.0 161 4.1% 26 4 104 7 Aratina 太阳能+储能 (3 小时) 加州克恩县 20 23年6月 80.0 265 6.6% 20 3 60 8 Atlas Solar 亚利桑那州拉巴斯县 10 22年12月 50.0 151 3.8% 0 0 0 9 Angela 太阳能+储能 (4 小时) 亚利桑那州图莱里县 15 23年3月 20.0 57 1.4% 10 4 40 10 San Luis West 太阳能+储能 (4 小时) 加州弗雷斯诺县 15 23年12月 62.5 163 4.1% 15.625 4 62.5 11 AES Mountain View Wind 加州河滨县 20 23年1月 33.5 128 3.2% 总计 550.2 1977.7 50% 148.1 25.5 561
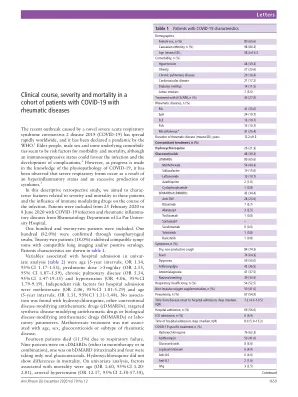
表 1 COVID-19 患者特征
在这项描述性回顾性研究中,我们旨在描述这些患者的严重程度和死亡率相关特征以及免疫调节药物对感染病程的影响。研究对象为 2020 年 2 月 25 日至 2020 年 6 月 8 日期间在拉巴斯大学医院风湿病科就诊的患有 COVID-19 感染和风湿性炎症疾病的患者。共纳入 122 名患者。其中 100 名(82.0%)通过鼻咽拭子确诊。22 名患者(18.0%)表现出相符的症状,且肺部影像学检查结果相符和/或血清学检查呈阳性。患者特征如表 1 所示。单因素分析显示(表2),与住院相关的变量包括年龄(5年间隔;OR 1.34,95% CI 1.17-1.55)、泼尼松剂量>5mg/天(OR 2.55,95% CI 1.07-5.59)、慢性肺部疾病(OR 5.34,95% CI 1.47-19.35)和高血压(OR 4.06,95% CI 1.79-9.19)。住院的独立危险因素是甲氨蝶呤(OR 2.06,95% CI 1.01-5.29)和年龄(5年间隔;OR 1.31,95% CI 1.11-1.48)。未发现与羟氯喹、其他常规抗风湿药物 (cDMARDs)、靶向合成抗风湿药物或生物抗风湿药物 (bDMARDs) 或实验室参数有任何关联。甲氨蝶呤治疗与年龄、性别、糖皮质激素或风湿病亚型无关。14 名患者 (11.5%) 死于呼吸衰竭。9 名患者使用 cDMARDs(单药或联合治疗),1 名使用 bDMARD(利妥昔单抗),4 名仅服用口服糖皮质激素。羟氯喹在死亡率方面没有差异。单变量分析显示,与死亡率相关的因素包括年龄(OR 1.60,95% CI 1.20-2.01)、动脉高血压(OR 12.17,95% CI 2.58-57.38)、
具有阿斯曲霉风险的患者的先发性基因分型策略
摘要 引言 侵袭性曲霉病是血液病患者发病和死亡的最重要原因。目前,伏立康唑是侵袭性真菌病的一线治疗药物。伏立康唑的药代动力学个体间差异取决于遗传因素。伏立康唑总代谢的 70%–75% 参与 CYP450,主要是 CYP3A4 和 CYP2C19,其余 25%–30% 的代谢由单加氧酶黄素进行。CYP2C19 单核苷酸多态性可以解释伏立康唑代谢中 50%–55% 的变异性。材料和方法主要目的是比较预先伏立康唑基因分型与常规实践的效率。主要结果是第五天血清伏立康唑是否在治疗范围内。次要结果是与伏立康唑相关的治疗失败和首次给药后 90 天内不良事件的综合变量。总共将招募 146 名可能接受伏立康唑治疗的侵袭性曲霉病风险患者,并进行 CYP2C19 基因分型。如果患者最终接受伏立康唑治疗,他们将被随机分配(1:1 实验/对照)。在实验组中,患者将根据药物遗传学算法接受剂量,包括 CYP2C19 基因型和临床及人口统计信息。在对照组中,患者将根据临床实践指南接受剂量。此外,将进行西班牙国家医疗保健系统 (NHS) 的成本效益评估。将对每个组进行直接成本计算。结论这项试验将提供有关在西班牙 NHS 中实施预防性伏立康唑基因分型策略的可行性和成本效益的信息。伦理与传播 该方案的西班牙语版本已通过拉巴斯大学医院伦理委员会和西班牙药品和医疗器械管理局的评估和批准。 试验结果
使用Eltrombopag改善抗CD19 CAR-T细胞治疗的患者的血小板减少症和静息需求
1 Virgen delRocíO,塞维利亚塞维利亚生物医学研究所,塞维利亚大学,西班牙塞维利亚41004; juanlu_jlr@hotmail.com(J.L.R. -O。 div>); josea.perez.simon.sspa@juntadeandalucia.es(J.A.P.-S。)2大学医院28041年10月12日,西班牙马德里; josemspina@gmail.com(J.M.S.-P。)3西班牙瓦伦西亚大学46010大学关闭医院的含健康研究所4 46010 4血液学部门,莫拉莱斯 - 摩尔米尔大学医院IMIB-PASCUAL GRILLA区域血液化中心,30008 Murcia,Spain,Spain,Spain; oilpezgodino@gmail.com 5血液学服务,大学和Polyte Hospital La Fe,46026西班牙瓦伦西亚6号儿童儿童医院耶稣,28009,西班牙马德里; blanca.herrero@salud.madrid.com 7 IBSAL,CIBERONC,C ciberonc,C to Citr-ibmcc(USAL-CSIC),西班牙萨拉曼卡大学医院(西班牙),西班牙萨拉曼卡37007; lucialopezcorral@usal.es(L.L.-C。); aamartin@saludcastillayleon.es(A.A..M。)8 Ram o n y Cajal大学医院,28034西班牙马德里9号,9010 Gran Canaria大学医院NEGRIN博士,35010 Las Palmas de Gran Canaria Canaria Canaria Canaria Canaria Canaria,西班牙10号,西班牙10号,卫生调查研究所,Barrona Saniation san santhitution saniTute of Sanitalight of Concerca西班牙nmartinc@clinic.cat 12 University vall d'Hebron医院,西班牙巴塞罗那08035; pbalsalobre@geth.es(P.B. div>); sfilaferro@geth.es(s.f.) div>13 RECERCA SANT JOAN dedéu,Sant Joan dedédéuU U,西班牙08950; anna.alonso@sjd.es 14西班牙移植群体船体Éticoand Cell Therapy,28040,西班牙马德里; pbarba@vhio.net 15西班牙马德里28034的拉巴斯大学医院儿科血液肿瘤学系; Anerezmartinez@salud.madrid.org 16儿科系,马德里自治大学,28034马德里,西班牙17 Cibere-ICIII,IDIPAZ-CNI
一组患有风湿性疾病的 COVID-19 患者的临床病程、严重程度和死亡率
在这项描述性回顾性研究中,我们旨在描述这些患者的严重程度和死亡率相关特征以及免疫调节药物对感染病程的影响。研究对象为 2020 年 2 月 25 日至 2020 年 6 月 8 日期间在拉巴斯大学医院风湿病科就诊的患有 COVID-19 感染和风湿性炎症疾病的患者。共纳入 122 名患者。其中 100 名(82.0%)通过鼻咽拭子确诊。22 名患者(18.0%)表现出相符的症状,且肺部影像学检查结果相符和/或血清学检查呈阳性。患者特征如表 1 所示。单因素分析显示,与住院相关的变量(表 2)包括年龄(5 年间隔;OR 1.34,95% CI 1.17-1.55)、泼尼松剂量 >5 mg/天(OR 2.55,95% CI 1.07-5.59)、慢性肺部疾病(OR 5.34,95% CI 1.47-19.35)和高血压(OR 4.06,95% CI 1.79-9.19)。住院的独立危险因素是甲氨蝶呤(OR 2.06,95% CI 1.01-5.29)和年龄(5 年间隔;OR 1.31,95% CI 1.11-1.48)。未发现与羟氯喹、其他常规抗风湿药物 (cDMARDs)、靶向合成抗风湿药物或生物抗风湿药物 (bDMARDs) 或实验室参数有任何关联。甲氨蝶呤治疗与年龄、性别、糖皮质激素或风湿病亚型无关。14 名患者 (11.5%) 死于呼吸衰竭。9 名患者使用 cDMARDs(单药或联合治疗),1 名使用 bDMARD(利妥昔单抗),4 名仅服用口服糖皮质激素。羟氯喹在死亡率方面没有差异。单变量分析显示,与死亡相关的因素包括年龄(OR 1.60,95% CI 1.20- 2.01)、动脉高血压(OR 12.17,95% CI 2.58-57.38)、肺部疾病(OR 5.36,95% CI 1.60-17.94)和泼尼松剂量>5 mg/天(OR 5.70,95% CI 1.63-19.92)。最近爆发的 COVID-19 引起了人们对炎症性风湿病患者管理的担忧。然而,一些报告表明,通常用于治疗风湿病的治疗方法可能对 COVID-19 有效。 4 在我们的系列研究中,与其他群体相比,因感染严重而需要住院的患者比例较高 (56.6%),这可能是由于合并症患病率较高,尤其是高血压,糖皮质激素的使用率较高或对更严重病例的潜在选择偏见。5 6
Leonard、Szekely 和 Wang:2023 年 ACS 可持续化学与工程讲座奖获奖者
(1) Seuferling, T.;Larson, T.;Barforoush, J.;Leonard, KC 用于高电流密度下电化学分解水的碳酸盐衍生多金属催化剂。ACS Sustainable Chem. Eng. 2021 ,9 ,16678 − 16686。 (2) Stalcup, MA;Nilles, CK;Lee, H.-J.;Subramaniam, B.;Blakemore, JD;Leonard, KC 在 CO 2 膨胀电解质中进行有机电合成:实现选择性苯乙酮羧化生成阿卓酸。ACS Sustainable Chem. Eng. 2021 ,9 ,10431 − 10436。 (3) Farris, BR;Niang-Trost, T.;Branicky, MS; Leonard,KC 使用人工策划的数据集评估电化学 CO 2 还原的机器学习模型。ACS 可持续化学工程。2022,10,10934 − 10944。 (4) Park,S.-H.;Yang,C.;Ayaril,N.;Szekely,G. 来自生物质衍生构建块的耐溶剂薄膜复合膜:壳聚糖和 2,5-呋喃二甲醛。ACS 可持续化学工程。2022,10,998 − 1007。 (5) Voros,V.;Drioli,E.;Fonte,C.;Szekely,G. 通过连续和同时分离抗氧化剂进行工艺强化:一种橄榄叶废料的升级回收方法。ACS 可持续化学工程。 2019, 7, 18444 – 18452。 (6) Didaskalou, C.;库派,J.;切里,L.;巴拉巴斯,J.;瓦斯,E.;霍尔茨尔,T.; Szekely, G. 用于集成合成-分离平台的膜接枝不对称有机催化剂。 ACS目录。 2018, 8, 7430 – 7438. (7) 李杰;特雷奇科,M.;尹,J.;朱,Y。李,G。宋,S。杨,H。李,J。吴,J。卢,J。 Wang, X. 分子成像中的机器视觉自动手性分子检测和分类。 J. Am.化学。苏克。 2021 ,143 ,10177 − 10188。 (8) Zheng, Y.;Wang, X.;Wu, Z. 间歇结晶过程的机器学习建模和预测控制。Ind. Eng. Chem. Res. 2022 ,61 ,5578 − 5592。 (9) Zhu, X.;Ho, C.-H.;Wang, X. 生命周期评估和机器学习在绿色化学替代品高通量筛选中的应用。ACS Sustainable Chem. Eng. 2020 ,8 ,11141 − 11151。
2030 年的计算病理学:德尔菲研究预测未来十年人工智能在病理学中的作用
a 西班牙科尔多瓦圣胡安迪奥斯医院 HT Médica 研发部 b 西班牙马德里自治大学医学院 c 美国明尼苏达州罗切斯特市梅奥诊所实验室医学和病理学系 d 日本千叶县鸭川市龟田医疗中心病理学系 e 荷兰奈梅亨拉德堡德大学医学中心病理学系 f 美国密歇根州安娜堡市密歇根大学病理学系 g 美国马萨诸塞州波士顿市麻省总医院/哈佛医学院综合诊断中心病理学系 h 新西兰惠灵顿市奥塔哥大学惠灵顿医学与健康科学学院 i 瑞典斯德哥尔摩市卡罗琳斯卡医学院肿瘤病理学系 j 葡萄牙波尔图市波尔图大学分子病理学与免疫学研究所病理实验室 k 美国佐治亚州亚特兰大市埃默里大学病理学与实验室医学系 l Azienda 病理学部意大利卡尔塔吉罗内格拉维纳医院卡塔尼亚省立卫生研究院 m 西班牙格拉纳达圣塞西利奥临床大学医院病理学系 n 美国宾夕法尼亚州匹兹堡大学医学中心解剖病理学系 o 美国马萨诸塞州波士顿麻省总医院和哈佛医学院病理学系 p 荷兰鹿特丹伊拉斯姆斯大学医学中心病理学系 q 美国威斯康星州密尔沃基威斯康星医学院病理学系 r 加拿大温哥华不列颠哥伦比亚大学迈克尔·史密斯基因组科学中心病理学与实验室医学系 s 德国海德堡海德堡大学医院病理学研究所 t 美国德克萨斯州奥斯汀 Sonic Healthcare 病理学系 u 美国康涅狄格州纽黑文耶鲁大学医学院病理学系 v 美国密歇根州底特律亨利·福特医院病理学系 w英国利兹 x 西班牙马德里拉巴斯大学医院整形与重建外科系 y 西班牙马德里 Puerta de Hierro-Majadahonda 大学医院普通外科和消化道系 z 西班牙哈恩 Clínica Las Nieves HT Médica 综合诊断系 aa 美国加利福尼亚州斯坦福斯坦福大学医学院病理学系和医学与成像人工智能中心
2030 年的计算病理学:德尔菲研究预测未来十年人工智能在病理学中的作用
a 西班牙科尔多瓦圣胡安迪奥斯医院 HT Médica 研发部 b 西班牙马德里自治大学医学院 c 美国明尼苏达州罗切斯特市梅奥诊所实验室医学和病理学系 d 日本千叶县鸭川市龟田医疗中心病理学系 e 荷兰奈梅亨拉德堡德大学医学中心病理学系 f 美国密歇根州安娜堡市密歇根大学病理学系 g 美国马萨诸塞州波士顿市麻省总医院/哈佛医学院综合诊断中心病理学系 h 新西兰惠灵顿市奥塔哥大学惠灵顿医学与健康科学学院 i 瑞典斯德哥尔摩市卡罗琳斯卡医学院肿瘤病理学系 j 葡萄牙波尔图市波尔图大学分子病理学与免疫学研究所病理实验室 k 美国佐治亚州亚特兰大市埃默里大学病理学与实验室医学系 l Azienda 病理学部意大利卡尔塔吉罗内格拉维纳医院卡塔尼亚省立卫生研究院 m 西班牙格拉纳达圣塞西利奥临床大学医院病理学系 n 美国宾夕法尼亚州匹兹堡大学医学中心解剖病理学系 o 美国马萨诸塞州波士顿麻省总医院和哈佛医学院病理学系 p 荷兰鹿特丹伊拉斯姆斯大学医学中心病理学系 q 美国威斯康星州密尔沃基威斯康星医学院病理学系 r 加拿大温哥华不列颠哥伦比亚大学迈克尔·史密斯基因组科学中心病理学与实验室医学系 s 德国海德堡海德堡大学医院病理学研究所 t 美国德克萨斯州奥斯汀 Sonic Healthcare 病理学系 u 美国康涅狄格州纽黑文耶鲁大学医学院病理学系 v 美国密歇根州底特律亨利·福特医院病理学系 w英国利兹 x 西班牙马德里拉巴斯大学医院整形与重建外科系 y 西班牙马德里 Puerta de Hierro-Majadahonda 大学医院普通外科和消化道系 z 西班牙哈恩 Clínica Las Nieves HT Médica 综合诊断系 aa 美国加利福尼亚州斯坦福斯坦福大学医学院病理学系和医学与成像人工智能中心