XiaoMi-AI文件搜索系统
World File Search System与杏仁核相关的电纹指纹进行调制,并通过神经反馈训练进行调节,并与深度脑激活相关:边界人格障碍中的概念验证
。cc-by-nd 4.0国际许可证可永久提供。是作者/资助者,他已授予Medrxiv的许可证,以显示预印本(未通过同行评审证明)预印版本的版权持有人此版本发布于2023年3月30日。 https://doi.org/10.1101/2023.03.28.23287782 doi:medrxiv preprint
研究发现冥想可以引起与记忆和情绪调节相关的深层大脑区域的变化
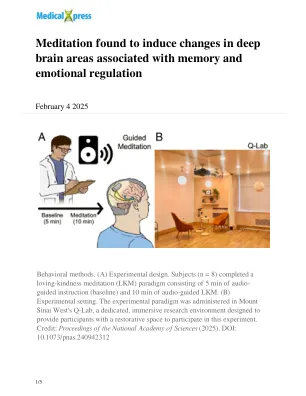
“传统上,使用头皮脑电图等标准方法研究人类的这些深层边缘大脑区域一直具有挑战性。我们的团队能够通过利用从独特患者群体收集的数据来克服这一挑战:癫痫患者通过手术植入设备,可以通过植入杏仁核和海马深处的电极进行慢性脑电图记录,”伊坎医学院生物医学科学研究生院神经科学博士生、论文第一作者克里斯蒂娜·马赫 (Christina Maher) 表示。
心理学的科学和教师ATAR年
• developmental stages across the lifespan – prenatal, infancy, childhood, adolescence, early adulthood, middle age, older age • role of brain neural plasticity in infancy and adolescent development through the lifespan ▪ adaptive and developmental plasticity ▪ infancy ▪ stages of plasticity – proliferation, migration, circuit formation synaptogenesis , synaptic pruning, myelination ▪ adolescence ▪ effect of changes在青春期的行为和情绪的大脑结构中 - 小脑,杏仁核,call体和额叶前叶皮层o额叶发展对行为和情感的变化影响 - 前额外
CRISPR 破坏和英国生物库对高度保守的多态性增强子的分析表明,该基因与男性焦虑和乙醇摄入有关
摘要 全球 5.9% 的死亡与过量饮酒有关。然而,这一数字在男性中尤其严重,7.6% 的死亡可归因于饮酒。先前的研究发现,在不同男性群体中,甘丙肽 (GAL) 基因的基因型与焦虑和酒精滥用之间存在显著的相互作用,但无法确定其中的机制。为了解决这些问题,本研究分析了英国生物银行的人类队列,并发现高度保守的人类 GAL5.1 增强子的等位基因变异 (GG 或 CA 基因型)、酒精摄入量 (AUDIT 问卷分数) 和男性焦虑之间存在显著的相互作用 (n = 115,865; p = 0.0007)。至关重要的是,使用 CRISPR 基因组编辑破坏小鼠的 GAL5.1 显著降低了杏仁核和下丘脑中的 GAL 表达,同时相应减少了 KO 小鼠的乙醇摄入量。有趣的是,我们还发现雄性 GAL5.1KO 动物的焦虑样行为减少的证据与我们在英国生物库研究中看到的人类相似。通过生物信息学分析和共转染研究,我们进一步确定了 EGR1 转录因子,该因子与杏仁核和下丘脑中的 GAL 共同表达,对蛋白激酶 C (PKC) 支持的 GG 基因型 GAL5.1 活性很重要,但在 CA 基因型中则不那么重要。我们独特的研究采用了人类关联分析、小鼠 CRISPR 基因组编辑、动物行为分析和细胞培养研究的新组合,以确定一种高度保守的调节机制,该机制将焦虑和酒精摄入联系起来,这可能导致男性对焦虑和酒精滥用的敏感性增加。
e2062232024.full.pdf
慢性疼痛和抑郁症的合并症对两者的治疗构成了巨大的挑战,因为它们会以未知的机制相互加剧。作为后岛的皮层(PIC)整合了多种体感和情感信息,并与慢性疼痛或抑郁症有关,我们假设PIC及其预测可能有助于慢性慢性疼痛和抑郁症的病理生理学。我们表明,在幼稚和神经性疼痛的雄性小鼠中,机械,热,厌恶,压力性和开胃刺激很容易激活PIC神经元。PIC神经元的光遗传激活诱导的痛觉过敏并在天真小鼠中厌恶调节,而这些神经元的抑制导致了镇痛,调节位置偏好(CPP)以及天真和SNI小鼠的抗抑郁作用。结合神经元跟踪,上遗传学和电生理技术,我们发现从图片到基底外侧杏仁核(BLA)的单突触谷氨酸助剂和腹腔核核(VM)的基底外侧杏仁核(bla)含糊不清的神经膜中的神经症中的神经症状症状症状症状症状。在SNI小鼠中,这两种投影都伴随着PIC,BLA和VM神经元的多动症,并且对这些投影的抑制导致了镇痛,CPP和抗抑郁药样效应。本研究表明,PIC→BLA和PIC→VM投影的增强可能是神经性疼痛中痛觉过敏和类似sion的行为的重要病理生理碱基,并且可以逆转增强性可能是对稳定的慢性疼痛和抑郁症的有前途的治疗策略。
长期戒断过程中焦虑的行为是由肠道微生物疾病驱动的,并受到益生菌治疗的减弱
摘要长期的阿片类药物戒断期间焦虑的发展增加了复发到成瘾循环的风险。了解在阿片类药物戒断过程中驱动焦虑的机制可能有助于促进治疗剂的发展,以防止负面影响并促进持续的戒酒。我们的实验室以前已经建立了肠道微生物组,是阿片类药物使用的各种副作用的驱动力,包括镇痛耐受性和躯体戒断症状。因此,我们假设肠道微生物组有助于长期戒断过程中焦虑样行为的发展。在这项研究中,我们首先建立了一种旷虫戒断的小鼠模型,其特征在于焦虑样行为和肠道微生物营养不良。接下来,我们使用粪便微生物群移植(FMT)表明,仅肠道营养不良就足以诱导焦虑样行为。我们进一步证明吗啡戒断期间的益生菌治疗会减轻焦虑样行为的发作,突出其治疗潜力。最后,我们检查了用益生菌治疗的吗啡 - 韦斯特拉的小鼠杏仁核中的转录变化,以探索肠道轴介导类似焦虑行为的机制。我们的结果支持使用益生菌作为一种有希望的治疗策略,以防止阿片类药物戒断期间肠道营养不良和相关的焦虑,这可能对改善阿片类药物恢复计划的治疗结果有潜在的影响。关键词阿片类药物提取,焦虑,肠脑轴,杏仁核,益生菌,5-羟色胺
慢性压力对心理健康的影响
I. i ntroduction慢性应激是由持续压力源引起的生理和心理压力状态的长期状态。与急性压力不同,急性应激在短时间内通过提高机敏性和性能可能是有益的,慢性压力会导致大脑的连续压力,从而导致长期功能障碍。这种长时间暴露于压力激素,尤其是皮质醇,有助于大脑的结构和功能变化,从而影响认知,情绪调节和整体心理健康。由于调节认知和情感功能的神经元网络和神经递质网络,人脑特别容易受到慢性压力的影响。研究表明,慢性应激会导致神经变性,突触功能障碍和神经发生受损。海马是一个对学习和记忆至关重要的大脑区域,非常容易受到压力引起的损害。慢性应激已显示可减少海马体积,损害记忆巩固并增加对神经退行性疾病(例如阿尔茨海默氏病)的敏感性。同样,在慢性应激条件下,杏仁核在情绪调节和威胁检测中起着至关重要的作用。增加的杏仁核活性与焦虑,恐惧反应和情绪不稳定有关,这导致焦虑症和抑郁症的发作。此外,慢性压力对前额叶皮层产生负面影响,前额叶皮层是负责执行功能的区域,例如决策,冲动控制和认知灵活性。研究表明,长时间的压力暴露会导致前额叶皮层萎缩,从而导致认知功能受损和情绪调节不良。
使用MRI脑图的进行性核上麻痹综合征的分阶段
人类寿命的大脑图表,以在正常衰老和各种神经系统疾病中构建脑解剖结构的动态模型。他们提供了新的可能性来量化从临床前阶段到死亡的神经解剖学变化,那里没有longi tudinal MRI数据。在这项研究中,我们使用大脑图来对脑萎缩的进展进行进行性超核麻痹 - 瑞奇综合征。 我们组合了多个数据集(n = 8170个涵盖整个寿命的健康受试者的质量控制的MRI,以及从四个重复的tauopathy神经疗法的核定型起始(4Rttni)to to to to to to to to contrapice to to to contrapice to to to to to to to to n = 62 MRI的核酸内核(4rtni)的核能效率和健康的效率象征性象征性象征性象征性象征性象征性象征性象征性象征性象征性象征性象征性的效率为麻痹 - 瑞典综合症大脑结构。 然后,我们在时间和空间中映射了健康和进行性核上麻痹 - 瑞典邦综合征图表之间的顺序差异。 我们发现了萎缩进展的六个主要阶段:(i)ven tral diencephalon(包括丘脑下核,底胺和红色核),(ii)Pallidum,(iii)脑干,纹状体,纹状体,纹状体和杏仁核,(IV)丘脑,(IV)thalamus,(v)thalamus,(v)lobe和(VI)。 随着时间的流逝,具有最严重萎缩的三个结构是丘脑,其次是钯和脑干。 这些结果与进步性上核瘫痪 - 里希尔森综合症的陶氏病进展的神经病理学分期相匹配,该病理应该在pallido-nigro-luysian系统中开始,并通过纹状体和杏仁核向Cerebral cortral cortex和Caudess和Caudsemton和Caudsemth the Pallido-Nigro-luysian系统开始传播。在这项研究中,我们使用大脑图来对脑萎缩的进展进行进行性超核麻痹 - 瑞奇综合征。我们组合了多个数据集(n = 8170个涵盖整个寿命的健康受试者的质量控制的MRI,以及从四个重复的tauopathy神经疗法的核定型起始(4Rttni)to to to to to to to to contrapice to to to contrapice to to to to to to to to n = 62 MRI的核酸内核(4rtni)的核能效率和健康的效率象征性象征性象征性象征性象征性象征性象征性象征性象征性象征性象征性象征性的效率为麻痹 - 瑞典综合症大脑结构。然后,我们在时间和空间中映射了健康和进行性核上麻痹 - 瑞典邦综合征图表之间的顺序差异。我们发现了萎缩进展的六个主要阶段:(i)ven tral diencephalon(包括丘脑下核,底胺和红色核),(ii)Pallidum,(iii)脑干,纹状体,纹状体,纹状体和杏仁核,(IV)丘脑,(IV)thalamus,(v)thalamus,(v)lobe和(VI)。随着时间的流逝,具有最严重萎缩的三个结构是丘脑,其次是钯和脑干。这些结果与进步性上核瘫痪 - 里希尔森综合症的陶氏病进展的神经病理学分期相匹配,该病理应该在pallido-nigro-luysian系统中开始,并通过纹状体和杏仁核向Cerebral cortral cortex和Caudess和Caudsemton和Caudsemth the Pallido-Nigro-luysian系统开始传播。这项研究支持在人类寿命中使用大脑图表来研究神经退行性疾病的进展,尤其是在没有特定的生物标志物的情况下,如PSP中。
化学合成的psilocybin和迷幻蘑菇提取物对小鼠脑中分子和代谢特征的影响
psilocybin是一种天然发生的色氨酸生物碱前药,目前正在研究用于治疗一系列精神疾病。临床前报告表明,含psilocybin的蘑菇提取物或“全光谱”(迷幻)蘑菇提取物(PME)的生物学作用可能与化学合成的psilocybin(PSIL)的生物学作用可能不同。我们将PME与PSIL的影响对雄性C57BL/6J小鼠中的神经可塑性相关的突触蛋白和额叶皮层代谢组纤维的影响,神经可塑性相关的突触蛋白和额叶皮层代谢组纤维的影响。HTR测量在20分钟内显示出PSIL和PME的相似作用。脑标本(额叶皮层,海马,杏仁核,纹状体)使用蛋白质印迹分析突触蛋白,GAP43,PSD95,Synaptophysin和sv2a。这些蛋白质可以用作突触可塑性的指标。治疗三天后,突触蛋白的增加最少。11天后,额叶皮层中的PSIL和PME显着增加了GAP43(分别为p = 0.019; p = 0.039)和海马(P = 0.015; p = 0.027; p = 0.027)和突触possinpocyin and Synaptophysin在海马中(p = 0.041; p = 0.041; p = 0.05)和am amy; p = 0.03(p = 0.03)(p = 0.03);psil在杏仁核中增加了SV2A(p = 0.036),并且PME在海马中这样做(p = 0.014)。在纹状体中,仅PME增加突触素(P = 0.023)。分别分析这些大脑区域对PSD95的PSIL或PME对PSD95没有显着影响。与氧化应激和能量产生途径相关的嘌呤鸟嘌呤,甲黄嘌呤和肌苷显示出从车辆到PSIL再到PME的逐渐下降。的嵌套方差分析(ANOVA)显示,在所有大脑区域中,四种蛋白质中的每一种都显着增加,以进行PME和媒介物控制,而仅在海马和杏仁核中观察到显着的PSIL效应,并且仅在Hippocampus和Amygdala中观察到,并且仅限于PSD95和SV2A。利用毛细管电泳的非靶向极性代谢组学 - 傅立叶变换质谱法(CE-FEFTM)进行了前额叶皮层的代谢组学分析,并在PME和媒介物组之间显示出差异代谢分离。总而言之,我们的突触蛋白发现表明,PME对突触可塑性具有比PSIL更有效,更长时间的作用。我们的代谢组学数据支持从惰性车辆通过化学psilocybin到PME的梯度进一步支持差异效应。需要进一步的研究来确认和扩展这些发现,并确定与单独使用psilocybin相比,可能导致PME效应增强的分子。