XiaoMi-AI文件搜索系统
World File Search System新型三重抗生素糊剂对主要口腔病原体的抗菌效果:
摘要 乳牙的慢性感染,特别是那些涉及根尖周围病变的感染,对儿童牙髓病学构成了重大挑战。由于这些感染的根管系统复杂且具有多种微生物的特性,有效的抗菌治疗至关重要。三联抗生素糊剂 (TAP) 结合了甲硝唑、环丙沙星和米诺环素,在感染根管的消毒方面表现出良好的前景。然而,其对一系列口腔病原体的抗菌效果需要进一步研究。这项体外研究评估了 TAP 对五种口腔病原体的抗菌效果:粪肠球菌 (ATCC 35550)、变形链球菌 (ATCC 25175)、金黄色葡萄球菌 (ATCC 12598)、乳酸杆菌属 (ATCC 4356) 和白色念珠菌 (ATCC 10231)。 TAP 被制备成三种浓度(25 μg/mL、50 μg/mL 和 100 μg/mL),并使用琼脂孔扩散法进行测试。在 37°C 下孵育 24 小时后测量抑菌圈直径。研究发现,TAP 对所有测试的微生物都表现出显著的抗菌活性。在 100% 浓度的 TAP 下观察到最高的抑制区。粪肠球菌显示出最大的抑制区(44.40 ± 0.89 毫米),其次是金黄色葡萄球菌(48.87 ± 0.43 毫米)。虽然 50% 浓度的 TAP 也表现出显著的抗菌活性,但对于大多数生物体来说,50% 和 100% 浓度之间没有统计学上的显著差异。统计分析表明,两种浓度的 TAP 对粪肠球菌、变形链球菌、金黄色葡萄球菌、白色念珠菌和乳酸杆菌均有效。三重抗生素糊剂对主要口腔病原体(包括粪肠球菌和金黄色葡萄球菌等生物膜形成细菌)表现出强大的抗菌效果。虽然 100% 浓度显示出最显著的效果,但 50% 浓度也表现出显著的抗菌活性,这表明较低浓度在临床应用中同样有效。需要进一步的临床研究来证实 TAP 在治疗儿科患者慢性牙髓感染方面的潜力。
r e v i w uganda的糖尿病足溃疡微生物景观的系统评价
背景:糖尿病在全球范围内日益严重。管理不良的糖尿病可能导致糖尿病足溃疡(DFU),这可能成为慢性感染的来源,称为糖尿病足感染。乌干达糖尿病的日益趋势表明,糖尿病足溃疡的潜力可能最终被感染,并且随之而来的是对糖尿病患者生活质量的影响。本综述评估了乌干达DFU的微生物多样性,旨在指导治疗和识别研究差距。摘要的主体:我们在乌干达进行了PubMed,Scopus和Embase搜索了在乌干达进行的研究,这些研究报告了从糖尿病足溃疡中分离出微生物的研究。遵循用于系统评价和荟萃分析(PRISMA)的首选报告项目,我们包括了两项合格的研究,这些研究报告了使用拭子样品和常规培养方法报道了122种细菌分离的细菌。重要的分离株包括世界卫生组织的优先病原体,包括:肠杆菌,金黄色葡萄球菌,肺炎克雷伯氏菌和肺炎杆菌。耐甲氧西林金黄色葡萄球菌(MRSA)占葡萄球菌种的33.3%,所有细菌分离株的26%,而长期谱β-内酰胺酶产生埃斯切里希菌大肠杆菌和klebsiella specie占总体微生物隔离的14.29%。大多数细菌表现出对丙霉素,万古霉素,环丙沙星和克林霉素的敏感性,但注意到对共瑞唑唑和氨苄西林的耐药性。关键字:糖尿病足溃疡,脚感染,乌干达,伤口细菌,脚并发症简短的结论:我们得出结论,乌干达DFU的微生物学数据很少;但是,该国DFU的生物负担与世界其他地区的生物负担相似,MRSA对抗生素疗法构成了挑战。因此,继续使用拭子样品以及常规培养和灵敏度方法可能会限制其他重要分离物的隔离,鉴定和表现。我们建议对细菌分离株进行表征,以更好地了解其遗传构成,并制定用于管理糖尿病足感染的国家指南。
人畜共患病 炭疽病感染的潜在治疗方法
摘要 炭疽病是由炭疽杆菌引起的,对人类和动物的健康构成重大威胁。炭疽病需要彻底而快速的治疗计划,因为它能够通过不同的方式传播,例如吸入、食用受污染的食物或直接接触皮肤。主要方法是使用环丙沙星、左氧氟沙星和强力霉素等抗生素来消灭细菌。抗生素治疗的时间长短取决于炭疽病的类型,吸入性炭疽病通常需要更长的疗程。除了抗生素之外,抗毒素对于最大限度地减少炭疽毒素的有害影响至关重要。炭疽免疫球蛋白 (AIG) 与抗生素结合使用时,可使毒素失活,最大限度地减少组织损伤并提高治疗的整体效果。疫苗接种在提供预防和治疗效益方面起着至关重要的作用。建议定期为有接触炭疽风险的人接种疫苗。如果有人接触过,他们可以开始服用炭疽疫苗和抗生素来预防疾病的发展。此外,炭疽感染患者将接受支持性护理,如止痛、帮助呼吸和输液以控制症状和并发症。隔离感染者并实施严格的感染控制措施对于控制疾病的传播至关重要。必须通过临床和实验室评估密切监测患者对治疗的反应,以便对治疗方法进行必要的调整。及时发现和治疗疑似炭疽病例至关重要,这凸显了及时医疗干预的重要性。持续的护理可确保感染得到完全解决,从而减少出现任何其他问题的机会。随着传染病的变化,继续研究治疗和预防炭疽的新方法至关重要,以提高我们对抗炭疽的能力并保护公众健康。关键词:炭疽;炭疽芽孢杆菌;抗生素;抗毒素;疫苗接种 引文 Altaf S、Khan S、Iqbal T、Farooq MA 和 Muzaffar H,2023 年。炭疽感染的潜在治疗方法。在:Aguilar-Marcelino L、Zafar MA、Abbas RZ 和 Khan A(编辑),人畜共患病,Unique Scientific Publishers,巴基斯坦费萨拉巴德,第 3 卷:576-588。https://doi.org/10.47278/book.zoon/2023.125 章节历史 收到日期:2023 年 5 月 14 日 修订日期:2023 年 6 月 20 日 接受日期:2023 年 7 月 15 日
4 cfu/g,最低为 1.9 x 10 -4 cfu/g,而平均值为 4.09 x 10 4。使用标准微生物组对分离物进行鉴定和表征
4 cfu/g,最低为 1.9 x 10 -4 cfu/g,而平均值为 4.09 x 10 4。使用标准微生物程序对分离物进行鉴定和表征。最常见的细菌是金黄色葡萄球菌(26%),霍乱弧菌(22%),志贺氏菌(13%),而最少的是沙门氏菌(9%)。革兰氏阳性菌(金黄色葡萄球菌)对环丙沙星(100%)和氧氟沙星(100%)高度敏感,但对氨苄西林(100%)高度耐药。革兰氏阴性病原体(大肠杆菌、霍乱弧菌和志贺氏菌)对培氧氟沙星(100%)和氧氟沙星(100%)高度敏感。它还显示出对阿莫西林(100%)、氯霉素(100%)、庆大霉素(100%)、呋喃妥因(100%)的高耐药性。本研究中抗生素耐药菌的高流行率是一个严重问题,因为大肠杆菌、金黄色葡萄球菌、沙门氏菌、霍乱弧菌和志贺氏菌的耐药模式会对人类健康产生影响,从而建议鱼类加工商和销售商应改善处理卫生状况,消费者也应妥善处理鱼类,以尽量减少可能的健康危害。DOI:https://dx.doi.org/10.4314/jasem.v28i12.26 许可证:CC-BY-4.0 开放获取政策:JASEM 发布的所有文章均为开放获取文章,任何人都可以免费下载、复制、重新分发、转发、翻译和阅读。版权政策:© 2024。作者保留版权并授予 JASEM 首次出版权。本文的任何部分均可未经许可重复使用,但必须引用原始文章。引用本文为:NWUZO,AC;IGWE,PC;OKPOKWU,UA;ANIOKETE,UC;NOMEH,OL;NWOJIJI,EC;CHUKWUEMEKA–ODI,LO;UGWU,J;NWADUM,EF;AGBOM,JN;NWOKPORO,NR(2024)。对尼日利亚埃邦伊州阿巴卡利基水产养殖鱼细菌污染及其公共卫生影响的评估。应用科学环境管理杂志 28 (12) 4153-4160 日期:收到日期:2024 年 9 月 18 日;修订日期:2024 年 10 月 20 日;接受日期:2024 年 11 月 5 日;出版日期:2024 年 11 月 15 日 关键词=抗生素耐药性;公共卫生影响;水产养殖;细菌学;人类 在过去的 35 年里,尼日利亚的水产养殖产量每年增长 12%,从 1980 年的 6,000 吨增加到 2016 年的约 307,000 吨(Worldfish,2018 年)。尼日利亚是最大的鱼类养殖国
识别和隔离微生物的负责...
摘要:这项研究研究了与新鲜西红柿恶化相关的细菌和真菌(Lycopersicum esculentum)。从卡杜纳(Kaduna)Ungwan Rimi地区的四(4)个不同的零售店获得了16(16)个番茄样品。使用标准方案确定所选番茄样品的近端组成。使用浇注板法用于与番茄样品分离细菌和真菌。使用磁盘扩散技术确定了针对细菌和真菌分离株的选定抗生素和抗真菌药物的抗生素图。The results of proximate composition showed that sample A had a moisture content of 94.10 %, 0.74% of ash, 0.97 % of crude protein, 0.66 % of crude fat, 1.10 % crude fiber, and 2.43 % of carbohydrate while sample B showed similar percentage composition of 93.89 % of moisture content, 0.86 % of ash, 1.0 % of crude protein, 0.69 % of crude fat, 1.34%的粗纤维和2.22%的碳水化合物。分离和鉴定的细菌是金黄色葡萄球菌,大肠杆菌和沙门氏菌。最普遍的细菌分离株是金黄色葡萄球菌,其50%,而沙门氏菌和大肠杆菌的分离菌则分别为25%。真菌分离株是尼日尔曲霉和曲霉菌的青霉素。尼日尔曲霉最为普遍,而青霉人SP的占30.8%,而曲霉菌的患病率最少为15.4%。在不同浓度的抗生素下,大肠杆菌对庆大霉素和链霉素具有抗性,对氯霉素,Spafloxacin,ciproflofloxacin,amoxycillincillin,peffloxacin,peffloxacin,tarvid和agenmentine敏感。沙门氏菌SP的抗菌易感性表明,它耐庆大霉素,对链霉素和粘膜链霉素的敏感性适中,对氯霉素,替福洛沙星,ciprofloflofloxin,ciproflofloxin,Amoxycillin,amoxycillin,pefloboxacin,pefloxacin,tarvid和Audmentine consives Adimenty consivessine spectimity敏感。金黄色葡萄球菌对rocephin,Zinacef和链霉菌素具有抗性,对氨木酸和阿莫西林敏感,并且对斑岩蛋白,环丙沙星,源自源环霉素,pefloxacin和Erythromycin敏感。抗真菌敏感性在其针对测试真菌分离株的有效性方面显示出不同浓度的变化。这些真菌的存在以及能够引起食物中毒的细菌分离株引起了人们对公共卫生风险的关注,这些风险可能与消耗变质的新鲜西红柿有关。用清洁或氯化水进行适当的处理,运输和彻底洗涤,将降低与细菌和真菌物种相关的番茄变质的风险。
喀麦隆(中非)城市地区地下和雨水中分离出的某些芽孢杆菌菌株的抗生素敏感性以及季节变化的潜在影响
Morelle Raïsa Djiaala Tagne、Mireille Ebiane Nougang、Edith Brunelle Mouafo Tamnou、Awawou Manouore Njoya、Pierrette Ngo Bahebeck、Samuel Davy Baleng、Paul Aain Nana、Yves Yogne Poutoum、Genevieve Bricheux、Claire Stéphane Metsopkeng、Télesphore Sime-Ngando 和 Moïse Nola DOI: https://doi.org/10.22271/micro.2023.v4.i1b.72 摘要 这项研究评估了在雅温得(喀麦隆)的井和雨水样本中分离的蜡状芽孢杆菌、苏云金芽孢杆菌和枯草芽孢杆菌菌株的抗生素敏感性。在长旱季 (LDS)、短旱季 (SDS)、长雨季 (LRS) 和短雨季 (SRS) 期间每月收集水井水样,对于雨水则在 LRS 和 SRS 期间收集。考虑的抗生素包括亚胺培南、阿米卡星、庆大霉素、环丙沙星、氧氟沙星、磺胺甲唑和四环素。对于来自地下水的菌株,对于苏云金芽孢杆菌,抗生素抑制直径从 9.13 毫米(SDS 期间的磺胺甲唑)到 32.78 毫米(LDS 期间的亚胺培南),对于蜡状芽孢杆菌,抗生素抑制直径从 8.2 毫米(SDS 期间的磺胺甲唑)到 35.25 毫米(LDS 期间的亚胺培南)不等,对于枯草芽孢杆菌,抗生素抑制直径从 5.05 毫米(LRS 期间的氧氟沙星)到 29.25 毫米(LDS 期间的亚胺培南)。雨水中的芽孢杆菌直径从 4.55 mm(LRS 期间使用磺胺甲唑)到 25.65mm(LRS 期间使用亚胺培南),蜡状芽孢杆菌从 2.13 mm(LRS 期间使用亚胺培南)到 20.05mm(SRS 期间使用亚胺培南),枯草芽孢杆菌从 5.03 mm(SRS 期间使用庆大霉素)到 25.15mm(SRS 期间使用四环素)。LRS 期间分离出的芽孢杆菌菌株对大多数抗生素具有多重耐药性。大多数抗生素的抑菌直径在不同季节之间存在显著差异(p<0.05)。关键词:抗生素敏感性,芽孢杆菌菌株,地下水和雨水,抑菌直径变化 1. 引言 不同国家的水消耗量差异很大。这取决于其发展、人口和资源本身。当水被污染时,水会成为许多疾病的主要传播媒介之一,而这些疾病是导致人类或动物大规模流行病的原因。污染源包括河流、水体、咸水以及雨水、露水、雪和极地冰。每种环境中的水都可能被化学物质和微生物污染,包括原生动物、病毒和细菌 [1] 。水环境中有各种细菌科。这些微生物具有各种特性。通常用于识别细菌微生物的一些特性是革兰氏染色细胞壁和产孢特性。芽孢杆菌属细菌被称为革兰氏阳性菌和产孢菌。它们存在于空气、水中或土壤中 [2] 。对于人类来说,一些芽孢杆菌种是病原体或机会性病原体,而另一些只是共生菌。然而,细菌的共生特性取决于其环境中的几个因素 [3] 。除了食物中毒外,这些细菌会引起局部和全身感染,有时会导致患者死亡 [4, 5] 。多年来,人们也认识到生物颗粒对大气过程的潜在相关性 [6, 7] 。空气中的生物颗粒作为一个整体也被称为生物气溶胶。它们可以包括细菌细胞和细胞碎片、真菌孢子和真菌
抗生素药物分类PDF
抗菌剂,也称为化学疗法,旨在通过抑制或杀死感染微生物,同时最大程度地减少对宿主的伤害来对抗感染。抗生素是一种由微生物产生的一种抗生素,可有选择地抑制或杀死低浓度的其他微生物的生长或杀死其他微生物。该定义不包括较高生物体产生的物质。可以根据其化学结构,作用机理,靶向生物类型,活性谱和来源分类。某些抗菌作用直接在细菌细胞壁上发挥作用,或者必须通过它,然后才能在细胞内水平破坏细菌代谢。类红霉素这样的抗生素可以靶向革兰氏阳性细菌,但对革兰氏阴性菌的含量无效,除非在极少数情况下。大多数细菌基于实验室中使用的染色技术属于这两类。革兰氏阴性物种,即使用最少的营养迅速繁殖,并且在医院和革兰氏阳性对应物的同时也发现。革兰氏阳性生物的例子包括金黄色葡萄球菌,化脓性链球菌和肺炎链球菌,而革兰氏阴性菌的葡萄球菌包括大肠杆菌,Neisseria Gonorrhea和Klebsiella。厌氧菌可在没有游离氧气的情况下生存,但需要特殊的条件才能在实验室中生长。但是,在某些情况下,它们会引起严重的感染。使用抗菌药物的问题之一是毒性,在注射部位或影响各种器官的全身毒性上可能表现为局部刺激。一些常见的分类包括: *磺酰胺和相关药物 *奎诺酮,如环丙沙星 *β-乳糖抗生素,例如青霉素和头孢菌素 * tetracyclines * tetracyclines,包括强力霉素 *氨基糖苷,包括氨基糖苷,包括链霉菌素和雌雄同体,包括Er雌激素 * Macrolosiv,酸毛霉素,酸糖尿病,酸糖苷,酸糖苷,酸糖尿病红唑和氯咪唑抗生素也可以根据其作用机制进行分类: *抑制细胞壁合成,例如青霉素和头孢菌素 *抑制蛋白质合成,包括四环素和红霉素在内*也可以根据它们主要针对的生物类型来分类: *抗菌剂,包括青霉素和氨基糖苷 *抗真菌药物,例如抗菌剂 *抗真菌药物,例如ZIDOVUDINE和ACYCLOVIR抗菌抗菌剂,也可以根据其靶向: *抗菌剂进行分类。抗吡喹剂,例如氯喹和甲硝唑 *抗智能剂,例如甲苯二唑和丙ama剂,也可以根据其活性谱进行分类: *狭窄的 - 谱抗微生物剂,例如青霉素g和erythromycin and themimictram and themicramic and themicriame and themicriame andimicrials,themicriame themiccl themiccl tatect themiccl themicrials themiCrimicClateCcltic themiCrimicClateCclticramic tatect the最后,抗菌物质通过迅速杀死细菌或阻止其复制来起作用。氯霉素会导致骨髓抑郁症,而四环素可能会损害肝脏和肾脏。抗菌剂还会引发无法预测且不与剂量有关的超敏反应。这些反应从轻度皮疹到严重的过敏性休克。它们可能是由青霉素,头孢菌素,磺酰胺或氟喹诺酮引起的。另一个主要问题是耐药性,随着时间的流逝,微生物对抗菌药物产生无反应性。这可能是由于某些微生物中的自然耐药性或由于这些药物长时间使用而获得的耐药性。超级感染是指抗菌治疗后新感染的发展。是因为人体的正常微生物菌群发生了改变,导致失衡会导致致病生物更容易确定自己。的例子包括念珠菌过度生长,这通常与四环素和氯霉素等广谱抗生素有关。为了最大程度地减少超级感染,尽可能使用特定的抗菌药物至关重要,避免使用这些药物治疗微不足道的感染,而不是不必要地延长抗菌治疗。使用抗菌剂会导致各种问题,例如肠道菌群被破坏时的维生素缺乏。这种破坏可能是由于某些改变肠道平衡的药物的使用可能会导致这种中断。此外,抗菌药物可以掩盖感染,暂时抑制症状,但可能导致后来更严重的结果。例如,将单剂量的青霉素用于淋病,可能会掩盖梅毒或TB,这是由于短期链霉素引起的。磺酰胺是一类较旧的抗菌剂,由于细菌耐药性和不良副作用的发展而被大大替换。这些化合物主要用作抑制抑制剂,抑制各种细菌的生长,包括革兰氏阳性和革兰氏阴性生物。其作用背后的机制涉及细菌干扰叶酸的合成,而人类可以从饮食中利用预先形成的叶酸。磺酰胺以不同的形式可用,每种都具有其独特的特征。可以根据其作用方式将它们广泛分为三个主要组:(1)抑制细胞壁合成,包括甲基核苷和奥沙西林等青霉素; (2)抑制蛋白质合成; (3)抑制细菌核酸合成。
闭角型青光眼的生物特征发现 光学... - CBO
Zypred® 加替沙星 0.3%,醋酸泼尼松龙 1%。适应症:ZYPRED® 适用于治疗眼部感染以及治疗和预防接受眼科手术的患者的眼部感染和炎症。禁忌症 - ZYPRED® 禁用于对加替沙星、其他喹诺酮类药物或该产品的任何其他成分有过敏史的患者,以及急性化脓性眼部感染、急性浅表单纯疱疹(树突状角膜炎)、牛痘、水痘和许多其他角膜和结膜病毒性疾病、眼结核和眼部真菌性疾病。警告和注意事项 - ZYPRED® 适合眼部局部使用。据报道,长期使用局部眼用皮质类固醇后会形成后囊下白内障。有单纯疱疹性角膜炎病史的患者应谨慎治疗。对于导致角膜变薄的疾病,使用局部类固醇可能会导致穿孔。对于化脓性眼部感染,局部使用类固醇可能会掩盖或加重现有感染。在存在单纯疱疹的情况下使用类固醇药物需要谨慎,并且必须经常用裂隙灯显微镜检查。由于长期使用外用类固醇有真菌感染的报道,因此当已经使用或正在使用类固醇时,任何角膜溃疡都应怀疑真菌入侵。使用局部皮质类固醇可能会导致某些患者眼压升高,从而导致视神经损伤和视野衰竭。建议经常监测眼压。与其他抗感染药一样,长期使用加替沙星可能会导致包括真菌在内的非敏感微生物的重复感染。如果发生重复感染,必须停止使用并采取替代治疗。只要临床判断表明,患者就应该接受图像放大设备的检查,例如裂隙灯、生物显微镜,如果合适的话,还可以进行荧光素染色。应告知患者,即使单次给药也会发生过敏反应,一旦出现皮疹或过敏反应迹象,应立即停止治疗并联系医生。怀孕和哺乳期:怀孕风险类别:C(FDA - 美国)。使用前摇匀瓶子。注册在对大鼠或兔子进行的研究中,口服给予加替沙星,剂量高达 50 mg/kg/天(约为眼科最大推荐剂量的 1,000 倍),未观察到致畸作用。尚未对孕妇进行过泼尼松龙的对照研究。然而实验研究表明,皮质类固醇一般对小鼠有致畸作用,反复局部眼部应用皮质类固醇治疗的动物腭裂发生率增加。由于尚未对妊娠期妇女进行对照研究,因此仅当对母亲的潜在益处大于对胎儿的潜在风险时,才应在妊娠期使用 ZYPRED®(加替沙星和泼尼松龙)。未经医生或牙医建议,怀孕期间不应使用此药。加替沙星会排泄至大鼠的乳汁中,但尚不清楚该物质是否会排泄至人乳汁中。目前尚不清楚局部眼部应用皮质类固醇是否会导致全身吸收足够量的皮质类固醇在人乳中被检测到。因此,建议在哺乳期妇女使用 ZYPRED® 时要谨慎。老年患者 老年患者与其他年龄段的患者之间在疗效和安全性上没有差异,因此对于老年人的使用没有特别的建议。儿科患者 ZYPRED® 对儿科患者的安全性和有效性尚未确定。肾功能或肝功能不全的患者:ZYPRED® 尚未对肾功能或肝功能不全的患者进行研究,因此对这些患者应谨慎使用。糖尿病患者:进行了一项开放、比较、前瞻性、纵向研究,评估了0.3%加替沙星+1.0%醋酸泼尼松龙固定组合在糖尿病患者中的疗效和安全性。在研究结束时,使用加替沙星 + 泼尼松龙的固定组合可使细菌生长减少 27.3%,而使用环丙沙星 + 泼尼松龙则可使细菌生长减少 22.7%。目前尚未发现局部眼用泼尼松龙与其他物质之间存在相互作用。剂量及使用方法 - 悬浮液已准备好使用。该药物用于局部眼部使用。请勿将瓶尖接触眼睛、手指或任何其他表面,以免污染瓶子和眼药水。答案。药物相互作用 - 没有对 ZYPRED® 进行具体的药物相互作用研究,但是,全身给药一些喹诺酮类药物会增加茶碱的血浆浓度,干扰咖啡因代谢并增加口服抗凝剂华法林及其衍生物的作用。 ,并且与同时接受环孢菌素全身治疗的患者血清肌酐短暂升高有关。治疗眼部感染的常用剂量是在受影响的眼睛上滴 1 滴,每天四次,最多 7 天。眼科手术后预防和治疗感染和炎症的常用剂量是在受影响的眼睛上涂抹 1 滴,每天 4 次,最多 15 天,但是,由于感染情况不同。 ,治疗时间可能会根据医疗判断进行修改。不良反应 - ZYPRED®(加替沙星和泼尼松龙)最常见的眼部不良反应按发生频率排列为: 非常常见的反应 (>10%):烧灼感、眼刺激、瘙痒和眼痛。常见反应(>1% 和 <10%):视力模糊/模糊、眼睛不适、流泪、异物感、干眼、结膜刺激、角膜炎和乳头性结膜炎。约 1% 至 4% 的研究人群中发生的其他报告反应包括:结膜水肿、结膜出血、干眼、眼部分泌物、眼部刺激、眼部疼痛、眼睑水肿、头痛、眼部发红、视力下降和变化在味道上。由于产品成分中存在泼尼松龙,可能会出现眼睑强烈烧灼感、剧烈瘙痒、肿胀或发红。在使用 ZYPRED® 进行的临床研究中,没有研究对象因出现不良反应而放弃治疗。本产品是一种新药,尽管研究表明疗效和安全性可接受,但即使指示和使用正确,也可能会发生不可预测或未知的不良事件。在这种情况下,请通过健康监测通知系统 -NOTIVISA(可在 http://www.anvisa.gov.br/hotsite/notivisa/index.htm 上获取)或向州健康监测或市政府通报不良事件。 ” 10.如果意外或故意摄入,建议饮用大量液体以稀释。如果中毒,如果您需要进一步指导,请致电 0800 722 6001。ANVISA/MS - 1.0147.0175 农场。:医生Flávia Regina Pegorer CRF-SP n° 18.150。药物过量:使用 ZYPRED®(加替沙星和泼尼松龙)不太可能发生药物过量,因为 6 毫升瓶 ZYPRED® 眼用混悬液中加替沙星和泼尼松龙的含量分别显着低于推荐的每日口服剂量。给予加替沙星和泼尼松龙。Allergan Produtos Farmacêuticos LTDA .Av。瓜鲁柳斯, 3272 - CEP 07030-000 瓜鲁柳斯 - SP。CNPJ 43.426.626/0009-24 巴西工业 - ® 注册商标。根据医疗处方销售。
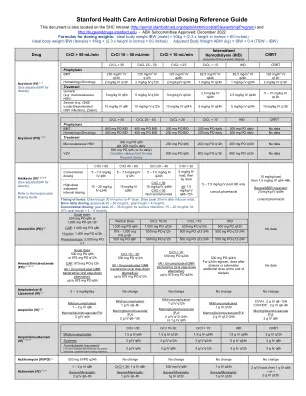
斯坦福医疗保健抗菌药物剂量参考指南
参考文献: 1. Lexicomp Online。访问日期:2017 年 4 月 9 日。http://online.lexi.com 2. MICROMEDEX®。访问日期:2017 年 4 月 9 日。http://www.micromedexsolutions.com.laneproxy.stanford.edu/micromedex2/librarian 3. Heintz BH、Matzke GR、Dager WE。接受持续性肾脏替代疗法或间歇性血液透析的重症成人患者的抗菌剂量概念和建议。Pharmacother J Hum Pharmacol Drug Ther。2009;29。doi:10.1592/phco.29.5.562 4. Trotman RL、Williamson JC、Shoemaker DM、Salzer WL。接受持续性肾脏替代疗法的重症成人患者的抗生素剂量。Clin Infect Dis。 2005;41(8):1159-1166。doi:10.1086/444500 5. Aronoff G、Bennett W、Berns J 等人。肾衰竭中的药物处方。第 5 版。美国内科医师学会;2007 年。 6. Turner RB、Cumpston A、Sweet M 等人。肥胖患者阿昔洛韦药代动力学的前瞻性对照研究。抗微生物药物化疗。2016;60。doi:10.1128/aac.02010-15 7. Tomblyn M、Chiller T、Einsele H 等人。造血细胞移植接受者感染并发症预防指南:全球视角。Biol Blood Marrow Transplant。 2009;15(10):1143-1238。doi:10.1016/j.bbmt.2009.06.019 8. Roger C、Wallis SC、Muller L 等人。肾脏替代方式对接受持续性肾脏替代治疗的危重患者阿米卡星群体药代动力学的影响。抗微生物剂化疗。2016;60。doi:10.1128/aac.00828-16 9. Taccone FS、Backer D de、Laterre PF 等人。接受持续性肾脏替代治疗的脓毒症患者负荷剂量阿米卡星的药代动力学。国际抗微生物剂杂志。2011;37。 doi:10.1016/j.ijantimicag.2011.01.026 10. Mora Lopez L、Serra Pla S、Serra-Aracil X、Ballesteros E、Navarro S。改良 Neff 分类法在无并发症憩室炎患者中的应用。结直肠疾病。2013;15(11):1442-1447。doi:10.1111/codi.12449 11. Biondo S、Golda T、Kreisler E 等。无并发症憩室炎的门诊与住院治疗:一项前瞻性、多中心随机临床试验(DIVER 试验)。外科年鉴。2014;259(1):38-44。 doi:10.1097/SLA.0b013e3182965a11 12. Mora-López L、Ruiz-Edo N、Estrada-Ferrer O 等人。非抗生素门诊治疗轻度急性憩室炎的疗效和安全性(DINAMO 研究):一项多中心、随机、开放标签、非劣效性试验。Ann Surg。2021;274(5):e435。doi:10.1097/SLA.0000000000005031 13. Tamma PD、Aitken SL、Bonomo RA、Mathers AJ、van Duin D、Clancy CJ。美国传染病学会关于治疗产 AmpC β-内酰胺酶肠杆菌、耐碳青霉烯类鲍曼不动杆菌和嗜麦芽窄食单胞菌感染的指导。临床传染病学杂志。2022;74(12):2089-2114。doi:10.1093/cid/ciab1013 14. Gerig JS、Bolton ND、Swabb EA、Scheld WM、Bolton WK。血液透析和腹膜透析对氨曲南药代动力学的影响。Kidney Int 。1984;26。doi:10.1038/ki.1984.174 15. Gustot T、ter Heine R、Brauns E、Cotton F、Jacobs F、Brüggemann RJ。对于 Child–Pugh B 或 C 级肝硬化患者,无需调整卡泊芬净剂量。J Antimicrob Chemother 。2018;73(9):2493-2496。doi:10.1093/jac/dky189 16. Roger C、Wallis SC、Muller L 等。接受持续性静脉-静脉血液滤过或血液透析滤过的危重患者中卡泊芬净的群体药代动力学。Clin Pharmacokinet 。2017;56(9):1057-1068。 doi:10.1007/s40262-016-0495-z 17. Pappas PG、Kauffman CA、Andes DR 等人。念珠菌病管理临床实践指南:美国传染病学会 2016 年更新。 Clin Infect Dis Off Public Infect Dis Soc Am。 2016;62(4):e1-50。 doi:10.1093/cid/civ933 18. Stryjewski ME、Szczech LA、Benjamin DK 等人。使用万古霉素或第一代头孢菌素治疗患有甲氧西林敏感金黄色葡萄球菌菌血症的血液透析依赖患者。临床感染病。 2007;44。 doi:10.1086/510386 19. Wong G, Briscoe S, McWhinney B 等人。重症患者 β-内酰胺类抗生素治疗药物监测:直接测量未结合药物浓度以实现适当的药物暴露。J Antimicrob Chemother 。2018;73(11):3087-3094。doi:10.1093/jac/dky314 20. Roberts JA, Udy AA, Jarrett P 等人。创伤后重症患者头孢唑林血浆和靶部位皮下组织群体药代动力学和给药模拟。J Antimicrob Chemother 。2015;70(5):1495-1502。 doi:10.1093/jac/dku564 21. Crandon JL、Bulik CC、Kuti JL、Nicolau DP。头孢吡肟在感染铜绿假单胞菌患者中的临床药效学。抗菌药物化疗。2010;54。doi:10.1128/AAC.01183-09 22. Bauer KA、West JE、O'Brien JM、Goff DA。延长输注头孢吡肟可降低感染铜绿假单胞菌患者的死亡率。抗菌药物化疗。2013;57。doi:10.1128/AAC.02365-12 23. Hoff BM、Maker JH、Dager WE、Heintz BH。接受间歇性血液透析、长期间歇性肾脏替代疗法和持续性肾脏替代疗法的重症成人患者的抗生素剂量:最新进展。药物治疗年鉴。2020;54(1):43-55。doi:10.1177/1060028019865873 24. Vidaillac C、Leonard SN、Rybak MJ。头孢洛林在中空纤维模型中对耐甲氧西林金黄色葡萄球菌和异质性万古霉素中间金黄色葡萄球菌的体外活性。抗菌药物化学治疗。2009;53(11):4712-4717。 doi:10.1128/AAC.00636-09 25. Loo AS, Neely M, Anderson EJ, Ghossein C, McLaughlin MM, Scheetz MH. 高通量血液透析中各种头孢他啶给药方案的药效动力学目标实现情况。抗菌药物化疗。2013;57(12):5854-5859. doi:10.1128/AAC.00474-13 26. Wenzler E, Bunnell KL, Bleasdale SC, Benken S, Danziger LH, Rodvold KA.接受持续性静脉静脉血液透析滤过的危重患者头孢他啶-阿维巴坦的药代动力学和透析清除率。抗微生物剂化疗。2017;61(7)。doi:10.1128/AAC.00464-17 27. Soukup P、Faust AC、Edpuganti V、Putnam WC、McKinnell JA。接受持续性静脉静脉血液透析滤过的治疗铜绿假单胞菌肺炎的危重患者稳态头孢他啶-阿维巴坦血清浓度和给药建议。Pharmacother J Hum Pharmacol Drug Ther。2019;39(12):1216-1222。 doi:10.1002/phar.2338 28. Pistolesi V、Morabito S、Di Mario F、Regolisti G、Cantarelli C、Fiaccadori E. 接受肾脏替代治疗的危重患者抗菌药物剂量理解指南。抗菌药物化学治疗。2019;63(8)。doi:10.1128/AAC.00583-19 29. Li L、Li X、Xia Y 等人。持续肾脏替代治疗期间抗菌药物剂量优化建议。Front Pharmacol。2020;11。doi:10.3389/fphar.2020.00786 30. Bremmer DN、Nicolau DP、Burcham P、Chunduri A、Shidham G、Bauer KA。接受连续性肾脏替代治疗的重症成人患者的头孢洛扎/他唑巴坦药代动力学。药物治疗学。2016;36(5):e30-e33。doi:10.1002/phar.1744 31. Oliver WD、Heil EL、Gonzales JP 等人。接受连续性静脉-静脉血液透析滤过的重症患者的头孢洛扎-他唑巴坦药代动力学。抗微生物剂化疗。2016;60。doi:10.1128/aac.02608-15 32. Aguilar G、Ferriols R、Martínez-Castro S 等人。在连续性静脉-静脉血液透析滤过期间优化重症患者的头孢洛扎-他唑巴坦剂量。重症监护。 2019;23。doi:10.1186/s13054-019-2434-5 33. Tamma PD、Aitken SL、Bonomo RA、Mathers AJ、van Duin D、Clancy CJ。美国传染病协会 2022 年产超广谱 β-内酰胺酶肠杆菌科细菌 (ESBL-E)、耐碳青霉烯类肠杆菌科细菌 (CRE) 和难治性耐药铜绿假单胞菌 (DTR-P. aeruginosa) 治疗指南。Clin Infect Dis Off Publ Infect Dis Soc Am。2022;75(2):187-212。doi:10.1093/cid/ciac268 34. Laville M、Mercatello A、Freney J 等人。头孢曲松在血液透析中的药代动力学。Pathol Biol(巴黎)。1987;35(5 Pt 2):719-723。35. Stevens DL、Bisno AL、Chambers HF 等。皮肤和软组织感染诊断和管理实践指南:美国传染病协会 2014 年更新。临床感染性疾病。2014;59。doi:10.1093/cid/ciu296 36. Roger C、Wallis SC、Louart B 等。等剂量持续性静脉-静脉血液滤过和血液透析滤过对危重患者环丙沙星群体药代动力学的影响比较。抗微生物化疗杂志。2016;71(6):1643-1650。 doi:10.1093/jac/dkw043 37. Marbury T、Dowell JA、Seltzer E、Buckwalter M。达巴万星在肾或肝功能不全患者中的药代动力学。临床药理学杂志。 2009;49(4):465-476。 doi:10.1177/0091270008330162 38. Dvorchik BH,Damphousse D. 达托霉素在中度肥胖、病态肥胖和匹配的非肥胖受试者中的药代动力学。临床药理学杂志。2005;45(1):48-56。doi:10.1177/0091270004269562 39. Pai MP、Norenberg JP、Anderson T 等人。病态肥胖对达托霉素单剂量药代动力学的影响。抗微生物剂化疗。2007;51(8):2741-2747。doi:10.1128/AAC.00059-07 40. Haselden M、Leach M、Bohm N. 接受每周三次间歇性血液透析的患者的达托霉素给药策略。药物治疗年鉴。 2013;47(10):1342-1347。doi:10.1177/1060028013503110 41. Patel N、Cardone K、Grabe DW 等。使用药代动力学和药效学原理确定接受标准化每周三次血液透析的患者达托霉素的最佳给药方式。抗微生物剂化疗。2011;55(4):1677-1683。doi:10.1128/AAC.01224-10 42. Falcone M、Russo A、Cassetta MI 等。接受连续性肾脏替代治疗的危重患者血清达托霉素水平。意大利佛罗伦萨化疗杂志。2012;24(5):253-256。 doi:10.1179/1973947812Y.0000000033 43. Preiswerk B、Rudiger A、Fehr J、Corti N。接受持续性肾脏替代治疗的ICU患者中达托霉素每日给药的经验。感染。2013;41(2):553-557。doi:10.1007/s15010-012-0300-3 44. Xu X、Khadzhynov D、Peters H 等。接受持续性肾脏替代治疗的成年患者中达托霉素的群体药代动力学。英国临床药理学杂志。2017;83(3):498-509。 doi:10.1111/bcp.13131 45. Diolez J、Venisse N、Belmouaz S、Bauwens MA、Bridoux F、Beraud G。高剂量达托霉素对感染医疗器械的血液透析患者的初步药代动力学研究。Am J Kidney Dis Off J Natl Kidney Found。2017;70(5):732-734。doi:10.1053/j.ajkd.2017.05.011 46. Geerlings CJC、de Man P、Rietveld AP、Touw DJ、Cohen Tervaert JW。对于慢性血液透析患者来说,每周三次厄他培南的实用给药方案是什么?临床肾脏病学。2013;80(4):312。 doi:10.5414/cn108071 47. Hsaiky LM, Salinitri FD, Wong J 等。间歇性血液透析患者厄他培南的药代动力学和最佳剂量研究。肾脏病学与移植杂志。2019;34(10):1766-1772。doi:10.1093/ndt/gfy166 48. Ueng YF, Wang HJ, Wu SC, Ng YY。每周三次厄他培南治疗方案对血液透析患者实用。抗微生物剂化疗。2019;63(12)。doi:10.1128/AAC.01427-19 49. 耐药结核病:临床医生生存指南,第 3 版 | Curry 国际结核病中心。访问日期:2017 年 4 月 10 日。http://www.currytbcenter.ucsf.edu/products/cover-pages/drug-resistant- tuberculosis-survival-guide-clinicians-3rd-edition 50. Nahid P、Dorman SE、Alipanah N 等。美国胸科学会/疾病控制与预防中心/美国传染病学会官方临床实践指南:药物敏感结核病的治疗。Clin Infect Dis Off Publ Infect Dis Soc Am。2016;63(7):e147-195。doi:10.1093/cid/ciw376 51. Muilwijk EW、Lange DW de、Schouten JA 等人。重症患者氟康唑剂量不理想:是时候重新考虑剂量了。抗微生物药物化疗。2020;64(10)。doi:10.1128/AAC.00984-20 52. Aweeka FT、Jacobson MA、Martin-Munley S 等人。肾脏疾病和血液透析对膦甲酸药代动力学和给药建议的影响。J Acquir Immune Defic Syndr Hum Retrovirology Off Publ Int Retrovirology Assoc。1999;20(4):350-357。53. Jayasekara D、Aweeka FT、Rodriguez R、Kalayjian RC、Humphreys MH、Gambertoglio JG。肾功能不全的 HIV 患者的抗病毒治疗。 J Acquir Immune Defic Syndr 1999 . 1999;21(5):384-395。 54. MacGregor RR、Graziani AL、Weiss R、Grunwald JE、Gambertoglio JG。膦甲酸疗法成功治疗接受血液透析的艾滋病患者巨细胞病毒性视网膜炎:经验性用药和血浆水平监测的原理。J Infect Dis . 1991;164(4):785-787。 55. Nicolau DP、Freeman CD、Belliveau PP、Nightingale CH、Ross JW、Quintiliani R。每日一次氨基糖苷类药物治疗 2,184 名成年患者的经验。抗微生物药物化疗。1995;39(3):650-655。 56. Kuti JL, Dandekar PK, Nightingale CH, Nicolau DP. 使用蒙特卡罗模拟设计美罗培南的优化药效学给药策略。J Clin Pharmacol。2003;43(10):1116-1123。doi:10.1177/0091270003257225 57. Robson R, Buttimore A, Lynn K, Brewster M, Ward P. 奥司他韦混悬液在血液透析和持续性非卧床腹膜透析患者中的药代动力学和耐受性。Nephrol Dial Transplant Off Publ Eur Dial Transpl Assoc - Eur Ren Assoc。2006;21(9):2556-2562。 doi:10.1093/ndt/gfl267 58. Lodise TP, Lomaestro B, Drusano GL。哌拉西林-他唑巴坦治疗铜绿假单胞菌感染:延长输注给药策略的临床意义。Clin Infect Dis Off Publ Infect Dis Soc Am。2007;44(3):357-363。doi:10.1086/510590 59. Patel N, Scheetz MH, Drusano GL, Lodise TP。确定住院患者传统和延长输注哌拉西林-他唑巴坦给药方案的最佳肾脏剂量调整。抗微生物药物化疗。2010;54(1):460-465。 doi:10.1128/AAC.00296-09 60. Sandri AM、Landersdorfer CB、Jacob J 等。重症患者静脉注射多粘菌素 B 的群体药代动力学:对给药方案选择的影响。Clin Infect Dis Off Publ Infect Dis Soc Am。2013;57(4):524-531。doi:10.1093/cid/cit334 61. Tsuji BT、Pogue JM、Zavascki AP 等。多粘菌素最佳使用国际共识指南:由美国临床药学学院 (ACCP)、欧洲临床微生物学和传染病学会 (ESCMID)、美国传染病学会 (IDSA)、国际抗感染药理学学会 (ISAP)、重症监护医学学会 (SCCM) 和传染病药剂师学会 (SIDP) 认可。Pharmacother J Hum Pharmacol Drug Ther。2019;39(1):10-39。doi:10.1002/phar.2209 62。Baddour LM、Wilson WR、Bayer AS 等。成人感染性心内膜炎:诊断、抗菌治疗和并发症处理:美国心脏协会面向医疗专业人士的科学声明。《循环》。2015;132(15):1435-1486。doi:10.1161/CIR.0000000000000296 63. Osmon DR、Berbari EF、Berendt AR 等。假体关节感染的诊断和处理:美国传染病协会临床实践指南。《临床感染性疾病 Off Publ Infect Dis Soc Am》。2013;56(1):e1-e25。doi:10.1093/cid/cis803