XiaoMi-AI文件搜索系统
World File Search System欧盟循环经济行动计划及成员国实践:比利时和法国
欧洲的海滩,并推广可持续的替代品):生效日期:2019 年 7 月 - 修订后的废物框架指令:生效日期:2018 年 7 月。- 欧盟塑料战略,在现有措施的基础上减少塑料垃圾(2018 年 1 月)
SOPP 8217:新药临床试验申请行政处理和审查管理程序 版本:5 生效日期:2017 年 7 月 5 日
答:联邦食品、药品和化妆品法案 (FD&C Act) 第 505 条规定,药品或生物制品必须获得食品和药物管理局 (FDA) 的上市批准,才能跨州运输或分销。IND 是赞助商向 FDA 提出的豁免此法律要求的请求。IND 用于临床研究,以收集安全性和有效性信息,以支持生物制品和药品的上市申请或医学研究。根据 21 CFR 312 子部分 I 中的扩展获取条款,当没有可比或令人满意的替代治疗方案时,IND 还用于在临床试验之外治疗患有立即危及生命的疾病或严重疾病或病症的患者。
主题:海军记录 ICO 审查
, ,工作生效日期为 2020 年 4 月 14 日,预计轮换日期 (PRD) 为 2023 年 4 月。e. 2019 年 12 月 3 日,申请人从 调任,并于 2020 年 1 月 4 日抵达 ,从事临时工作。f. 2020 年 3 月 23 日,请愿人驻扎在 期间收到正式的变更职务命令修改 (BUPERS 命令:1339),生效日期为 2019 年 12 月。请愿人的中间活动 (01) 是根据指示执行临时职务,生效日期为 2020 年 1 月 4 日。请愿人的中间活动 (02) 是临时职务,生效日期为 2020 年 3 月 18 日。请愿人的最终活动是执行职务,生效日期为 2020 年 6 月 30 日,PRD 为 2023 年 4 月。g. 根据参考 (b),本 NAVADMIN 宣布了修订后的现役部队 (AC) 和全职支援 (FTS) 的 SRB 政策,取代了 NAVADMIN 272/19。水手现在必须在其 EAOS 的 365 天内重新入伍(而 NAVADMIN 272/19 要求为 270 天),但接受过核训练的水手除外,他们可以根据 OPNAVINST 1160.8B 中的指导,在重新入伍区的任何时间点重新入伍。h. 2020 年 5 月 21 日,请愿人收到正式的变更职务命令修改通知(BUPERS 命令:1339),驻扎在 ,生效日期为 2019 年 12 月。请愿人的中间活动(01)是根据指示执行临时职务,生效日期为 2020 年 1 月 4 日。请愿人的中间活动(02)是执行临时职务,生效日期为 2020 年 3 月 18 日。请愿人的最终活动是执行职务,生效日期为 2020 年 8 月 17 日,PRD 为 2023 年 9 月。i.2020 年 8 月 26 日,请愿人从 调任,并于 2020 年 8 月 29 日抵达 执行职务。j.2022 年 5 月 10 日,请愿人签署了一份指挥职业申请 (NPPSC 1160/1),要求自 2022 年 8 月 30 日起重新入伍 6 年。请愿人的请求于 2022 年 7 月 18 日获得相关部门批准。k. 根据参考 (c),FY22 SRB 奖励计划 (N13 SRB 004/FY22),列出了 ET 费率的奖励级别为 0.5(奖励上限为 30,000 美元)的“B”区 SRB。l. 2022 年 8 月 30 日,请愿人重新入伍 6 年,EAOS 为 2028 年 8 月 29 日。m. 2023 年 1 月 26 日,通知 BCNR,请愿人于 2022 年 8 月 30 日重新入伍,并担任重新入伍官员。请愿人有资格获得 SRB,并已协商六年入伍,预计 SRB 批准。然而,
1780.1D.pdf - 海军预备役
6. 审查和生效日期。根据 OPNAVINST 5215.17A,COMNAVRESFOR 将在本指令发布周年纪念日每年审查一次,以确保适用性、时效性以及与联邦、国防部、海军部长和海军政策和法定权力的一致性,使用 OPNA V 5215/40 指令审查。本指令将在生效日期后 5 年自动失效,除非在 5 周年纪念日之前重新发布或取消,或已获得延期。
6.01.56心力衰竭患者的心肌交感神经神经成像原始政策日期:2016年1月1日生效日期:11月1日,20
调节状态在2008年,Adreview®(Iobenguane I 123)注射(GE Healthcare)通过美国食品和药物管理局(FDA)新药申请过程(22-290)批准,用于检测原发性或转移性细胞瘤或神经细胞瘤或神经细胞瘤或神经细胞瘤作为辅助测试。5, The FDA (2013) approved a supplemental new drug application (22-290/S-001) for AdreView and expanded the labeled indication to include scintigraphic assessment of sympathetic innervation of the myocardium by measurement of the H/M ratio of radioactivity uptake in patients with New York Heart Association (NYHA) class II or class III heart failure and LVEF less than 35%.6,理由背景心力衰竭估计在美国有620万成年人患有心力衰竭。在2018年,根据2022年心脏和中风统计更新的数据,在2018年的379,800次死亡证明中提到了心力衰竭,六分之一的心力衰竭和射血分数减少在诊断的18个月内导致疾病恶化恶化,这些人更有可能是黑人,> 80岁,> 80岁,> 80岁,> 80岁,> 80岁,合并症率提高了。2,黑人个体在未来发展心力衰竭的风险最高,其次是西班牙裔,白人和美国人,反映了这些人群中高血压,糖尿病和社会经济地位的发生率的差异。黑人个体在未持有心肌梗塞之前的入射心力衰竭的比例最高(75%)。心力衰竭的根本原因包括冠状动脉疾病,高血压,瓣膜疾病和原发性心肌病。These conditions reduce myocardial pump function and decrease left ventricular ejection fraction (LVEF).一种补偿这种降低心肌功能的早期机制是激活交感神经系统。最初增加的交感神经活动有助于通过增加心率和心肌收缩力来补偿心力衰竭,以维持血压和器官灌注。但是,随着时间的流逝,这会给心肌增加额外的压力,增加冠状动脉灌注要求,从而导致缺血性心脏病和/或心肌损伤恶化。作为弥补心肌功能降低的心脏的能力,会导致心力衰竭的临床症状。增强的交感神经活动的另一种有害作用是增加对潜在致命性心律不齐的敏感性。与心力衰竭相关的过度活跃的交感神经涉及心脏交感神经系统的主要神经递质的神经元释放增加。响应交感神经刺激,含有NE的囊泡被释放到神经元突触裂口中。释放的NE与突触后β1,β2和α受体结合,增强了腺基环化酶活性,并带来了所需的心脏刺激作用。去甲肾上腺素被带回储存或分解代谢处置的突触前空间,终止了摄取-1途径的突触反应。NE的释放增加通常伴随着NE的再摄取减少,从而进一步增加了NE水平。诊断成像鸟嘌呤是一种假神经递质,是NE的类似物。它也被摄取-1途径所采用。碘123个二苯甲酰瓜甘油(123 I-MIBG或MIBG)是用放射性碘标记的化学修饰的鸟嘌呤。碘123元碘苯甲烷基鸟氨酸移入突触裂缝中,然后以类似于NE的方式将其置于突触前神经空间中。但是,与NE不同,MIBG未被分解代谢,因此将其集中在心肌交感神经末端。可以使用常规的伽马摄像机对此集中的MIBG进行成像。3,注射后几个小时内MIBG的浓度是交感神经活性的反映,这反过来又可能与心力衰竭的严重程度相关。
俄勒冈州健康计划(OHP)药房现在可以对Covid进行账单...最小化疫苗废物的策略听力通知热水器生效日期
330-092-0015 Effective Dates for Regulated Equipment ¶ The following list specifies the effective dates for equipment standards, test procedures, listing, and labeling requirements which have been adopted in these rules.¶ (1) Bottle-type water dispensers, as defined in OAR 330-092-0010(1): The standards in OAR 330-092-0020(1) are effective for bottle-type water在2022年1月1日或之后制造的分配器。(2)商业热食品持有柜,如ORS 469.229(13)所定义的:ORS 469.233(2)的标准是2009年9月1日生效的,在俄勒冈州销售,2010年9月1日,安装。 469.233(3)是2009年9月1日生效的,用于安装俄勒冈州的设备。在OAR 330-092-0010(14)中定义:OAR 330-092-0020(5)中的标准对于在2022年1月1日或之后制造的便携式电动水疗中心有效。 (7)ORS 469.229(6)中定义的电池充电器系统:ORS 469.233(7)的标准有效:¶(a)2014年1月1日或之后制造的大电池充电器系统。在2018年6月13日或之后生产的联邦监管的大型电池充电器系统被预先获得进一步的州法规。¶(b)零售业出售的小型电池充电器系统不是USB充电器系统,不是电池容量为20瓦小时或更长时间,并且在2014年1月1日或在2014年1月1日之后制造。在2018年6月13日或之后生产的联邦监管的小型电池充电器系统被抢占进一步的州法规。¶(c)零售业出售的小型电池充电器系统是USB充电器系统,其电池容量为20瓦小时或更长时间,并且在2014年1月1日或之后。在2018年6月13日或之后生产的联邦监管的小型电池充电器系统被抢占了进一步的州法规。¶(d)在2017年1月1日或之后生产的零售业未出售的小型电池充电器系统。在2018年6月13日或之后制造的联邦调节的小电池充电器系统是从进一步的州法规中供不应求的。Federally regulated inductive charger systems that are manufactured on or after June 13, 2018 are pre-empted from further state regulation.¶ (f) Battery backups and uninterruptible power supplies, manufactured on or after January 1, 2014, for small battery charger systems for sale at retail, which may not consume more than 0.8+ (0.0021xEb) watts in battery maintenance mode, where (Eb) is the battery capacity in瓦特小时。Federally regulated uninterruptible power supplies that are manufactured on or after June 13, 2018 are pre-empted from further state regulation.¶ (g) Battery backups and uninterruptible power supplies, manufactured on or after January 1, 2017, for small battery charger systems not sold at retail, which may not consume more than 0.8+ (0.0021xEb) watts in battery maintenance mode, where (Eb) is the battery capacity in瓦特小时。在2018年6月13日或之后制造的联邦监管的不间断电源被预先获得进一步的州法规。¶(8)高光输出双端双层石英卤素灯,如ORS 469.229(27)所定义的,ORS 469.233(8)(8)(8)的标准为2016年1月1日,设备均为1月1日的empplion。 OAR 330-092-0020(9)中的标准对高CRI荧光灯有效,该灯在2023年1月1日或之后制造。
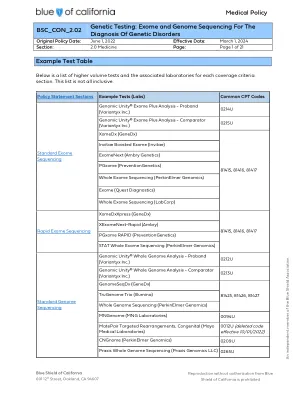
BSC_CON_2.02基因测试:遗传疾病诊断的外显子组和基因组测序原始政策日期:2022年6月1日生效日期:MA
1。可用时至少有3代的完整家族史(或符号为何不符号)2。概率表3的完整详细描述。任何以前的基因检测结果(例如染色体微阵列/CMA,单基因或小面板)4。如果没有进行过以前的测试,则该成员的临床表现不符合良好描述的综合征,该综合征(例如,可以进行特定的测试(例如,单基因测试,CMA))5。外显子测试可能避免的任何侵入性测试6。为什么遗传病因可能是临床和历史发现II的可能解释。标准基因组测序(81425,81426,81427,0209U,0212U,0213U,0265U,0267U)被认为是研究的。iii。重复上述适应症的重复标准外显子组测序(不是重新分析*)可能是
Camino Rojo 项目可行性研究 NI 43-101 技术 ...
报告生效日期:2021 年 1 月 11 日 矿产储量生效日期:2021 年 1 月 11 日 作者:Carl Defilippi、Kappes、Cassiday & Associates、RM SME Michael Hester、Independent Mining Consultants、Inc.、FAusIMM Dr. Matthew Gray、Resource Geosciences Incorporated、CPG John Ward、地下水顾问、CPG