XiaoMi-AI文件搜索系统
World File Search System依赖 PLL2 的伤口反应激活使系统素与其他免疫信号通路区分开来
然后,我们对磷酸肽丰度谱进行了 k 均值聚类,以比较两种细胞培养物之间蛋白质磷酸化的动态变化(图 1d,扩展数据图 2a)。在簇 2 和簇 3 中观察到了最大的差异,其特征是在系统素处理后 1 分钟内磷酸化迅速且短暂地下降。这些簇中不到 20%(198)的肽来自 syr1,而来自系统素反应野生型的肽则超过 80%(1036)(图 1c)。然后,我们检查了这 1036 个肽在 syr1 细胞中是否显示出随时间变化的磷酸化变化,如果是,它们属于哪个簇。我们在除 2 和 3 之外的所有簇中都发现了它们;它们都没有在处理后 1 分钟显示出系统素引起的丰度下降(图 1e)。数据表明,SYR1 介导的系统素反应以细胞蛋白质快速、瞬时去磷酸化为特征,这意味着蛋白磷酸酶在系统素信号传导早期就被激活。
kallikrein抑制剂肽
Abbexa Ltd,创新中心,剑桥科学公园,剑桥,CB4 0EY,英国电话:+44(0)1223 755950-传真:+44(0)1223 755951-
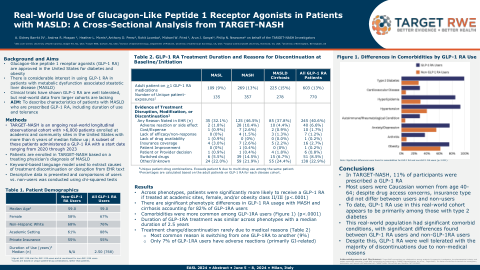
胰高血糖素样肽 1 受体激动剂在 MASLD 患者中的实际使用情况:TARGET-NASH 横断面分析
结论 • 在 TARGET-NASH 中,11% 的参与者被处方了 GLP-1 RA • 大多数使用者是 40-64 岁的白人女性;尽管存在药物获取方面的担忧,但使用者和非使用者之间的保险类型并无差异 • 到目前为止,在这个现实世界的队列中,GLP-1 RA 的使用似乎主要是在那些患有 2 型糖尿病的人身上 • 这个现实世界的人群有明显的合并症,GLP-1 RA 使用者和非 GLP-1RA 使用者之间存在明显差异 • 尽管如此,GLP-1 RA 的耐受性良好,大多数停药都是由于非医疗原因
弓状核介导 GLP-1 受体激动剂……
简介 目前用于治疗肥胖症的大多数药物都是小分子,它们可以穿过血脑屏障 (BBB) 并影响不同的神经元网络。其中几种化合物对大脑的影响范围相当广,有时会导致中枢神经系统副作用 (1)。正在考虑用于治疗肥胖症的新药物是外周肽激素的类似物,如胰高血糖素样肽-1 (GLP-1)、肽 YY 和胰高血糖素,还有一些是受体的拮抗剂,如生长素释放肽受体 (2, 3)。这些激素是肠脑轴的一部分,它们各自的受体通常存在于外周和大脑中 (4-6)。虽然许多研究描述了将激素或类似物直接注入大脑,但令人惊讶的是,人们对这些生理分泌或外周给药的肽激素如何以及在多大程度上进入大脑以及它们如何影响调节能量的关键神经通路知之甚少
KLF15的丧失通过抑制子宫内膜异位症
胰高血糖素是由胰腺α细胞分泌的29个氨基酸胰肽激素。它是源自前体激素progucagon的,它也是胰高血糖素样肠肽的前体(Sandoval&D'Alessio 2015)(图1)。已有近50年的历史,胰高血糖素被认为是相反的胰岛素作用的高血糖因子,并已在药理学上用于纠正胰岛素诱导的低血糖。最近,研究提高了我们对胰高血糖素的生理学的理解,其在糖尿病的因果关系中的潜在作用及其与其他肠激素在调节代谢方面的协同作用。在本文文章中,我们旨在总结胰高血糖素及其转化方面的已知影响。我们将首先回顾胰高血糖素在正常生理和糖尿病中的作用,然后讨论如何将该领域的研究转化为代谢状况的治疗。