XiaoMi-AI文件搜索系统
World File Search System人参皂苷 Rg3 与青蒿琥酯联合使用可克服肝癌细胞和小鼠模型中的索拉非尼耐药性
背景:索拉非尼可有效治疗肝癌,但大多数患者会产生耐药性。STAT3 信号传导与索拉非尼耐药性有关。青蒿琥酯 (ART) 和 20(R)-人参皂苷 Rg3 (Rg3) 具有抗肝癌作用,可抑制癌细胞中的 STAT3 信号传导。本研究旨在评估 Rg3 与 ART 联合使用 (Rg3-plus-ART) 在克服索拉非尼耐药性方面的作用,并研究 STAT3 信号传导在这些作用中的作用。方法:使用索拉非尼耐药的 HepG2 细胞 (HepG2-SR) 评估 Rg3-plus-ART 的体外抗肝癌作用。使用患有 HepG2-SR 肝癌的 BALB/c-nu/nu 小鼠模型评估 Rg3-plus-ART 的体内抗肝癌作用。 CCK-8 测定和 Annexin V-FITC/PI 双染分别用于检测细胞增殖和凋亡。使用免疫印迹法检测蛋白质水平。通过测量 DCF-DA 荧光检测 ROS 生成。结果:Rg3-plus-ART 协同降低 HepG2-SR 细胞活力并诱发其凋亡,并抑制小鼠 HepG2-SR 肿瘤生长。机制研究表明,Rg3-plus-ART 抑制 HepG2-SR 培养物和肿瘤中 Src 和 STAT3 的活化/磷酸化。该组合还降低了 STAT3 核水平并诱导 HepG2-SR 培养物中的 ROS 产生。此外,过度激活 STAT3 或去除 ROS 会降低 Rg3-plus-ART 的抗增殖作用,而去除 ROS 会降低 Rg3-plus-ART 对 HepG2-SR 细胞中 STAT3 活化的抑制作用。结论:Rg3-plus-ART 在实验模型中克服了索拉非尼耐药性,抑制 Src/STAT3 信号和调节 ROS/STAT3 信号是其潜在机制之一。本研究为将 Rg3-plus-ART 开发为治疗索拉非尼耐药性肝癌的新方法提供了药理学基础。© 2021 韩国人参协会。由 Elsevier BV 提供出版服务 这是一篇根据 CC BY-NC-ND 许可 ( http://creativecommons.org/licenses/by-nc-nd/4.0/ ) 发表的开放获取文章。
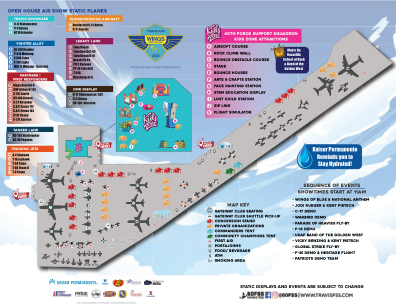
索拉诺上空的翼 8x10 地图 - 特拉维斯空军基地
门户俱乐部座位 门户俱乐部班车接送 小卖部 私人组织 指挥官帐篷 社区冠军帐篷 急救站 移动厕所 食品/饮料 ATM 吸烟区
索拉非尼的广泛转录组学影响及其与肝癌细胞抗肿瘤特性的关系
简单总结:肝细胞癌 (HCC) 是全球第四大癌症相关死亡原因。尽管消融、切除和原位肝移植适用于疾病早期阶段,但索拉非尼 (Sfb) 是目前最常用的晚期 HCC 一线治疗药物,尽管由于出现耐药性,其治疗效果有限。深入了解 Sfb 治疗的分子后果对于优化新的治疗策略以改善晚期 HCC 患者的预后至关重要。在本研究中,我们分析了两种特征明确的肝癌细胞系在 Sfb 治疗后的差异基因表达变化,表明两种细胞系对治疗的反应相似。我们的研究结果提供了有关 Sfb 对各种细胞基本过程(例如 DNA 修复、翻译和蛋白质稳态)的分子作用的宝贵信息,并确定了可以为 Sfb 提供不同治疗视角的合理化问题。
Nrf2 信号促进索拉非尼耐药肝细胞癌细胞中的癌症干细胞性、迁移和 ABC 转运蛋白基因的表达
肝细胞癌 (HCC) 是最常见的原发性肝癌,其发病率持续增长,是一个严重的医学问题。HCC 的发展是一个复杂的多步骤过程,最终会导致炎症损害、肝细胞坏死/再生和纤维化沉积 [1]。然而,HCC 的化疗治疗有局限性。目前用于一线全身治疗的药物,如索拉非尼和仑伐替尼,只能延长患者生存期几个月,主要是因为对这些疗法产生了耐药性 [2]。先前的研究报道了导致索拉非尼耐药 HCC 的潜在机制 [3]。核受体结合蛋白 2 (NRBP2) 可能通过影响 Bcl2 和 Akt 通路中存活蛋白的表达来增加 HCC 细胞化疗耐药性 [4]。组蛋白去甲基化酶赖氨酸特异性去甲基化酶 1 (KDM1A) 可通过激活 Wnt 信号增加 β -catenin 通路,从而降低 HCC 的治疗敏感性 [5]。此外,KRAS 通路加速 RAF/ERK 和 PI3K/AKT 信号传导,导致索拉非尼耐药 HCC 细胞增殖增加、凋亡抑制 [6]。多项研究表明,癌症干细胞 (CSC) 在癌症复发和对分子靶向疗法的主要耐药性中起着重要作用。最近的研究表明,具有干细胞样特征的 HCC 细胞,例如表达 CSC 表面标志 CD44、EpCAM、CD133 和 CD90,对索拉非尼诱导的细胞死亡表现出抗性 [7]。然而,索拉非尼耐药细胞获得癌症干性的机制仍不清楚 [8]。核因子红细胞衍生2样2 (Nrf2) 信号异常常见于多种癌症,包括 HCC,并参与肿瘤发生、肿瘤进展和化疗耐药性[9]。Nrf2 有助于维持氧化应激平衡,并可通过激活多种抗氧化基因的转录促进癌细胞在外来化合物毒素下的存活。Keap1/Nrf2 通路被认为是调节细胞防御氧化应激的主要信号级联。此外,Nrf2 通过驱动巨噬细胞极化为 M2 表型并促进癌细胞迁移来影响肿瘤微环境[10]。正常情况下,Keap1 在细胞质中分离并结合 Nrf2,导致蛋白酶体介导的下游基因降解[11]。在某些情况下,Nrf2 从 Keap1 中释放出来并转移到细胞核中,从而激活 ARE 介导的解毒酶基因表达,包括 HO-1 [ 12 ]。HO-1 参与调节 NRF2 靶向的 ATP 结合盒 (ABC) 外排转运体 (ABCC1、ABCG2 等) [ 13 ]。此外,Nrf2 诱导糖酵解基因的表达,并参与对癌细胞干细胞特性很重要的基因的转录调控,从而促进恶性肿瘤的发生 [14]。Nrf2 信号转导的阴暗面在癌症干细胞中也有描述。激活的 Nrf2 可减少 ROS 的产生并对药物产生抵抗性 [15]。作为转录因子,Nrf2 通过基因编辑技术促进了癌症干细胞的肿瘤生成 [16]。在本研究中,我们研究了肝癌细胞对索拉非尼耐药的机制,重点研究了 Nrf2 信号通路。我们检查了索拉非尼耐药的肝癌细胞
研究文章索拉非尼在...
肝细胞癌(HCC)分别是男性和女性的第五和第八大最常见的恶性肿瘤,每年在全球范围内诊断出500,000多例新病例(Bosch等,1999; Bosch等,2004; Arzumanyan; Arzumanyan等,2013)。跨性化学栓塞(TACE)赋予中级HCC患者的生存益处(Llovet等,2003)。Most clinical practice guidelines, including those of the Barcelona Clinic Liver Cancer (BCLC) (Forner et al., 2018), European Association for the Study of the Liver (European Association for the Study of the Liver, 2018), American Association for the Study of Liver Diseases (AASLD) (Heimbach et al., 2018; Bruix et al., 2011), Asian Pacific Association for the Study of the Liver (APASL) (Omata等,2017)和日本社会
晚期肝细胞癌患者经动脉化疗栓塞术 (TACE) 联合阿帕替尼与 TACE 联合索拉非尼的疗效比较:多中心
在过去十年中,尽管所有肿瘤的发病率呈下降趋势,但肝细胞癌 (HCC) 的发病率却有所上升,东亚地区占了新病例的很大一部分 (1,2)。超过 60% 的 HCC 病例在诊断时已是中期或晚期,大多无法进行治愈性治疗 (3)。根据欧洲肝脏研究协会的临床指南,全身治疗是目前推荐的晚期 HCC [巴塞罗那诊所肝癌 (BCLC) C 期] 的治疗方法 (4)。索拉非尼是一种阻断肿瘤血管生成和生长的多激酶抑制剂,被公认为晚期 HCC 的首个靶向药物。然而,与安慰剂相比,索拉非尼的疗效并不显著,可将 HCC 患者的中位总生存期 (OS) 延长 2.8 个月 (5)。在亚太地区,这种生存获益甚至更为微不足道(OS:6.5 个月 vs. 4.2 个月)(6)。随后,建议将经动脉化疗栓塞术 (TACE) 与索拉非尼联合使用,以在不可切除的肝细胞癌中发挥协同治疗作用。其基本原理是索拉非尼可以抑制 TACE 后的新生血管生成 (7,8)。多项试验已证明,与索拉非尼或 TACE 单药治疗相比,这种联合治疗对肝细胞癌患者的可行性和疗效更佳 (9-11)。然而,不令人满意的缓解率和异质性生存获益仍然促使研究人员寻找新的靶向药物、改进的介入疗法和最佳组合 (12-16)。
新型的抗CMET抗体Seemet 12在大肠癌模型中增强了索拉非尼治疗和放射疗法
酪氨酸 - 蛋白激酶Met(CMET),也称为肝细胞生长因子受体(HGFR),是由MET原始癌细胞编码的异二聚体跨膜酪氨酸激酶受体。CMET受体的天然配体是肝细胞生长因子(HGF),这是一种不活跃的蛋白质,通过蛋白水解裂解将其变为活性形式。与HGF结合后,CMET二聚并触发了催化域中的磷酸化,最终打开了CMET主动对接位点3。CMET激活激活了参与调节运动性,增殖和存活的多种信号转导途径,例如RAS,PI3K,STAT,Beta-catenin和Notch途径(1)。异常调节CMET(2-5)。CMET及其下游信号通路的高激活已被证明可引发过度增殖,肿瘤侵袭,血管生成,并且与存活率较差相关(6)。 各种过程,例如与其他细胞表面受体,配体刺激升高,突变和CMET受体的过表达可能刺激CMET的这种异常信号传导(1)。 除了其作为致癌驱动力的作用外,越来越多的证据表明,CMET是对化学疗法和放疗的抗性的核心因素,以及针对VEGFR和EGFR的靶向疗法。 建议的机制包括促进侵入性生长程序和/或诱导干细胞样性质,以及介导免受凋亡的保护(7-10)。 新的治疗CMET及其下游信号通路的高激活已被证明可引发过度增殖,肿瘤侵袭,血管生成,并且与存活率较差相关(6)。各种过程,例如与其他细胞表面受体,配体刺激升高,突变和CMET受体的过表达可能刺激CMET的这种异常信号传导(1)。除了其作为致癌驱动力的作用外,越来越多的证据表明,CMET是对化学疗法和放疗的抗性的核心因素,以及针对VEGFR和EGFR的靶向疗法。建议的机制包括促进侵入性生长程序和/或诱导干细胞样性质,以及介导免受凋亡的保护(7-10)。新的治疗因此,越来越多地研究了对CMET信号通路的抑制,这并不奇怪。这可能是增强现有靶向疗法以及预防或逆转耐药性的一种方法。索拉非尼耐药是一个例子,最近的研究将CMET活性视为具有重要临床意义的主要阻力因子(11,12)。Sorafenib是最近引入的小分子多激酶抑制剂,目前批准用于治疗例如晚期肾细胞癌和肝细胞癌(HCC),目前正在临床试验中用于治疗结直肠癌(13)。它抑制了参与肿瘤发生的多种激酶(RAF-1,野生型B-RAF,突变体B-RAF,C-KIT,FLT-3和RET)(14),以及促动型受体酪氨酸激酶,包括VEGFR-1/2/2/2/3,PDGFR-1/2,PDGFR-β和FGFR1。然而,在临床试验中,低和不稳定的反应率和短时间持续时间(15)表明固有的原发性和获得的次级电阻。
评论:Rini BI、Pal SK、Escudier BJ 等人。Tivozanib 与索拉非尼在晚期肾细胞癌患者中的疗效比较(TIVO-3):一项 3 期、
在 2020 年 1 月的《柳叶刀肿瘤学》杂志中,Rini 及其同事报道了 TIVO-3 的结果,这是一项开放标签 3 期随机对照试验 (RCT),比较了替沃扎尼与索拉非尼在难治性转移性透明细胞肾细胞癌 (mRCC) 患者中的疗效 (1)。替沃扎尼是一种高选择性血管内皮生长因子受体 (VEGFR) 酪氨酸激酶抑制剂 (TKI),可抑制 VEGFR1、VEGFR2 和 VEGFR3 的磷酸化 (2)。它的半衰期为 4-5 天,抑制 cKIT 和血小板衍生的生长因子 (PDGF) 需要十倍以上的浓度 (2)。与早期的 TKI 相比,替沃扎尼旨在优化 VEGFR 阻断,同时最大限度地减少脱靶毒性作用,最终减少剂量中断和剂量减少 (2,3)。
研究论文 AKR1B10 抑制剂依帕司他通过靶向肝细胞癌中的 mTOR 通路促进索拉非尼诱导的细胞凋亡和自噬
索拉非尼是晚期肝细胞癌 (HCC) 的标准全身治疗,提高其治疗效果对于解决癌症侵袭性至关重要。我们之前报道过,醛酮还原酶 1B10 抑制剂依帕司他增强了索拉非尼对裸鼠 HCC 异种移植瘤的抑制作用。本研究旨在阐明依帕司他抗肿瘤增强索拉非尼的作用机制。用索拉非尼、依帕司他及其组合处理 HepG2 细胞。用细胞计数试剂盒-8 和菌落形成试验评估细胞增殖。通过 ELISA 测定检测 AKR1B10 上清液浓度和酶活性,并检测 NADPH 在 340 nm 处的光密度降低。用流式细胞术进行细胞周期和细胞凋亡分析。蛋白质印迹阐明了对细胞周期、细胞凋亡和自噬影响的分子机制。然后通过 TUNEL 和 HCC 异种移植切片的免疫组织化学染色在体内验证抗肿瘤机制。依帕司他与索拉非尼联合应用在体外抑制 HepG2 细胞增殖,将细胞周期停滞在 G0/G1 期,促进细胞凋亡和自噬。用特定的 mTOR 激活剂 MHY-1485 治疗可增加 mTOR 磷酸化,同时抑制细胞凋亡和自噬。与体外结果一致,HCC 异种移植裸鼠模型的数据也表明联合治疗抑制了 mTOR 通路并促进了细胞凋亡和自噬。总之,依帕司他通过阻断 mTOR 通路增强索拉非尼的抗癌作用,从而诱导细胞周期停滞、细胞凋亡和自噬。
摘要:本研究旨在探讨脂质体氯膦酸盐联合顺铂或索拉非尼对 FOXQ1 表达的影响
摘要:本研究旨在探讨氯膦酸盐脂质体联合顺铂或索拉非尼对肝癌细胞系FOXQ1表达及生物学功能的影响。采用实时定量聚合酶链式反应(qRT-PCR)检测正常肝细胞系和肝癌细胞系中FOXQ1的表达。HepG2和MHCC97H细胞分别给予低、中、高浓度的顺铂(3、5和7 μg/ml)或索拉非尼(2、7和20 μg/ml)联合氯膦酸盐脂质体(LC,20μg/ml),检测各组FOXQ1的表达。采用细胞迁移、MTT和Transwell实验检测各处理对HepG2和MHCC97H细胞生物学功能的影响。 qRT-PCR结果显示,4种肝癌细胞系中FOXQ1 mRNA表达均高于正常细胞,且在HepG2和MHCC97H细胞中FOXQ1 mRNA的表达更占优势。所有试验剂量的顺铂均下调FOXQ1表达,但仅高剂量索拉非尼下调FOXQ1表达,而低、中浓度索拉非尼对FOXQ1表达无明显影响。顺铂或索拉非尼与LC联合应用时,FOXQ1表达水平明显降低。细胞迁移、MTT和transwell实验显示,各药物单独应用时增殖、迁移和侵袭均受到抑制,但与氯膦酸盐脂质体联合应用时作用更强。脂质体氯膦酸盐联合顺铂或索拉非尼可以下调HepG2和MHCC97H肝癌细胞中FOXQ1的表达,抑制其增殖、迁移和侵袭。