XiaoMi-AI文件搜索系统
World File Search System摘要:本研究旨在探讨脂质体氯膦酸盐联合顺铂或索拉非尼对 FOXQ1 表达的影响
摘要:本研究旨在探讨氯膦酸盐脂质体联合顺铂或索拉非尼对肝癌细胞系FOXQ1表达及生物学功能的影响。采用实时定量聚合酶链式反应(qRT-PCR)检测正常肝细胞系和肝癌细胞系中FOXQ1的表达。HepG2和MHCC97H细胞分别给予低、中、高浓度的顺铂(3、5和7 μg/ml)或索拉非尼(2、7和20 μg/ml)联合氯膦酸盐脂质体(LC,20μg/ml),检测各组FOXQ1的表达。采用细胞迁移、MTT和Transwell实验检测各处理对HepG2和MHCC97H细胞生物学功能的影响。 qRT-PCR结果显示,4种肝癌细胞系中FOXQ1 mRNA表达均高于正常细胞,且在HepG2和MHCC97H细胞中FOXQ1 mRNA的表达更占优势。所有试验剂量的顺铂均下调FOXQ1表达,但仅高剂量索拉非尼下调FOXQ1表达,而低、中浓度索拉非尼对FOXQ1表达无明显影响。顺铂或索拉非尼与LC联合应用时,FOXQ1表达水平明显降低。细胞迁移、MTT和transwell实验显示,各药物单独应用时增殖、迁移和侵袭均受到抑制,但与氯膦酸盐脂质体联合应用时作用更强。脂质体氯膦酸盐联合顺铂或索拉非尼可以下调HepG2和MHCC97H肝癌细胞中FOXQ1的表达,抑制其增殖、迁移和侵袭。
大麻用户对莫达非尼的药物滥用
尽管四氢大麻酚(大麻-THC)的依赖性并不像其他非法物质(如海洛因或可卡因)那样严重,但它在过渡到使用其他非法物质的情况下构成了问题1。THC具有许多不利影响,导致记忆,注意力,动机和人际关系的逐步恶化。如今,无法获得针对大麻依赖性的有效药物疗法,行为治疗仅适度有效。不仅疲劳,以及在长期使用THC期间遇到的动力以及动机的困难以及在长期使用THC时遇到的困难,损害受到损害。 为了克服这种情况,用户和医生偶尔会尝试采用一些治疗方式。 莫达非尼,可用于此目的,已被批准为促进药物治疗发作性睡病,工作睡眠障碍和阻塞性睡眠呼吸暂停综合征3的清醒。 此外,它已被用作可卡因成瘾者4的标签外药物,并注意到有利的效果4。 我们在观察一名20岁男性患者后决定写这份报告,该病人是由缓刑和假释办公室指示的。 患者说他已经使用了大约6年的时间,而当他不使用它时,他变得受到约束和烦躁。 患者说他一直在定期使用THC,并且没有停止使用它一个多月,并且没有为此目的接受任何治疗。 4个月前开始服兵役的患者损害受到损害。为了克服这种情况,用户和医生偶尔会尝试采用一些治疗方式。莫达非尼,可用于此目的,已被批准为促进药物治疗发作性睡病,工作睡眠障碍和阻塞性睡眠呼吸暂停综合征3的清醒。此外,它已被用作可卡因成瘾者4的标签外药物,并注意到有利的效果4。我们在观察一名20岁男性患者后决定写这份报告,该病人是由缓刑和假释办公室指示的。患者说他已经使用了大约6年的时间,而当他不使用它时,他变得受到约束和烦躁。患者说他一直在定期使用THC,并且没有停止使用它一个多月,并且没有为此目的接受任何治疗。4个月前开始服兵役的患者
采用预测性生物标志物的不同方法
可操作基因在预测索拉非尼疗效中的作用。方法:通过定量实时逆转录 PCR,我们分析了 220 例接受索拉非尼治疗的 HCC 患者的肿瘤与非癌组织中 7 种可操作基因( VEGFR2 、 PDGFRB 、 c-KIT 、 c-RAF 、 EGFR 、 mTOR 和 FGFR1 )的表达水平。我们的分析发现,与无反应者相比,9 名反应者并没有独特的临床特征。受试者操作特征曲线评估了根据可操作基因计算的治疗效益评分 (TBS) 的预测性能。结果:反应者的 TBS 值明显高于无反应者。曲线下面积为 0.779,mTOR 与 VEGFR2 、 c-KIT 和 c-RAF 相结合的 TBS 是索拉非尼疗效的最显著预测因子。索拉非尼单独使用时,HCC 患者的反应率为 0.7–3%,但当根据可操作基因对患者进行分层时,肿瘤反应率上升至 15.6%。此外,可操作基因表达与肿瘤反应显着相关。结论:我们根据可操作分子亚型对患者进行分层的研究结果可能为提高索拉非尼治疗 HCC 的有效性提供一种治疗策略。
新型的抗CMET抗体Seemet 12在大肠癌模型中增强了索拉非尼治疗和放射疗法
酪氨酸 - 蛋白激酶Met(CMET),也称为肝细胞生长因子受体(HGFR),是由MET原始癌细胞编码的异二聚体跨膜酪氨酸激酶受体。CMET受体的天然配体是肝细胞生长因子(HGF),这是一种不活跃的蛋白质,通过蛋白水解裂解将其变为活性形式。与HGF结合后,CMET二聚并触发了催化域中的磷酸化,最终打开了CMET主动对接位点3。CMET激活激活了参与调节运动性,增殖和存活的多种信号转导途径,例如RAS,PI3K,STAT,Beta-catenin和Notch途径(1)。异常调节CMET(2-5)。CMET及其下游信号通路的高激活已被证明可引发过度增殖,肿瘤侵袭,血管生成,并且与存活率较差相关(6)。 各种过程,例如与其他细胞表面受体,配体刺激升高,突变和CMET受体的过表达可能刺激CMET的这种异常信号传导(1)。 除了其作为致癌驱动力的作用外,越来越多的证据表明,CMET是对化学疗法和放疗的抗性的核心因素,以及针对VEGFR和EGFR的靶向疗法。 建议的机制包括促进侵入性生长程序和/或诱导干细胞样性质,以及介导免受凋亡的保护(7-10)。 新的治疗CMET及其下游信号通路的高激活已被证明可引发过度增殖,肿瘤侵袭,血管生成,并且与存活率较差相关(6)。各种过程,例如与其他细胞表面受体,配体刺激升高,突变和CMET受体的过表达可能刺激CMET的这种异常信号传导(1)。除了其作为致癌驱动力的作用外,越来越多的证据表明,CMET是对化学疗法和放疗的抗性的核心因素,以及针对VEGFR和EGFR的靶向疗法。建议的机制包括促进侵入性生长程序和/或诱导干细胞样性质,以及介导免受凋亡的保护(7-10)。新的治疗因此,越来越多地研究了对CMET信号通路的抑制,这并不奇怪。这可能是增强现有靶向疗法以及预防或逆转耐药性的一种方法。索拉非尼耐药是一个例子,最近的研究将CMET活性视为具有重要临床意义的主要阻力因子(11,12)。Sorafenib是最近引入的小分子多激酶抑制剂,目前批准用于治疗例如晚期肾细胞癌和肝细胞癌(HCC),目前正在临床试验中用于治疗结直肠癌(13)。它抑制了参与肿瘤发生的多种激酶(RAF-1,野生型B-RAF,突变体B-RAF,C-KIT,FLT-3和RET)(14),以及促动型受体酪氨酸激酶,包括VEGFR-1/2/2/2/3,PDGFR-1/2,PDGFR-β和FGFR1。然而,在临床试验中,低和不稳定的反应率和短时间持续时间(15)表明固有的原发性和获得的次级电阻。
敲低SALL4抑制人体和体外肺癌细胞的增殖,迁移和侵袭
直到最近,索拉非尼(7)和兰瓦替尼(8)是唯一被批准用于晚期HCC一线治疗的靶向疗法。尽管在过去几十年中不断寻求有效的高级HCC药物治疗,但患者的生存却没有显着改善。基于检查员040(9)和主题演讲224(10),Nivolumab和pembrolizumab被批准为索拉非尼后的二线治疗。然而,在2019年,第一线与索拉非尼(11)和第三阶段主题演讲240相对于安慰剂与安慰剂(12)的结果是负面的,导致全球批准失败。实际上,这些药物都无法证明具有统计学意义的生存益处。在2020年,Finn等人。(13)报道了Imbrave 150的结果,Imbrave 150的结果是一项临床试验,其中atezolizumab [反编程的细胞死亡配体配体1(PD-L1)单克隆抗体(MAB)]和贝伐单抗研究了对索拉替尼的贝伐单抗,以在第一线设置中治疗先进的HCC。这种组合疗法的无进展生存期(MPF)为6.8个月,索拉非尼单一疗法明显超过4.3个月。尽管在组合疗法组中未达到总体生存期(MOS),但它比索拉非尼组的13.2个月MOS(HR = 0.58,95%CI,0.42-0.79)长得多。因此,
WS9056X 非隔离降压型LED 恒流驱动芯片 - NET
X-ON Electronics 最大的电气和电子元件供应商 点击查看 LED 显示驱动器类别的类似产品: 点击查看 Winsemi 制造商的产品: 其他 类似产品如下:
肝动脉化疗栓塞联合仑伐替尼序贯治疗不可切除肝细胞癌的疗效及安全性
近十年来,分子靶向药物在HCC治疗的临床探索中取得了诸多突破。索拉非尼虽然是HCC最热门的一线治疗药物,但其有效率仅为2%(7)。仑伐替尼是另一种一线药物,于2018年8月获美国食品药品监督管理局(FDA)批准用于治疗HCC。此前有研究表明,仑伐替尼在未治疗的晚期HCC患者中,总生存期(OS)并不劣于索拉非尼,且与索拉非尼相比,中位无进展生存期(PFS)、中位进展时间和客观缓解率(ORR)均显著改善(8)。此外,仑伐替尼在作用机制上更具优势,对多个肿瘤血管调控相关靶点表现出更强的抑制活性和良好的协同抑制作用,尤其是对血管内皮生长因子受体(VEGFR)、成纤维细胞生长因子受体(FGFR)等受体有较好的抑制作用(9)。在 TACTICS 试验之前,许多研究未能证明 TACE 联合分子靶向药物(索拉非尼、布立尼布、奥兰替尼)的疗效(10)。TACTICS 试验表明,对于不可切除的 HCC 患者,与单纯 TACE 相比,TACE 联合索拉非尼可显著改善 PFS(3)。关于 TACE-lenvatinib 序贯疗法治疗 HCC 的研究很少。本研究旨在评估 TACE-lenvatinib 序贯疗法治疗不可切除的 HCC 的疗效和安全性。我们根据 STROBE 报告清单(可访问 https://jgo.amegroups.com/article/)撰写了以下文章
BC癌症协议摘要用于使用阿扎西丁氨酸和索拉非尼治疗急性髓样白血病
4。药物相互作用:索拉非尼主要代谢并通过细胞色素P4503A4在肝脏中排出。必须考虑与细胞色素P4503A4相互作用剂的潜在药物相互作用。另请参见:http://medicine.iupui.edu/flockhart/table.htm 5。高血压:高血压患者在索拉非尼时应谨慎行事。需要严格的血压治疗,因为索拉非尼可能会引起高血压的快速发作。建议使用严重的高血压(大于200 mmHg收缩期或大于110 mmHg舒张压)的暂时悬浮。一旦控制高血压,就可以恢复治疗(另请参见http://www.hypertension.ca)。至少在前两个治疗周期中,患者应每天监测血压(家庭测量,GP办公室等)并保留可以在下次任命时提交给医师的血压期刊。6。乙型肝炎重新激活:有关更多详细信息,请参见SCHBV方案。
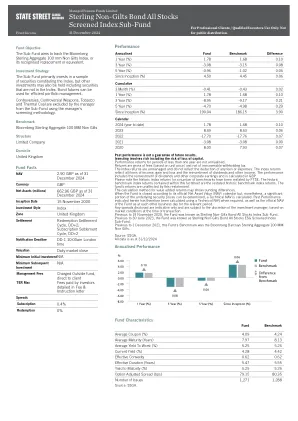
英镑的非镀金债券所有股票筛选索引子基金
过去的表现并不是未来结果的保证。投资涉及风险,包括损失资本的风险。少于一年的绩效收益不到年化。收益是总费用(基于单位价格)和无法抵消的扣除税。指数退货是不受管理的,并且不会反映任何费用或费用的扣除。指数回报反映了收入,收益和损失的所有项目,以及股息和其他收入的再投资。绩效包括股息和其他公司收益的再投资,并在英镑中进行了计算。请注意,FTSE重述了许多基准的历史索引返回。此事实说明中包含的历史基准索引回报是重述的历史基准指数回报。基金的收益不受此重述的影响。增值回报的计算方法可能显示舍入差异。当基金根据其官方净资产价值(NAV)日历关闭时,但是可以确定基本安全价格的很大一部分,则计算出技术NAV。因此,本文指定的过去的绩效是在需要时使用技术导航以及基金的官方NAV在相关期间与互助的官方NAV进行了计算的。根据交易时的市场条件,披露的任何价差仅指示,并由投资经理的酌处权。在2020年11月19日之前,该基金被称为Sterling非Gilts Bond所有股票指数子基金。在2023年6月30日之前,该基金被称为Sterling非Gilts Bond所有股票ESG筛选指数子基金。在2021年12月1日之前,该基金的基准是Bloomberg Barclays Sterming Extregate 100毫米非镀金。
利用CD44V6和V600EBRAF-MON命名甲状腺癌的体外靶向组合疗法
目的:这项研究的目的是通过免疫组织化学和突变分析来评估甲状腺癌的靶向治疗,首次探索患者材料中潜在目标BRAF,EGFR和CD44V6。材料和方法:评估了由七个乳头状(PTC),八个偏型(ATC)和七个卵泡(FTC)甲状腺癌组成的患者队列(n = 22)。此外,分析了八个甲状腺癌细胞系的CD44V6表达以及对多激酶抑制剂索拉非尼(Nexavar®)的敏感性,该抑制剂(Nexavar®)靶向许多丝氨酸/苏氨酸和酪氨酸激酶,包括RAF家族激酶。在3D多细胞肿瘤球体中评估了使用131 I-ABN44V6(一种新型抗CD44V6抗体和/或索拉非尼)的靶向治疗。结果:在两个细胞表面蛋白EGFR和CD44V6中,后者在> 80%的样品中过表达,而EGFR表达水平仅在少数样品中最中等。BRAF突变在PTC患者样品中比在ATC样品中更为普遍,而FTC样品没有含有BRAF突变。与患者样品相比,甲状腺癌细胞系中 CD44V6表达水平的异质性更高,而BRAF突变状态与原始肿瘤类型一致。 3D多细胞ATC肿瘤球体中的单一疗法具有131 I-ABN44V6或索拉非尼导致球体生长延迟。 131 I-ABN44V6和索拉非尼的组合是最有效的,并导致球体生长受到明显损害。CD44V6表达水平的异质性更高,而BRAF突变状态与原始肿瘤类型一致。3D多细胞ATC肿瘤球体中的单一疗法具有131 I-ABN44V6或索拉非尼导致球体生长延迟。131 I-ABN44V6和索拉非尼的组合是最有效的,并导致球体生长受到明显损害。结论:在体外ATC 3D多细胞肿瘤球体中,“概念验证”有针对性的治疗研究表明,将CD44V6用于分子放射疗法作为单一疗法和与索拉非尼结合使用。