XiaoMi-AI文件搜索系统
World File Search System呕吐和腹泻事件清理指南
使用 5.25% 氯漂白剂进行消毒和杀菌浓度 氯消毒浓度应介于 1,000-5,000ppm 之间。食品接触表面应在消毒后冲洗,然后使用 50-100ppm 氯进行杀菌。在对食品接触表面进行杀菌之前,使用化学试纸验证浓度是否合适。请勿使用无溅、低溅或有香味的氯。查看产品标签,确保其对细菌和病毒(如诺如病毒、甲型肝炎和大肠杆菌 O157:H7)有效。其他常用的氯浓度包括 6% 和 8.25%。请注意,其他氯浓度品种的稀释率会有所不同。
1。产品名称Losartan Actavis(氯丹钾12.5mg,25mg,50mg和100mg平板电脑)
基于生命的种族(氯沙坦干预以减少高血压的终点)研究,与atenolol相比,氯沙坦钾对心血管发病率和死亡率的益处不适用于黑人患者的高血压和左心室肥大,尽管两种治疗方案都有效地降低了黑人患者的血液压力。在整体生命研究人群中(n = 9193),与阿替诺洛尔相比,氯沙坦钾治疗的风险降低(p = 0.021),即达到心血管死亡,中风,中风和心肌梗死的患者的患者的风险降低(p = 0.021)。在这项研究中,氯沙坦钾降低了与阿替洛尔在非黑,高血压患者左心室肥大(n = 8660)中相比的心血管发病率和死亡率的风险,这是通过心血管死亡,Stroke,Stroke,STROKE和心肌施加(P = 0.0003)的主要终点所测量的。然而,在这项研究中,与接受Losartan Potassium治疗的黑人患者相比,接受阿替洛尔治疗的黑人患者患有主要复合终点的风险较低(P = 0.03)。在黑人患者的亚组中(n = 533;占生命研究患者的6%),在263例阿替诺尔(11%,每1000名患者年25.9)的患者中,有29例主要终点,在270名患者中有46例(17%,每1000名患者年41.8例)的主要终点。
第 18 章 – 硝化行动计划
确定优化的氯胺消毒处理和分配硝化问题需要监测几个参数。这些参数的量化对于理解和优化氯胺过程以及确定分配系统中可能存在硝化问题的区域至关重要。为了实施 NAP,CWS 应监测总氨氮、游离氨氮、亚硝酸盐氮、硝酸盐氮、一氯胺残留物、二氯胺残留物和总氯残留物。了解氯化曲线(见图 18-1)和这些监测参数的相关性提供了必要的信息,可以在处理方案中进行调整,以优化氯胺过程并最大限度地降低硝化风险。额外的过程管理可能包括监测游离氯和 pH 值。当怀疑存在硝化时,可以使用发现的细菌的种类和量化作为测量硝化程度的手段。
法国圭亚那的结ab:与治疗失败相关的定量和定性因素
摘要背景:控制疮的策略应适用于本地设置。法国圭亚那的传统社区具有非西方的疾病和健康概念。目标:这项研究的目标是探索知识,态度和实践,以识别与这些社区中cab脚治疗失败相关的潜在因素。方法:在2021年4月01日至2021年8月31日之间在卡扬医院或13个卫生中心之一中看到的a疮的患者被包括在内,并在6周后再次看到以检查持久性病变。在围绕和6周时都发现了与治疗失败有关的因素。半结构化访谈是与参与者多样化的子样本进行的。结果:总共有164名参与者在定量组件中包括了21个定性组成部分。宣布已服用第二种治疗剂量与治疗成功有关。西方治疗并不总是负担得起的。用局部治疗观察到比口服伊维菌素更好的依从性,而苄氯菊酯单一疗法则与失败有关。与cabies相关的耻辱感在美洲印第安人和海地人中很高,但在Ndjuka Maroons中不存在。参与者报告的环境解音非常复杂。结论:传统圭亚那社区中疮的治疗可能会因当地对盛装配方的看法,疾病相关的污名和获得医疗保健的差异而有所不同。在制定针对居住在偏远地区和移民人口的传统社区的sc ab夫时,应考虑这些因素。
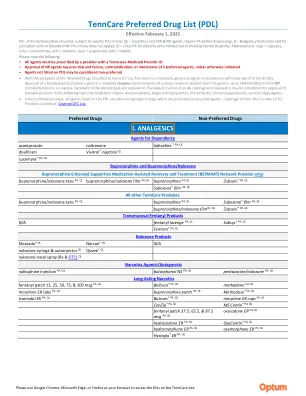
TennCare 首选药物清单 (PDL)
塞来昔布 QL 酮咯酸片 QL Anaprex ® 酮洛芬 1% 双氯芬酸凝胶 QL 美洛昔康片 Celebrex ® QL 酮咯酸鼻喷雾剂 PA 双氯芬酸 50mg 片 萘丁美酮 Daypro ® 甲氯芬那酸 双氯芬酸片 DR 萘普生片(处方药和非处方药) 双氯芬酸胶囊 PA 甲芬那酸 双氯芬酸片 ER Pennsaid ® PA 双氯芬酸小袋 PA 美洛昔康悬浮液和胶囊 PA, QL 布洛芬(处方药和非处方药) 舒林酸 双氯芬酸贴剂 PA, QL Mobic ® 吲哚美辛 双氯芬酸钾 25mg 片 PA Motrin ® 吲哚美辛 ER 双氯芬酸钾 50mg 片 Nalfon ® 双氯芬酸钠片 Naprelan ® 双氯芬酸溶液 PA Naprosyn ® EC-Naprosyn ® 萘普生混悬剂 Elyxyb ® PA, QL 萘普生钠 ER 依托度酸 萘普生 CR 依托度酸 ER 奥沙普秦 Feldene ® 吡罗昔康 非诺洛芬 Relafen DS ® Flector ® PA, QL Sprix ® PA, QL 氟比洛芬 托美汀 Licart ® Toradol ® QL Lofena ® PA Zipsor® Zorvolex® PA
vaxigriptetra-sg-sh-2024.pdf
6.5容器的性质和内容•在预填充的注射器(I型玻璃)中,溶液(I型玻璃)带有柱塞塞子(氯伯木丁基或氯丁基或溴丁基) - 1和20的盒子。•在预灌注注射器(I型玻璃)中,溶液(I型玻璃)带有柱塞塞子(氯丁基或氯丁基或溴丁基),尖端帽(氯伯龙丁基),无针头 - 盒子-1。•在预灌注注射器(I型玻璃)中溶液,带有柱塞塞子(Chlorobromobutyl或chlrobutyl或bromobutylyy),尖端帽(氯伯龙丁基),带有1或2个单独的针 - 1。并非所有包装尺寸或演示文稿都可以销售。
AH Tablet U.S.P. 5mg/160mg/12.5mg empagliflozin/etformin hcl empagliflozin/linagliptin/二甲双胍hcl m XR长时间释放片B.P. 50mg/500mg (MeropeNem作为三水合物)用于注入USP gvia
临床药理学:作用机理:氨氯地平阻止了钙含量对心脏和血管平滑肌细胞的收缩作用; Valsartan阻断了血管紧张素II对心脏,血管平滑肌,肾上腺和肾细胞的血管收缩和钠保留作用;并直接促进肾脏中钠和氯化物在肾脏中的排泄,从而导致血管内体积的造成。药效学:氨氯地平会产生血管舒张,导致仰卧和静脉压力减少。valsartan抑制血管紧张素II输注的压力效应。氢氯噻嗪,二尿症在口服后2小时内开始,在大约4小时内达到峰值,持续约6至12小时。药代动力学:氨氯地平:单独给药后6-12小时,达到了氨氯地平的峰值血浆浓度。从血浆中消除氨氯地平是双相,末端消除半衰期约为30-50小时。连续7至8天的每日给药后达到了氨氯地平的稳态血浆水平。valsartan:在口服瓦尔萨坦之后,仅在2至4小时内达到瓦尔萨坦血浆峰浓度。氢氯噻嗪:氢氯噻嗪并未代谢,而是被肾脏迅速消除。至少有61%的口服剂量在24小时内被消除为未改变的药物。消除半衰期在5.8至18.9小时之间。肾功能不全:瓦尔萨坦:轻度至中度肾功能障碍患者不需要剂量调整。如果发生严重的肾脏疾病,请服用瓦尔萨坦的剂量。氢氯噻嗪:肾功能受损的患者(平均肌酐清除量为19ml/min)的氢氯噻嗪消除的半衰期延长至21小时。肝功能不全:氨氯地平:肝功能不全的患者患有DE-
2023 年 SCI 索引出版物年度数量
轴向 5-[6-(苄氧基)-2H-1,3-苯并恶嗪-3(4H)-基]戊氧基和 5-[6-(己氧基)-2H-1,3-苯并恶嗪-3(4H)-基]戊氧基取代的硅酞菁。有机金属化学杂志,期刊:1003,2023