XiaoMi-AI文件搜索系统
World File Search SystemLeishmania Donovani中的凋亡蛋白 - 寄生虫
摘要 - 内脏利什曼病是一种威胁生命的载体传播疾病,对儿童和老年人免疫功能低下的人的影响不成比例,是一种主要的热带忽视疾病。在利什曼尼亚·多诺瓦尼(Leishmania Donovani)尚未报道过凋亡的伴侣蛋白质,而它们的识别可能会导致有关寄生虫细胞死亡和建立替代治疗剂的知识。我们搜索了哺乳动物的Bcl-2家族蛋白直系同源物,并在多诺瓦尼乳杆菌中发现了一种抗凋亡和两个促凋亡的直系同源物。。 进行了进行分子对接和分子动力学模拟,以评估已识别的凋亡蛋白与模拟哺乳动物固有的凋亡途径之间的蛋白质蛋白相互作用。 恢复表明,两种促凋亡蛋白都与抗凋亡直系同源物的疏水袋相互作用,形成稳定的复合物。 这种相互作用可能代表L. Donovani的凋亡途径中的关键事件。 为了进一步表征它,我们使用了CRISPR-CAS9方法来靶向识别蛋白。 纯敲门的种群突变体,并暴露于凋亡刺激中。 末端脱氧核苷酸转移酶Dutp nick末端标记(TUNEL)测定和定量表达促进表明,这些蛋白质与寄生虫的凋亡有关,并可能在其生存中起作用。。进行分子对接和分子动力学模拟,以评估已识别的凋亡蛋白与模拟哺乳动物固有的凋亡途径之间的蛋白质蛋白相互作用。恢复表明,两种促凋亡蛋白都与抗凋亡直系同源物的疏水袋相互作用,形成稳定的复合物。这种相互作用可能代表L. Donovani的凋亡途径中的关键事件。为了进一步表征它,我们使用了CRISPR-CAS9方法来靶向识别蛋白。纯敲门的种群突变体,并暴露于凋亡刺激中。末端脱氧核苷酸转移酶Dutp nick末端标记(TUNEL)测定和定量表达促进表明,这些蛋白质与寄生虫的凋亡有关,并可能在其生存中起作用。
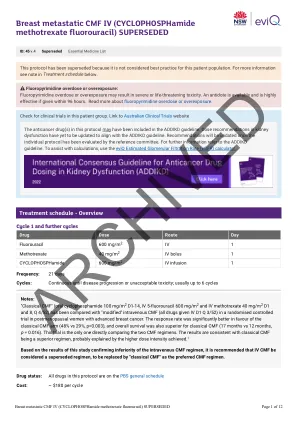
45-胸转移性CMF IV(环磷酰胺甲氨蝶呤)取代| EVIQ
剂量修改的证据是有限的,EVIQ提出的建议仅作为指导。他们通常是保守的,重点是安全。任何剂量修改均应基于临床判断,以及个体患者的状况,包括但不限于治疗意图(治愈性与姑息治疗),抗癌治疗方案(单一对组合疗法与化学疗法与化学疗法与免疫疗法),癌症的生物学,癌症,大小,突变,转移酶的其他副作用,良好的效果,表现良好,效果和其他副作用,表现为其他。修改基于临床试验结果,产品信息,已发表的指南和参考委员会共识。降低剂量适用于每个单独剂量,除非另有说明,否则不适用于治疗周期的总天数或持续时间。非血液学等级基于不良事件的共同术语标准(CTCAE),除非另有说明。肾脏和肝剂量修饰已
«ALzyme-HSTaq» DNA 聚合酶
特性 ALzyme-HSTaq 是一种重组耐热酶,在 dNTP 和引物存在下可催化 5'→3' 单链基质 DNA 合成。它具有 5'→3' 外切酶活性,但没有校正活性。ALzyme-HSTaq 可有效扩增长达 5 bp 的 DNA 片段。特定突变使该酶对血液、土壤、植物组织等中所含的某些抑制剂具有抗性。此外,ALzyme-HSTaq 具有脱氧核苷酸转移酶活性,因此相当一部分扩增的 DNA 分子在 3' 端带有突出的脱氧腺苷 (dA) 残基。热启动技术。该酶在 PCR 混合物混合条件下无活性,在初始变性步骤后被激活。ALzyme-HSTaq 浓度为 5 单位/µl。 100 微升酶(ZHSTaq-100)含有 500 单位,500 微升(ZHSTaq-500)含有 2500 单位。ALzyme-HSTaq-B 反应缓冲液为 ALzyme-HSTaq DNA 聚合酶提供最佳条件。
我们在哪里跑步?
摘要:ALK易位约为所有NSCLC的3–7%。ALK+ NSCLC的临床特征是腺癌组织学,年轻年龄,吸烟史和脑转移。化学疗法和免疫疗法的活性在ALK+疾病中是适度的。几项随机试验证明,在基于铂的化学疗法方面,ALK抑制剂(ALK-IS)具有更大的效率,并且第二/第三代ALK-IS比Crizotinib更好,从而改善了中值无进展的无进展生存和脑转移酶管理。不幸的是,大多数患者会产生对碱性IS的抗性,这是由靶向机制和脱靶机制介导的。转化和临床研究正在继续开发新药和/或组合,以提高标准并进一步改善到目前为止的结果。本综述总结了几种ALK-IS的第一线随机临床试验以及脑转移的管理,重点是ALK-I耐药机制。最后一节解决了未来的发展和挑战。
脑转移中表皮生长因子受体异二聚体的景观
简单的摘要:HER2+乳腺癌患者被用标记HER2+肿瘤细胞的药物治疗,以通过免疫系统消除,下调HER2活性和/或阻止形成HER2二聚体,包括Neuregulin-1受体HER2-HER3。针对HER2靶向的疗法通过降低复发风险,但不能防止脑转移。原因尚未完全理解。我们在203个脑转移和34个原发性乳腺肿瘤样品中量化了HER2-HER3二聚体。与患者匹配的乳腺肿瘤相比,乳腺,卵巢,肺和肾脏癌的脑转移酶的二聚体频率相对较高。但是与HER2/HER3表达或激活没有可靠的相关。在体外实验中,pertuzumab未能抑制HER2+乳腺癌细胞中的HER2-HER3二聚体。这些发现可能会提供有关HER2靶向疗法的颅内和颅外效率差异的见解。
转基因植物(检测
PCR方法是增加想要检查的基因或区域的量,依靠DNA中的双基碱基捕获DNA的新DNS开始是由DNA设计的短DNS或底漆(底漆)。在该基因或我们要检查基因顶部DNA的区域上可能是启动子上的位置。 Terpector or genes selected (Table 1) Table 1 Marker and Reporter Gene Transfer in Plant Gene Enzyme/Protein Encoded Antibiotic Resistance Dihydrofolalate Reductase Methotrexate Resistant Cat Chloramphenicol Acetyltransferase Chloramphenicol Resistant NPTII NOMYCIN PHOTRANFERSE KANAMYCIN RESISTANT AROSISTANT AROVVY Shihimate-3-磷酸合酶草甘膦抗性报告基因CAT CAT氯霉素乙酰基转移酶GUSβ-葡萄糖醛酸糖苷酶诺巴胺合酶Lucifa-Galasse glep glep grep grep grep grep grep grep geel geel fluorescence geel fluorescent div>
外周血指数用Anlotinib预测PFS/OS作为晚期小细胞肺癌的后续治疗
摘要目的:在II阶段Alter-12202(NCT03059797)试验中,Anlotinib显着改善了小型小细胞肺癌(SCLC)患者的无进展生存率(PFS)和总生存期(OS),他们接受了至少2个先前的化学疗法疗法,而与一个地位组相比,他们接受了至少2个先前的化学疗法。为了确定通过Anlotinib治疗预测功效和预后的潜在因素,我们在Anlotinib治疗过程中分析了基线和不良事件(AES)的血液学指数。方法:从2017年3月到2019年4月收集数据,是从Anlotinib的随机,双盲,安慰剂对照,多中心,II期试验中收集的。合格的患者被随机分配2:1,接受Anlotinib或安慰剂,直到疾病进展,无法忍受的毒性或撤回同意。患者每天每3周接受一次酸(12 mg)或类似胶囊(安慰剂)14天。记录了基线时的血液学指数和在最初2个治疗周期中发生的AE。使用Kaplan-Meier检验和Cox回归模型来评估生存差异。结果:将共有82例患者(81例具有完整数据的患者)随机分配接受藻替尼,其中38例接受安慰剂作为对照。多变量分析表明,基线时中性粒细胞与淋巴细胞比> 7.75和乳酸脱氢酶> 254.65 U/L是PFS的独立风险因素。基底升高天冬氨酸氨基转移酶> 26.75 U/L,神经元特异性烯醇酶> 18.64 ng/ml,纤维蛋白原> 4.645 g/L是OS的独立危险因素。在治疗过程中,γγ-谷氨酸转移酶升高和低磷酸血症是PFS较差的独立预测因子,γ-谷氨酸转移酶和高胆固醇血症升高是OS的独立因素。结论:我们的研究初步定义了潜在因素,这些因素在晚期SCLC患者的基线和Anlotinib治疗期间影响了PFS和OS。我们的发现为筛查主要人群和通过Anlotinib治疗进行动态疗效监测提供了基础。关键字小细胞肺癌; Anlotinib;预测因素; PFS; OS
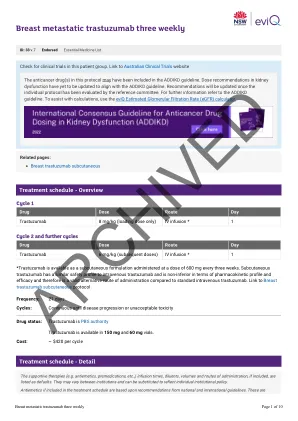
33-胸转移曲妥珠单抗三周
剂量修改的证据是有限的,EVIQ提出的建议仅作为指导。他们通常是保守的,重点是安全。任何剂量修改均应基于临床判断,以及个体患者的状况,包括但不限于治疗意图(治愈性与姑息治疗),抗癌治疗方案(单一对组合疗法与化学疗法与化学疗法与免疫疗法),癌症的生物学,癌症,大小,突变,转移酶的其他副作用,良好的效果,表现良好,效果和其他副作用,表现为其他。修改基于临床试验结果,产品信息,已发表的指南和参考委员会共识。降低剂量适用于每个单独剂量,除非另有说明,否则不适用于治疗周期的总天数或持续时间。非血液学等级基于不良事件的共同术语标准(CTCAE),除非另有说明。肾脏和肝剂量修饰已在可能的情况下进行标准化。有关更多信息,请参见剂量注意事项和免责声明。
引用本文:Abdallah DI、de Araujo ED、Patel NH、Hasan LS、Moriggl R、Krämer OH 等。药物化学在靶向 I 类组织学方面取得进展
组蛋白去乙酰化酶 (HDAC) 是一类锌 (Zn) 依赖性金属酶,负责表观遗传修饰。HDAC 主要与在 DNA 水平上调节基因表达的组蛋白有关。这种严格的调节由组蛋白和非组蛋白的乙酰化 [通过组蛋白乙酰转移酶 (HAT)] 和去乙酰化 (通过 HDAC) 控制,这些蛋白会改变 DNA 的卷曲状态,从而影响基因表达作为下游效应。在过去的二十年里,HDAC 得到了广泛的研究,并被应用于一系列疾病,其中 HDAC 失调与疾病的出现和进展密切相关 - 最突出的是癌症、神经退行性疾病、艾滋病毒和炎症性疾病。HDAC 作为这些生化途径的调节剂参与其中,使其成为一个有吸引力的治疗靶点。本综述总结了为创造 HDAC 抑制剂 (HDACis),特别是 I 类 HDAC 而做出的药物开发努力,重点关注这些抑制剂的药物化学、结构设计和药理学方面。
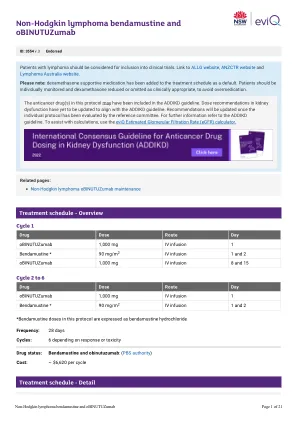
非霍奇金淋巴瘤Bendamustine和obinutuzumab
剂量修改的证据是有限的,EVIQ提出的建议仅作为指导。他们通常是保守的,重点是安全。任何剂量修改均应基于临床判断,以及个体患者的状况,包括但不限于治疗意图(治愈性与姑息治疗),抗癌治疗方案(单一对组合疗法与化学疗法与化学疗法与免疫疗法),癌症的生物学,癌症,大小,突变,转移酶的其他副作用,良好的效果,表现良好,效果和其他副作用,表现为其他。修改基于临床试验结果,产品信息,已发表的指南和参考委员会共识。降低剂量适用于每个单独剂量,除非另有说明,否则不适用于治疗周期的总天数或持续时间。非血液学等级基于不良事件的共同术语标准(CTCAE),除非另有说明。肾脏和肝剂量修饰已在可能的情况下进行标准化。有关更多信息,请参见剂量注意事项和免责声明。