XiaoMi-AI文件搜索系统
World File Search SystemForm Energy 宣布与 Great River Energy 合作进行试点,帮助该公司过渡到经济实惠、可靠且可再生的电网
长效电池使可再生能源即使在极端天气条件下也能可靠地为电网供电,为无碳未来铺平了道路。马萨诸塞州萨默维尔 — Form Energy 是一家为电网开发超低成本、长效储能的公司,今天宣布与明尼苏达州公用事业公司 Great River Energy 签署合同,共同部署位于明尼苏达州剑桥的 1MW/150MWh 试点项目。Great River Energy 是明尼苏达州第二大电力公司,也是美国第五大发电和输电合作社。该系统将是 Form Energy 专有长效储能系统的首次商业部署。Form Energy 的水空气电池系统利用了地球上一些最安全、最便宜、最丰富的材料,为低成本、长效储能转型提供了一条清晰的道路。 Great River Energy 的项目将是一个 1 兆瓦的电网连接存储系统,能够连续提供 150 小时的额定功率,远远超过目前公用事业规模部署的锂离子电池的两到四小时使用时间。这个持续时间允许从存储中为电网提供全新的可靠性功能,而这种功能过去只有热发电资源才能提供。在决定部署试点项目之前,Form Energy 使用 Formware™ 对 Great River Energy 独特的系统特性进行了投资组合优化研究,Formware™ 是一种专有软件分析平台,旨在帮助能源规划人员模拟未来电网。Formware™ 专门用于在系统级别模拟高渗透率可再生能源,并确定所有类型的存储如何实现具有成本效益的可再生能源整合。该工具可帮助规划人员减少极端天气事件的影响,并在各种未来电网情景下最大限度地减少商品价格的不确定性。 Form Energy 分析和业务开发高级副总裁 Marco Ferrara 表示:“为了了解如何最好地实现能源转型,需要新的分析工具,Formware™ 使我们能够与 GRE 合作,系统地、彻底地了解我们的资产可以为其系统带来的价值。”“Great River Energy 很高兴与 Form Energy 合作开展这一重要项目。电网越来越多地由可再生能源供应。商业上可行的长期存储可以通过确保由发电厂产生的电力来提高可靠性。
介孔碳包覆的铝掺杂磁铁矿:在温和条件下固定床反应器中用于苯酚 CWPO 的长效芬顿催化剂
封装在介孔碳 (MC) 中的 Al 掺杂磁铁矿尖晶石纳米粒子被认为是一种有前途的非均相 Fenton 催化剂,可用于实际应用中的连续苯酚降解。在固定床反应器内的工作条件下,制备的 21%γ-Fe 2 O 3 /28%FeAl 2 O 4 @MC 材料中的铁铝尖晶石与 H 2 O 2 发生反应。在该反应中,Al 离子占据了 γ-Fe2O3 组分框架中的空八面体阳离子位,将其转化为 Al 取代的磁铁矿尖晶石。获得的 Fe 3+ 0.66 Fe 2+ 0.33 (Fe 2+ 0.33 Fe 3+ 0.33 Al 3+ 0.33 ) 2 O 4 @MC 中的 Al 通过其路易斯酸特性使铁离子的电子极化,从而使铁离子 (Fe n+(δ+) ) 带上更多的正电荷。这加快了具有挑战性的还原反应 Fe 3+ → Fe 2+ 与 H 2 O 2 生成 HOO˙ 的速度,并加强了尖晶石中铁离子的键合,提高了它们的活性和稳定性。因此,在温和的操作条件下(pH5、40°C、8.6 mlwater/mlcat*h、0.036mol H 2 O 2、200ppm 苯酚),原位生成的催化剂 Fe(Fe 0.66 Al 0.33 ) 2 O 4 @MC 为 35 nm,含有 19.9%Fe 和 2.4%Al,表面积为 335 m 2 /g,在 500 小时的运行中表现出持久的高催化活性和稳定性。在催化性能没有明显变化的情况下,获得了 80% 的 TOC 转化率和处理水中约 1ppm 的浸出 Fe。
抗逆转录病毒方案的耐受性和遵守性含有长效融合抑制剂albuvirvirtide用于HIV暴露后预防:中国的同类研究
(TDF)?lamivudine(3TC)(第2组)和DTG?tdf?3TC(第3组)。 所有招募的子主管在暴露后72小时内接受了PEP,并持续了28天,然后进行了12周。 结果:三组中共有330名参与者。 大多数参与者是男性(87.2%)。 性接触是最频繁的暴露方式(91.9%)。 接触治疗的平均时间为26.8±19.5 h。三个研究组在28天完成口服药物方面没有统计学上的差异。 与口头相比,28天的完成率显示出显着高度(88.9%对64.0%; p \ 0.0001),而ABT的依从性为94.4%,而口服PEP(p \ 0.0001)为75.7%。 含ABT组1的受试者表现出比第3组(87.3%vs. 72.9%; P \ 0.05)更高的依从性。 所有参与者都没有报告严重的不良药物反应,从而导致该研究退出。 所有药物方案均被发现安全且耐受性良好。 在研究期间未观察到HIV事件。 结论:含ABT的方案(ABT?) DTG还是ABT? tdf? 3TC)为HIV PEP提供了一个不错的选择,这是由于更高的完成率和依从性,而不是DTG? tdf? 3TC方案。 三组之间的总体安全性是可比的且可以接受的。3TC(第3组)。所有招募的子主管在暴露后72小时内接受了PEP,并持续了28天,然后进行了12周。结果:三组中共有330名参与者。大多数参与者是男性(87.2%)。性接触是最频繁的暴露方式(91.9%)。接触治疗的平均时间为26.8±19.5 h。三个研究组在28天完成口服药物方面没有统计学上的差异。与口头相比,28天的完成率显示出显着高度(88.9%对64.0%; p \ 0.0001),而ABT的依从性为94.4%,而口服PEP(p \ 0.0001)为75.7%。含ABT组1的受试者表现出比第3组(87.3%vs. 72.9%; P \ 0.05)更高的依从性。所有参与者都没有报告严重的不良药物反应,从而导致该研究退出。所有药物方案均被发现安全且耐受性良好。在研究期间未观察到HIV事件。结论:含ABT的方案(ABT?DTG还是ABT?tdf?3TC)为HIV PEP提供了一个不错的选择,这是由于更高的完成率和依从性,而不是DTG?tdf?3TC方案。 三组之间的总体安全性是可比的且可以接受的。3TC方案。三组之间的总体安全性是可比的且可以接受的。
新闻稿dupixent在欧盟批准为COPD患者的首次有针对性治疗
*基于两项具有标志性的嗜酸性嗜酸性嗜酸菌的不受控制的成年人的双胞胎批准,基于两项具有标志性的嗜酸性粒细胞升高的COPD,这表明dupixent显着降低了dupixent,肺功能的改善,改善了与健康相关的生活质量的改善 * dupixent的第一个新的治疗方法,是一种超过220的新疗法。在欧盟和第七批准的指示全球巴黎和纽约州塔里敦的第六批准指示,2024年7月3日。欧洲药品局(EMA)已批准Dupixent(Dupilumab)作为对不受控制的慢性阻塞性肺疾病(COPD)的插件维护治疗,其特征是血液嗜酸性粒细胞升高。具体而言,该批准涵盖了已经结合了吸入皮质类固醇(ICS),长效beta2-agenist(LABA)和长效的毒蕈碱拮抗剂(LAMA)的患者,如果IC不合适,则是LABA和LABA和LAMA的组合。EMA是世界上第一个批准COPD患者dupixent的监管机构。对全球其他监管机构(包括美国,中国和日本)的其他监管机构正在审查。
首选药物清单 2024 年 1 月 1 日
● 最大允许吗啡毫克当量 (MME) 为 200 MME。短效 (SA) 和长效 (LA) 阿片类药物处方累计计入此计算。超过会员 200 MME 累计 MME 限制的处方需要事先授权,并且可能需要与疼痛管理医生进行提供者对提供者的电话咨询(免费,由 Health First Colorado 提供)。 ● 将授予事先授权以允许逐渐减少剂量 ● 将授予 1 年的事先授权以诊断镰状细胞性贫血 ● 将授予 1 年的事先授权以入住或诊断临终关怀或临终关怀 ● 将授予 1 年的事先授权以治疗癌症相关疼痛 MME 计算使用以下链接中的转换因子进行:https://pharmacypmp.az.gov/resources/mme-calculator 仅一种长效阿片类药物(包括不同强度)和一种短效阿片类药物(包括不同强度)将被考虑用于事先授权。 Medicaid 在我们的网页上“疼痛管理资源和阿片类药物使用”标题下提供了有关疼痛治疗(包括逐渐减少剂量)的指导,网址为:https://www.colorado.gov/pacific/hcpf/pain-management-resources-and-opioid-use
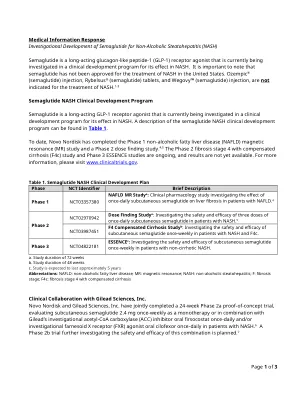
表1。SemaglutideNASH临床开发计划
医学信息反应研究二氟丁物的非酒精性脂肪性肝炎(NASH)Semaglutide是一种长效的胰高血糖素样肽-1(GLP-1)受体激动剂,目前正在临床开发计划中对其在NASH中的作用进行调查。重要的是要注意,Semaglutide尚未被批准用于美国NASH的治疗。ozempic®(semaglutide)注射,rybelsus®(semaglutide)片剂和Wegovy™(semaglutide)注射,未用于治疗NASH。1-3 Semaglutide NASH临床开发计划Semaglutide是一种长效的GLP-1受体激动剂,目前正在临床开发计划中研究其在NASH中的作用。可以在表1中找到Semaglutide NASH临床开发计划的描述。迄今为止,Novo Nordisk已完成1期非酒精性脂肪肝病(NAFLD)磁共振(MR)研究和2期剂量发现研究。4,5阶段2纤维化阶段4具有补偿性肝硬化(F4C)研究和第3阶段的本质研究正在进行,尚不可用。有关更多信息,请访问www.clinicaltrials.gov。表1。Semaglutide NASH临床开发计划
2024 年 MPP 优先级报告
MPP 的工作始于小分子药物,在 2022 年开展了一项关于扩大生物治疗药物可及性的可行性研究后,其职责范围扩大到生物制剂。此外,鉴于其具有突破性的潜在影响,自 2021 年以来,长效技术和旨在延长药物使用时间的配方将被视为优先事项,同时还将考虑任何相关的新型医疗技术,MPP 的干预措施可能会对公共卫生产生积极影响。
国际抗病毒学会 2024 年建议
结果 继续建议所有 HIV 感染者接受抗逆转录病毒疗法。对于大多数 HIV 感染者,建议初始治疗方案由整合酶链转移抑制剂 (InSTI)(特别是比克替拉韦或多替拉韦)和 2 种(在某些情况下为 1 种)核苷或核苷酸逆转录酶抑制剂组成。建议针对具有特殊临床情况(例如怀孕和活动性机会性疾病)以及无法服用 InSTI 的人。治疗方案可能需要因病毒学失败、不良反应、便利性或成本等原因而改变。对于那些不喜欢每天服用口服药物的人以及难以坚持每天治疗的人,可以使用长效注射疗法。建议针对实验室监测、物质使用障碍和体重变化管理以及使用他汀类药物预防心血管疾病。对于 HIV 预防,口服(每日或间歇性)和注射长效药物是 HIV 暴露可能性较高的人的有效选择。此外,还推荐了维持艾滋病毒感染者健康和福祉的新工具,例如使用强力霉素进行暴露后预防以避免性传播感染,以及治疗物质使用障碍的策略。讨论了艾滋病毒感染和护理机会方面的差异,并提出了解决方案。
基于生长抑素受体的治疗测序......
大多数分化良好的神经内分泌肿瘤 (NET) 都表达高水平的生长抑素受体,特别是 2 型和 5 型。生长抑素类似物 (SSA) 与生长抑素受体结合,用于缓解激素综合征和控制肿瘤生长。长效 SSA 奥曲肽长效缓释片和兰瑞肽因其可耐受的副作用而常用于一线转移性治疗。放射性标记的 SSA 既可用于成像,也可用于 NET 治疗。177 Lu-DOTATATE 是一种放射性标记的 SSA,已被证明可显著改善进行性中肠 NET 患者的无进展生存期,并被批准用于治疗转移性胃肠胰腺 NET。在治疗胃肠胰腺和肺 NET 患者时,一个关键问题是 177 Lu-DOTATATE 的治疗顺序,以及与其他全身治疗(如依维莫司)或肝脏导向治疗的关系。鉴于 NET 的异质性以及几乎没有比较积极治疗方案的随机试验,这个问题尤其复杂。这篇最先进的综述研究了支持在 NET 治疗的更广阔领域中使用生长抑素受体靶向治疗的证据,并提供了有关最佳患者选择、效益与风险评估和治疗顺序的见解。