XiaoMi-AI文件搜索系统
World File Search System代谢和靶器官损伤 - ePrints Soton
摘要 在本综述中,我们讨论了与代谢紊乱精准医疗相关的选定主题。个性化饮食和运动可能有助于预防肥胖和 2 型糖尿病 (T2D)。减肥应根据年龄、性别、种族和共存合并症进行个性化。我们对肥胖的病理生理学、遗传学和表观遗传学的理解不断进步,有望提供量身定制的管理方案。干预前必须进行仔细的风险评估。风险可能被低估,例如在女性、不同种族群体和 2 型糖尿病患者中。对于那些对传统风险因素管理(如血脂异常和动脉高血压的药物治疗)没有反应的人,更个性化的方法可能会有用。非酒精性脂肪性肝病/代谢相关脂肪性肝病 (NAFLD/MAFLD) 既是葡萄糖和脂质代谢改变的原因,也是其结果。个性化医疗方法可能是确定更有效的药物策略以及逆转这种常见且繁重的代谢性肝病的关键。最后,代谢组学可用于识别与癌症诊断、分期和预后相关的生物标志物。结肠癌、直肠癌、乳腺癌、前列腺癌、甲状腺癌和卵巢癌表明,癌细胞代谢紊乱可用于临床实践。应追求真正的个性化药物治疗,尤其是对于肥胖癌症患者。
自我测量家庭血压控制良好的高血压患者的隐匿性夜间高血压和靶器官损害
有报道指出,隐匿性高血压(患者的诊室血压正常,但家庭自我测量的血压却高于诊室外血压)与持续性高血压非常相似,是心血管发病的预测因素。此外,夜间血压与心血管疾病密切相关。这可能意味着动态和家庭自我测量的血压监测各自提供独立的信息。我们对 165 名社区居民进行了动态血压监测、家庭自我测量的血压监测、超声心动图和颈动脉超声检查。我们根据动态和家庭自我测量的血压水平将患者细分为:隐匿性夜间高血压组,家庭自我测量的血压水平 < 135/85 mmHg,动态夜间血压水平≥ 120/75 mmHg;正常血压组患者家庭自我测量血压 < 135/85 mmHg,夜间动态血压 < 120/75 mmHg。隐匿性夜间高血压组的心肌内膜中层厚度 (IMT) 和相对壁厚度 (RWT) 均大于正常血压组(IMT:0.76±0.20 vs 0.64±0.14 mm,p < 0.05;RWT:0.50±0.14 vs 0.41±0.10,p < 0.05)。即使是家庭自我测量血压控制良好的高血压患者,夜间动态血压升高也可能促进靶器官损害。我们必须使用家庭自我测量血压监测来排除隐匿性高血压,我们也可能需要使用动态血压监测来排除夜间隐匿性高血压。 (高血压研究 2007;30:143–149)
抗高血压治疗对隐匿性高血压患者靶器官保护的疗效(ANTI-MASK):一项多中心、双盲、安慰剂对照试验
方法 这项在中国 15 家医院开展的多中心、随机、双盲、安慰剂对照试验纳入了 30 – 70 岁未经治疗的门诊患者,门诊血压 (BP) <140/<90 mm Hg,24 小时、白天或夜间动态血压 ≥ 130/≥ 80、≥ 135/≥ 85 或 ≥ 120/≥ 70 mm Hg。患者有 ≥ 1 个 TOD 体征:心电图左心室肥大 (LVH)、臂踝脉搏波速度 (baPWV) ≥ 1400 cm/s,或尿白蛋白与肌酐比值 (ACR) ≥ 3.5 mg/mmol(女性)和 ≥ 2.5 mg/mmol(男性)。排除标准包括继发性高血压、糖尿病肾病、血清肌酐≥176.8μmol/L和筛选前6个月内患心血管疾病。根据中心、性别和夜间高血压分层后,符合条件的患者被随机分配(1:1)接受抗高血压治疗或安慰剂治疗。患者和研究者都不知道分组情况。积极治疗包括从80mg/天开始的艾力沙坦,在第2个月增加到160mg/天,如果动态血压仍然无法控制,则在第4个月联合使用氨氯地平2.5mg/天。对照组同样使用匹配的安慰剂。主要终点是TOD的改善,定义为在48周的随访中baPWV、ACR或LVH恢复正常,或baPWV或ACR减少≥20%。意向治疗分析包括所有随机患者,符合方案分析包括完全遵守方案的患者,安全性分析包括所有接受至少一剂研究药物的患者。本研究已在 ClinicalTrials.gov 注册,注册号为 NCT02893358。
临床药物开发中的安全考虑
– 物种的选择或相关性 – 潜在的毒性靶器官 – 持续时间、剂量、暴露途径 – 药代动力学和药效学评估 – 确定剂量反应 – 特殊人群的安全性(儿科、孕妇
安全数据表 1158 (en-GB) - ezentrumbilder3.de
毒理学影响:这些陈述源自单个成分的特性。该产品本身没有毒理学数据。急性毒性(口服):缺乏数据。急性毒性(经皮):缺乏数据。急性毒性(吸入):缺乏数据。皮肤腐蚀/刺激:皮肤刺激 2;H315 = 引起皮肤刺激。严重眼损伤/刺激:眼睛刺激 2;H319 = 引起严重眼刺激。呼吸道致敏性:根据现有数据,不符合分类标准。皮肤致敏性:根据现有数据,不符合分类标准。生殖细胞致突变性/遗传毒性:根据现有数据,不符合分类标准。致癌性:根据现有数据,不符合分类标准。生殖毒性:缺乏数据。对哺乳或通过哺乳产生的影响:缺乏数据。特定靶器官毒性(单次暴露):STOT SE 3;H336 = 可能导致嗜睡或头晕。特定靶器官毒性(反复暴露):根据现有数据,未满足分类标准。吸入危害:根据现有数据,未满足分类标准。
次要药理学结合试验对非临床发现的转化价值
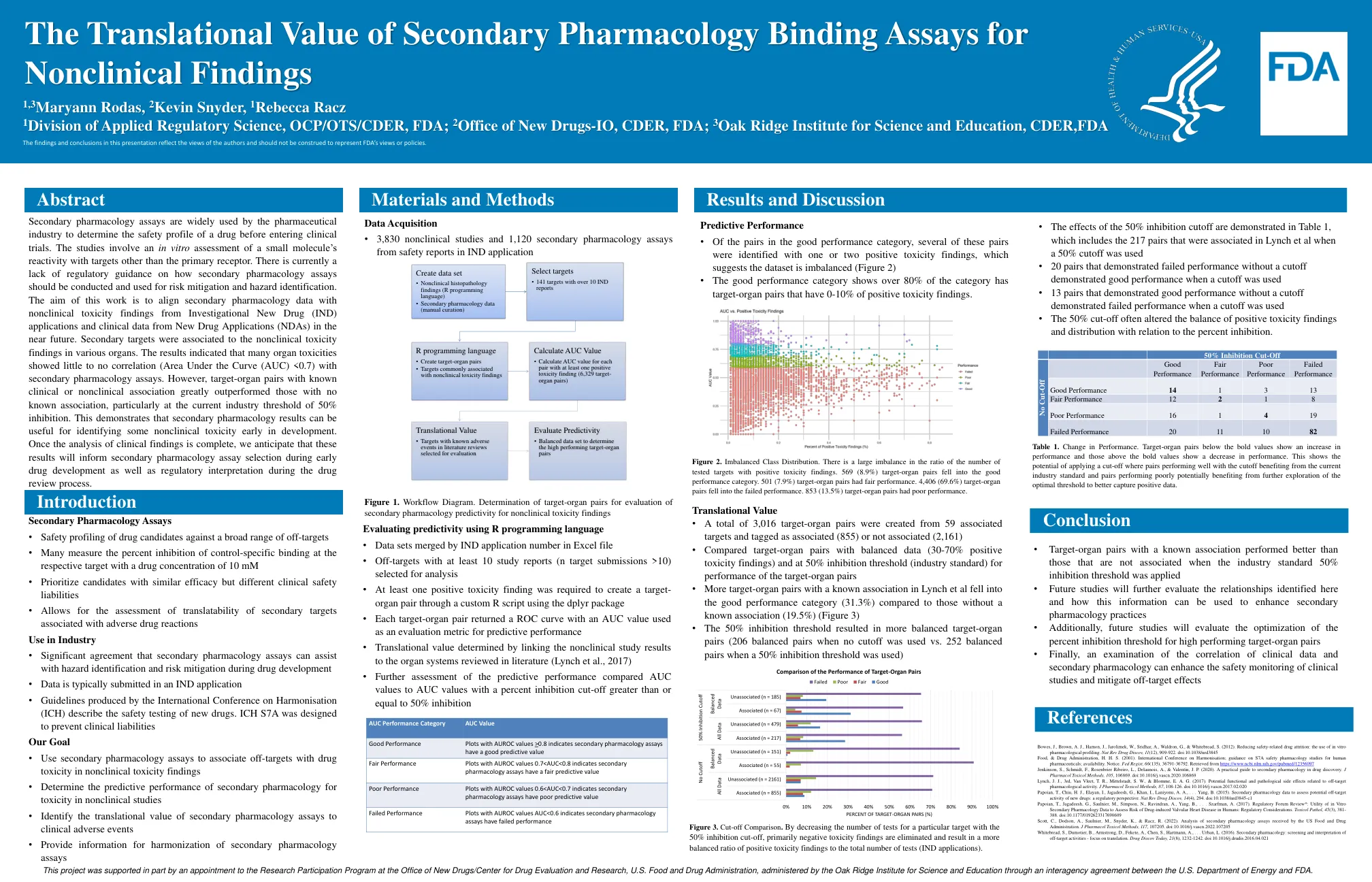
制药行业广泛使用次级药理学试验来确定药物在进入临床试验之前的安全性。这些研究涉及对小分子与主要受体以外的靶标的反应性的体外评估。目前缺乏关于如何进行次级药理学试验以及如何将其用于降低风险和识别危害的监管指导。这项工作的目的是将次级药理学数据与近期新药研究 (IND) 申请中的非临床毒性发现和新药申请 (NDA) 中的临床数据进行对比。次级靶标与各种器官中的非临床毒性发现相关。结果表明,许多器官毒性与次级药理学试验几乎没有相关性(曲线下面积 (AUC) <0.7)。然而,具有已知临床或非临床关联的靶器官对的表现远远优于没有已知关联的靶器官对,尤其是在当前行业阈值 50% 抑制的情况下。这表明,次要药理学结果可用于在开发早期识别一些非临床毒性。一旦完成对临床结果的分析,我们预计这些结果将为早期药物开发期间的次要药理学检测选择以及药物审查过程中的监管解释提供参考。
疏水性、运输和作用靶位对许多药物的活性至关重要
高度脂溶性,主要通过血脑屏障的疏水性概念,因此维生素 A、D、E、K 主要从血液循环迁移到脂肪组织,然后到达血脑屏障。因此,尽管疏水性很重要,但除了疏水性之外,还有其他因素参与了这一活动,例如,药物运输到药物靶器官的细胞,运输可能根据已知的运输机制进行,例如,根据药物浓度的被动扩散,从高浓度的细胞或器官外运输到细胞或器官内,主动运输,即药物的转移和需要
射频电磁辐射对大脑神经递质的影响
随着近30年来电子信息的飞速发展,基于电磁的技术成果被广泛应用于人类生产生活的各个领域,电磁辐射(EMR)已成为现代文明中重要的新型污染源。EMR的生物学效应已引起全世界的广泛关注,其中EMR与人体器官特别是脑的可能相互作用是目前最为关注的。许多研究表明,神经系统是对EMR敏感的重要靶器官系统。近年来,越来越多的研究集中于EMR的神经生物学效应,包括神经递质的代谢和转运。神经递质作为突触传递的信使,在认知和情绪行为中起着至关重要的作用。本文总结了EMR对脑内神经递质代谢和受体的影响。
高血压的免疫神经控制
摘要 — 神经系统和免疫系统具有在内部和外部环境界面上发挥守门人作用的共同能力。尽管这两个进化上高度保守的系统之间的相互作用早已被认识到,但对它们之间相互作用的病理生理机制的研究直到最近几十年才开始着手。过去几年的最新研究阐明了自主神经系统如何控制高血压引起的脾脏免疫。本综述将重点介绍调节免疫反应的神经机制以及这种神经免疫相互作用在高血压中的作用。在此背景下,本综述重点介绍了脑脾轴的组成部分,重点介绍了脾脏中建立的神经免疫界面,神经信号在此影响高血压靶器官的免疫反应。
SHR-A1811,一种新型抗HER2抗体 - 药物结合物,具有最佳的药物与抗体比,优越的旁观者杀戮效果和有利的安全概况
SHR169265比SHR197971(DXD类似物)表现出更好的渗透性,更强的细胞毒性和更快的全身清除率。SHR-A1811的药物与抗体比(DAR)通过平衡功效和毒性优化为6。SHR-A1811显示出对各种细胞系的HER2依赖性生长抑制作用,以及理想的旁观者杀死能力。SHR-A1811以剂量依赖性的方式导致肿瘤生长抑制甚至消退,至少与HRA18-C015(T-DXD的生物仿制药)和抗HER2-SHR2-SHR2-SHR169265(DAR 8)在具有HER2表达水平范围范围的多个Xenograft模型中。SHR-A1811表现出良好的药代动力学特征,在不同物种的血浆中出色的稳定性以及有利的临床前安全性。cynomolgus猴子中最高的非毒性剂量(HNSTD)为40 mg/kg,胸腺作为主要靶器官。