XiaoMi-AI文件搜索系统
World File Search SystemZolbetuximab
Zolbetuximab注射(Vyloy)
来自2个随机,双遮盖的,安慰剂对照的III期试验(Spotlight and Glow)的证据表明,Zolbetuximab添加到氟吡啶丁胺 - 和铂的化学疗法中时(改良的氟尿嘧啶加氟尿嘧啶加上白细胞素的改性,以及对OXALIPPATIN 6 [MFOLFOLFOFFOOX 6]或CAPECITIPLAT []或CAPECITIPLAT []或CAPECITIPLATIN []或CAPECALIPLATIN []患有局部晚期不可切除或转移性HER2-阴性胃癌或GEJ腺癌的患者具有CLDN18.2阳性的肿瘤患者,从而增加了临床益处。The SPOTLIGHT trial (N = 565) demonstrated that treatment with zolbetuximab in combination with mFOLFOX6 resulted in statistically significant and clinically meaningful improvements in overall survival (OS) (hazard ratio [HR] = 0.784; 95% confidence interval [CI], 0.644 to 0.954; P = 0.0075) and progression-free survival (PFS) (HR = 0.751;与安慰剂结合使用MFOLFOX6,CI,0.598至0.942;The GLOW trial (N = 507) similarly demonstrated that treatment with zolbetuximab in combination with CAPOX resulted in statistically significant and clinically important meaningful improvements in OS (HR = 0.763; 95% CI, 0.622 to 0.936; P = 0.0047) and PFS (HR = 0.687; 95% CI, 0.544 to 0.866; P = 0.0007),与安慰剂与Capox结合使用相比。在关键试验中,与单独的化学疗法相比,用化学疗法结合使用Zolbetuximab与化学疗法结合使用,与恶心,呕吐和输注相关的反应的风险增加有关。但是,PERC与临床专家一致,这些不良事件(AES)在临床实践中可能是可以管理的。
安斯泰来公司的 VYLOY™(佐贝妥昔单抗)在日本获批用于...
东京,2024 年 3 月 26 日——安斯泰来制药公司(TSE:4503,总裁兼首席执行官:Naoki Okamura,“安斯泰来”)今天宣布,2024 年 3 月 26 日,日本厚生劳动省 (MHLW) 批准了抗紧密连接蛋白 18.2 (CLDN18.2) 单克隆抗体 VYLOY™(zolbetuximab),用于治疗 CLDN18.2 阳性、不可切除、晚期或复发性胃癌患者。VYLOY 是全球首个也是唯一一个获得监管机构批准的 CLDN18.2 靶向疗法。由于早期症状与其他更常见的胃病重叠,胃癌通常在晚期或转移期才被诊断出来。 1 尽管日本努力减少胃癌的影响,但胃癌仍然是日本第三大致命癌症,2022 年诊断出 126,724 例。 2 Moitreyee Chatterjee-Kishore,博士,工商管理硕士,安斯泰来高级副总裁兼免疫肿瘤学开发主管 “厚生劳动省批准 VYLOY 标志着胃癌治疗的新时代,为患有这种毁灭性疾病的 CLDN18.2 阳性患者提供了第一个也是唯一的靶向治疗选择。安斯泰来很自豪能够帮助解决日本对这种难以治疗的癌症的迫切治疗需求,日本的发病率位居全球前列。重要的是,此次批准有可能为符合条件的患者提供更多宝贵的时间与亲人相处,兑现我们改善患者治疗效果的承诺。” SPOTLIGHT 试验首席研究员、日本柏市国立癌症中心东医院胃肠肿瘤科主任 Kohei Shitara 医学博士表示:“开发新的靶向疗法对于晚期胃腺癌等疾病至关重要,这种疾病的治疗选择非常有限,而且往往在晚期才被发现。作为 3 期 SPOTLIGHT 临床试验的首席研究员,我亲眼目睹了 VYLOY 联合化疗治疗患者的无进展生存期和总生存期与安慰剂联合化疗治疗患者的无进展生存期和总生存期相比有显著改善。这些结果支持 VYLOY 成为日本 CLDN18.2 阳性人群的新治疗选择,仅在 2022 年,日本就有近 44,000 人死于胃癌。”此次批准基于 3 期 SPOTLIGHT 和 GLOW 临床试验的结果,该试验针对局部晚期不可切除或转移性 HER2-
佐贝妥昔单抗治疗不可切除和转移性胃及胃食管连接部腺癌:文献综述
本文全面回顾了佐贝妥昔单抗的作用、疗效和安全性。佐贝妥昔单抗是一种开创性的嵌合单克隆抗体,旨在靶向 Claudin 18.2 (CLDN18.2),这是一种紧密连接蛋白,在各种胃肠道癌症中经常过表达,包括胃腺癌 (G) 和胃食管连接部腺癌 (GEJ)。这种药物在治疗不可切除和转移性 G/GEJ 癌症方面引起了关注,尤其是对于肿瘤表达 CLDN18.2 的 HER2 阴性患者。佐贝妥昔单抗是一种与 CLDN18.2 结合的药物,其结合可启动免疫反应,攻击和杀死癌细胞。它通常与氟嘧啶和含铂化疗联合使用。该药物(以前称为 IMAB362),商品名为 Vyloy,由日本东京的 Astellas Pharma 开发。经过多轮临床试验,它被美国食品药品监督管理局(FDA)批准作为局部晚期、不可切除癌症的一线治疗方案,成为晚期G/GEJ癌症的一种有希望的选择。
新闻稿
“我们很高兴为欧洲患者带来一流的靶向治疗选择佐贝妥昔单抗,在欧洲,胃癌和胃食管癌是癌症相关死亡的第六大原因。有了佐贝妥昔单抗,我们将进入晚期癌症精准医疗的新时代,这也巩固了我们持续致力于开拓科学发现以改善患者治疗效果的承诺。”支持欧洲营销授权的 3 期 SPOTLIGHT 和 GLOW 临床试验的数据表明,与其他标准化疗相比,佐贝妥昔单抗治疗在胃癌和 GEJ 癌符合条件的患者中,无进展生存期 (PFS) 和总生存期 (OS) 均有显着改善。1,2 在 SPOTLIGHT 试验中,佐贝妥昔单抗联合 mFOLFOX6 作为一线治疗的中位 PFS 为 10.61 个月,而安慰剂联合 mFOLFOX6 为 8.67 个月。两个治疗组的中位 OS 分别为 18.23 个月和 15.54 个月。1 在 GLOW 试验中也发现了类似的疗效结果,中位 PFS 分别为 8.21 个月和 6.80 个月,中位 OS佐贝妥昔单抗加 CAPOX 组为 14.39 个月,而安慰剂加 CAPOX 组为 12.16 个月。2 在 SPOTLIGHT 和 GLOW 试验中,佐贝妥昔单抗治疗组与对照组的严重治疗突发不良事件 (TEAE) 发生率相似。佐贝妥昔单抗治疗组中报告的最常见的全级别 TEAE 是恶心、呕吐和食欲下降。1,2
cldn18.2-阳性的线处理,...
基于IOMARKER的靶向疗法改变了癌症治疗范式。虽然早期胃和胃食管连接(GOJ)腺癌可以从手术中受益,但这些疾病的晚期表现具有有限的治疗选择和预后不良。Zolbetuximab,一种靶向Claudin 18.2(Cldn18.2)的嵌合单克隆抗体,通过抗体依赖性细胞细胞毒性和补体依赖性细胞毒性发挥作用。它已成为晚期胃/GOJ癌的有前途的治疗方法。临床试验评估了其在多个阶段的功效和安全性,表明无进展生存率和整体生存率有了显着改善。Zolbetuximab的安全性主要包括可管理的胃肠道不良事件,即恶心和呕吐。Zolbetuximab的潜力超出了其主要指示,正在进行的试验探索了其在其他表达恶性肿瘤(例如胰腺腺癌)中的功效。本评论重点介绍了Zolbetuximab作为CLDN18.2阳性,HER2阴性胃和GOJ腺癌的一线疗法的潜力,阐明了其作用机理,临床试验结果,安全性,安全性,安全性和当前治疗景观。
新闻稿
美国首个也是唯一一个 CLDN18.2 靶向疗法 东京,2024 年 5 月 30 日——安斯泰来制药公司(TSE:4503,总裁兼首席执行官:Naoki Okamura,“安斯泰来”)今天宣布,美国食品药品监督管理局 (FDA) 已承认该公司重新提交了 zolbetuximab 的生物制品许可申请 (BLA),zolbetuximab 是一种一流的试验性 claudin (CLDN) 18.2 靶向单克隆抗体,用于一线治疗局部晚期不可切除或转移性人表皮生长因子受体 2 (HER2) 阴性胃或胃食管连接处 (GEJ) 腺癌的成人患者,其肿瘤为 CLDN18.2 阳性。一旦获得批准,zolbetuximab 将成为美国批准针对该患者群体的首个 CLDN18.2 靶向治疗药物 根据处方药使用者付费法案 (PDUFA),FDA 设定了新的目标行动日期为 2024 年 11 月 9 日。 在美国,据估计,2024 年将有 26,890 人被诊断出患有胃癌,10,880 人将死于该疾病。1 由于早期胃癌症状经常与更常见的胃相关疾病重叠,因此胃癌通常在晚期或转移性阶段被诊断出来,或者在胃癌从肿瘤来源扩散到其他身体组织或器官后才被诊断出来。2 转移性患者的五年相对生存率为 7%。1 Moitreyee Chatterjee-Kishore,博士,工商管理硕士,安斯泰来高级副总裁兼免疫肿瘤学开发主管 “安斯泰来致力于为难治性癌症推出新的靶向疗法。晚期胃癌或 GEJ 癌患者通常面临着巨大的未满足需求,FDA 对 zolbetuximab BLA 重新提交的认可,使我们距离为美国面临这种致命疾病的合格患者提供这一重要治疗选择又近了一步。” zolbetuximab BLA 于 2024 年 5 月 9 日重新提交,此前 FDA 于 2024 年 1 月 4 日因在设施许可前检查中发现第三方制造缺陷而发出了完整回复信。FDA 未对 zolbetuximab 的临床数据(包括疗效或安全性)提出任何担忧,也未要求进行额外的临床研究来支持 BLA 批准。zolbetuximab BLA 基于 3 期 SPOTLIGHT 和 GLOW 临床试验的结果。 3,4 SPOTLIGHT 研究评估了佐贝妥昔单抗加 mFOLFOX6(一种包括奥沙利铂、亚叶酸钙和氟尿嘧啶的联合方案)与安慰剂加 mFOLFOX6 的疗效。GLOW 研究评估了佐贝妥昔单抗加 CAPOX(一种包括卡培他滨和奥沙利铂的联合化疗方案)与安慰剂加 CAPOX 的疗效。
pdf -Chin J Cancer Res
Zolbetuximab是一种与CLDN18.2结合的单克隆嵌合抗体,会导致抗体依赖性细胞毒性和补体依赖性细胞毒性,从而导致肿瘤细胞死亡。基于快速研究的结果(5),Zolbetuximab Plus Eox(半蛋白脂蛋白,草酸氨基蛋白和卡昔替邦),在Cldn18.2阳性(Cldn18.2 stription in Cldn18.2 stription in Cldn18.2- gaseacte,40%/gaseacte gaseacte in Cldn18.2)中,无进展生存率(PFS)显着延长腺癌患者与仅患有EOX化学疗法的患者相比。随后的III期研究,包括聚光灯和光芒(6),还报道了Zolbetuximab在CLDN18.2阳性肿瘤中对一线治疗的疗效(CLDN18.2≥2+,75%)。此外,多中心I期CT041-CG4006试验(NCT03874897)证实了针对胃肠道肿瘤的CLDN18.2特异性嵌合抗原受体(CAR)细胞的出色抗肿瘤活性(7)。因此,CLDN18.2当前被认为是最有希望的目标,尤其是对于HER2阴性微卫星稳定的GC。
报销建议
来自两个随机,双掩盖的,安慰剂对照的III期试验(聚光灯和光芒)的证据表明,Zolbetuximab添加到氟吡啶胺 - 和铂型化疗(MFOLFOX6或CAPOX)中,用于对局部先进的不可脱位或转移的成年患者的含量为flofofox6或capox) CLDN18.2阳性,从而增加了临床益处。Spotlight试验(n = 565)表明,Zolbetuximab在MFOLFOX6组合中的治疗导致统计学意义和临床上有意义的总体生存率(OS;危险比[HR] = 0.784; 95%置信区间; 95%置信区间[CI],0.644至0.644至0.954; P = 0.0075和Procesporive = 0.0075 = rsessive-freessive-freessive-freessive-freeversion-freeversiefeive(hr = rsessive-freeversie-freeverione-freeverione-freeverione free(hr); 95%CI,0.598至0.942; P = 0.0066)与安慰剂与MFOLFOX6相比。The GLOW trial (N = 507) similarly demonstrated that treatment with zolbetuximab in combination with CAPOX resulted in statistically significant and clinically important meaningful improvements in OS (HR = 0.763; 95% CI, 0.622 to 0.936; P = 0.0047) and PFS (HR = 0.687; 95% CI, 0.544 to 0.866; P = 0.0007),与安慰剂与Capox结合使用相比。在关键试验中,与单独的化学疗法相比,用Zolbetuximab与化学疗法结合使用的化学疗法治疗与恶心,呕吐和输注相关反应(IRR)的风险增加有关。但是,PERC与临床专家一致,这些不良事件(AES)在临床实践中可能是可以管理的。
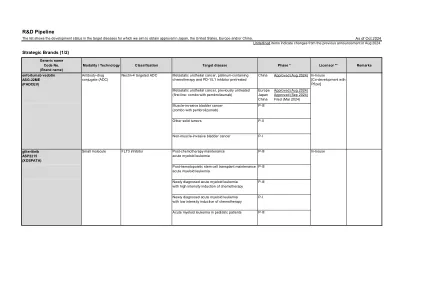
研发管线
与上一公告(2024年8月)的更新:enzalutamide:删除了2024年6月在中国批准用于转移性去势敏感性前列腺癌的描述。enfortumab vedotin:2024年8月在中国获批用于转移性尿路上皮癌,含铂化疗和PD-1/L1抑制剂预处理。2024年8月在欧洲获批用于不可切除或转移性尿路上皮癌的一线治疗(适合含铂化疗)。2024年9月在日本获批用于根治性不可切除的尿路上皮癌的一线治疗。 zolbetuximab:2024 年 10 月在美国获批,2024 年 9 月在欧洲获批,用于一线治疗局部晚期不可切除或转移性 HER2 阴性、claudin 18.2 阳性胃腺癌或胃食管连接部腺癌。avacincaptad pegol:2024 年 10 月在欧洲撤回了用于治疗继发于年龄相关性黄斑变性的地图状萎缩的申请。
勇敢的新世界 - 胃癌的新和新兴疗法
then, efforts to build on chemotherapy did not have a major impact on survival times and—with the exception of human epidermal growth factor receptor 2 (HER2)- directed treatments with trastuzumab (3) or more recently trastuzumab deruxtecan (T-DXd) (4)—clinical trials evaluating so-called targeted therapies in GC were on the whole disappointing.现在,该领域内有一种强烈的意义,这已经改变了。最著名的是Claudin 18.2和成纤维细胞生长因子受体2B(FGFR2B),其中Zolbetuximab和Bemarituzumab(5)可能在不久的将来得到批准。免疫检查点抑制剂(ICI)类药物对整个肿瘤学领域产生了巨大影响,2021年看到了GC中的第一个具有里程碑意义的研究,这些研究使ICIS成为护理标准的一部分。在这篇综述中,我们将讨论ICI类在该疾病中的影响,重点是晚期疾病环境,并讨论GC中新的和新兴的目标和治疗策略。