XiaoMi-AI文件搜索系统
World File Search System2024 IBIDI日历
“通道连接”是视黄酸诱导的羊膜源性多冰层水凝胶上神经干细胞分化的神经元网络形成的共聚焦显微镜图像。使用Tuj1(绿色)标记神经元,而核则使用带有DAPI(蓝色)的Ibidi安装培养基对其进行了反染色。使用具有10倍物镜的900公里共聚焦显微镜的Zeiss LSM获得图像。
DNA 扭转研究的光学扭矩计算和测量
摘要 角光阱 (AOT) 是一种用于测量生物分子扭转和旋转特性的强大仪器。迄今为止,AOT 对 DNA 扭转力学的研究是使用高数值孔径油浸物镜进行的,该物镜允许强捕获,但不可避免地会因玻璃-水界面而引入球面像差。然而,这些像差对扭矩测量的影响尚未通过实验完全了解,部分原因是缺乏理论指导。在这里,我们提出了一个基于有限元法的数值平台,用于计算捕获石英圆柱上的力和扭矩。我们还开发了一种新的实验方法,通过使用 DNA 分子作为距离标尺来准确确定由于球面像差导致的捕获位置偏移。我们发现计算和测量的焦移比非常一致。我们进一步确定了角陷阱刚度如何取决于陷阱高度和圆柱体与陷阱中心的位移,并发现预测和测量之间完全一致。作为对该方法的进一步验证,我们表明 DNA 固有的 DNA 扭转特性可以在不同的陷阱高度和圆柱位移下稳健地确定。因此,这项工作奠定了一个理论和实验框架,可以很容易地扩展到研究施加在具有任意形状和光学特性的粒子上的捕获力和扭矩。
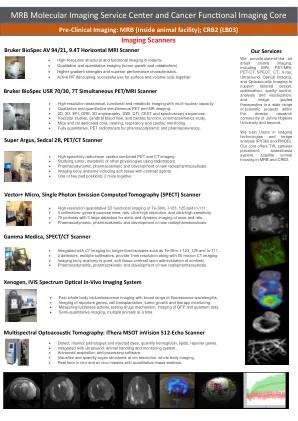
MRB分子影像服务中心及癌症功能影像核心
• 多种常规和水浸物镜,用于体内和体外成像。 • 20X 微探针,插入动物体内即可进行高分辨率荧光成像。 • 可调脉冲激光,波长范围为 690 nm 至 1040 nm,配有 3 个标准 PMT 光检测器。 • 能够检测大多数染料和荧光蛋白、DAPI、罗丹明、钙黄绿素、Fluo-3、Fluo-4。 • 产生二次谐波信号和自发荧光分子,如胶原蛋白 I 和 NADH。 • 对大脑中的神经网络、视网膜中的光感受器、癌细胞和胶原纤维进行成像。
Toolmaster TM250 - PFT Innovaltech
带远心物镜的数字 CMOS 相机探测刀尖并将实时图像传输到半透反射式 3.5 英寸 TFT 彩色显示屏。电子最大搜索功能允许刀尖旋转至最大直径(顶点)。测量过程由定位标记支持,当刀具轮廓和标线轴之间达到最佳一致性时,定位标记就会出现。因此,无需操作员参与,即可以 +/-2 微米的重复精度进行测量。测量过程非常简单,与使用轮廓投影仪没有什么不同。因此,操作员不会对测量结果产生任何影响,从而确保最高的测量可靠性。
奥沙利铂释放铂(IV)的白蛋白靶向...
图 1 CT26 细胞中白蛋白摄取的特征。(A)将细胞与 FITC 标记的白蛋白一起孵育。通过流式细胞术测定 FITC 阳性细胞(散点图,R2)和平均 FITC 荧光强度(条形图)(ex/em:488/530 nm,荧光强度标准化为自发荧光对照)。(B)通过流式细胞术测定内吞抑制剂 M b CD、CHP 和 EIPA(1 小时预处理)对 3 小时后 FITC 标记白蛋白摄取的影响。(A)和(B)中的值是三个独立实验的平均值 SD。通过单因素方差分析和 Dunnett 多重比较检验检验统计学显着性(* p < 0.05,** p < 0.01 和 *** p < 0.001)。 (C) 通过共聚焦显微镜验证了 FITC 标记白蛋白 (绿色) 的摄取和三种内吞抑制剂的影响。细胞核 (蓝色) 和膜 (红色) 分别用 DAPI 和 WGA 共染色。图像显示所有三个通道的叠加。 (D) 未经治疗的小鼠的 sc CT26 肿瘤中白蛋白含量的免疫组织化学分析 (用 20 和 63 物镜进行的显微镜检查)。细胞核和白蛋白分别用苏木精 (紫色) 和 3,3 0 -二氨基联苯胺 (棕色) 显影。 (E) 用 16.5 mg kg 1 荧光素标记的马来酰亚胺 (绿色) 治疗 CT26 小鼠。30 分钟和 5 小时后收获肿瘤,然后对细胞核 (DAPI,蓝色) 和血管 (内粘蛋白,红色) 进行免疫荧光染色。使用 40 倍物镜通过荧光显微镜进行评估。图像显示所有三个通道的叠加。使用 Definiens 软件计算每平方毫米的荧光强度(左图中的条形图)。荧光强度值以两个不同肿瘤样本的平均值 SD 表示。
ImageXpress Confocal HT.ai
与单一培养或其他 2D 细胞模型相比,复杂的 3D 细胞模型可产生更具预测性和生理相关性的结果。使用 ImageXpress Confocal HT.ai 系统,可以更快地探索这些模型的复杂性,即使在厚细胞外基质中生长的样本中也能获得更好的结果。它提供灵活的选项来满足特定的研究需求,并确保获得最佳的检测图像。使用水浸等选项可以更深入地了解 3D 细胞。水浸物镜可以将信号提高四倍,同时在深入样本成像时减少像差,从而提供更好的图像和数据质量。
CMOS 成像器微透镜优化的光学模拟
在第一部分中,我们描述了我们的方法。我们从标准微电子 CAD 软件中的像素布局描述开始,然后在光学射线追踪软件上生成三维模型。该光学模型旨在尽可能真实,同时考虑到像素所有组件的几何形状和材料的光学特性。还开发了一种特定的射线源来模拟真实条件下的像素照明(物镜后面)。在光学模拟之后,结果被传输到另一个软件以进行更方便的后处理,其中我们使用由角度响应模拟结果与测量值的拟合确定的加权表面作为感光区域。利用这个表面,我们计算基板内的射线密度以评估传感器的模拟输出信号。
薄玻璃切割中时间空气脉冲的效率
薄玻璃切割中的时间空气脉冲效率 Madalin-Stefan Radu、Cristian Sarpe、Elena Ramela Ciobotea、Bastian Zielinski、Radu Constantinescu、Thomas Baumert 和 Camilo Florian* *通讯作者电子邮件:camilo.florian@uni-kassel.de。这是以下文章的预印本:Radu、Madalin-Stefan、Sarpe、Cristian、Ciobotea、Elena Ramela、Zielinski、Bastian、Constantinescu、Radu、Baumert、Thomas 和 Florian、Camilo。 “时间艾里脉冲在薄玻璃切割中的效率” Zeitschrift für Physikalische Chemie,2024 年。最终认证和印刷版本可在线获取:https://doi.org/10.1515/zpch-2024- 0911 超短脉冲激光源是用于微和纳米加工大带隙介电材料的有用工具。这些脉冲的最大优势之一是能够达到高强度峰值,即使在对激光波长透明的材料中也能促进吸收。此外,如果修改脉冲时间分布,能量吸收可以烧蚀直径小、深度大的孔。在这项工作中,我们提出了初步结果,将三种类型的脉冲作为玻璃切割的前体:带宽受限(785 nm 时为 30 fs)、正色散和负色散时间艾里脉冲 (TAP)。所选材料为厚度为 170 μm 的钠钙玻璃,在不同激光能量和扫描速度下,以 1 kHz 的重复率在紧密(50 倍物镜)和松散(20 倍物镜)聚焦条件下进行刻划。激光加工后,使用自制的四点弯曲台通过机械应力对玻璃进行切割。我们分析了三种激光脉冲在表面和横截面上的刻划线质量以及断裂后所需的断裂力。我们报告称,与其他实施的脉冲相比,正 TAP 在玻璃样品上产生了整齐、平整的切割边缘。关键词:玻璃切割;超短脉冲激光;高纵横比结构;激光加工;时间脉冲整形;薄玻璃
测试个人脂肪阈值假设
1磁共振中心,纽卡斯尔纽卡斯尔医学科学学院转化和临床研究所,英国泰恩河畔纽卡斯尔; 2英国纽卡斯尔大学医学科学专业服务学院; 3英国纽卡斯尔大学医学科学学院衰老和活力校园的生物镜核心设施; 4美国弗吉尼亚大学弗吉尼亚大学内分泌学系; 5剑桥大学,剑桥大学289,剑桥生物医学校园,惠康信托MRC代谢科学研究所,英国剑桥; 6英国剑桥市剑桥大学NHS基金会信托基金会6沃尔夫森糖尿病和内分泌中心; 7意大利帕多瓦大学妇女和儿童健康系; 8英国牛津大学拉德克利夫医学系糖尿病试验部门,英国