XiaoMi-AI文件搜索系统
World File Search System南卡罗来纳州 - 州健康评估代谢障碍
苯基酮(PKU)高苯基血症是一种氨基酸疾病,是由于活性降低,合成障碍或苯丙氨酸羟化酶或其辅助因子的降低或回收的氨基酸疾病,BH 4。苯基酮(PKU)是由苯丙氨酸羟化酶缺乏引起的。没有这种酶,身体无法将苯丙氨酸(PHE)转化为酪氨酸(Tyr)。 苯丙氨酸在血液,尿液和中枢神经系统中积聚。 如果未经治疗,婴儿将经历深刻的智力残疾(ID)。 她或他也可以减少皮肤和头发的色素沉着,发霉的气味,异常行为和/或癫痫发作。 筛查PKU还可以鉴定出患有良性多苯基丙氨酸血症的婴儿,生物蛋白质辅因子生物合成的缺陷和生物蛋白辅助剂再生的缺陷。 Inheritance: Autosomal recessive Estimated Incidence: PKU - 1:16,000 Benign hyperphenylalaninemia (H-PHE) - unknown Defects of biopterin cofactors biosynthesis (BIOPT-BS) or regeneration (BIOPT-REG) - unknown, thought to be very rare Abnormal Screen Result: Elevated PHE Elevated PHE/TYR Method of Notification: All critical results are打电话给记录提供商。 下一步如果异常:在滤纸上尽快重复新生儿屏幕。 在已知重复结果之前,没有公式/喂养更改。 如果PHE在重复标本中仍明显升高,请参阅儿科代谢专家。 可能需要进一步的诊断评估来排除BH 4缺陷。 代谢专家将与代谢营养师协调进行PHE限制饮食。没有这种酶,身体无法将苯丙氨酸(PHE)转化为酪氨酸(Tyr)。苯丙氨酸在血液,尿液和中枢神经系统中积聚。如果未经治疗,婴儿将经历深刻的智力残疾(ID)。她或他也可以减少皮肤和头发的色素沉着,发霉的气味,异常行为和/或癫痫发作。筛查PKU还可以鉴定出患有良性多苯基丙氨酸血症的婴儿,生物蛋白质辅因子生物合成的缺陷和生物蛋白辅助剂再生的缺陷。Inheritance: Autosomal recessive Estimated Incidence: PKU - 1:16,000 Benign hyperphenylalaninemia (H-PHE) - unknown Defects of biopterin cofactors biosynthesis (BIOPT-BS) or regeneration (BIOPT-REG) - unknown, thought to be very rare Abnormal Screen Result: Elevated PHE Elevated PHE/TYR Method of Notification: All critical results are打电话给记录提供商。下一步如果异常:在滤纸上尽快重复新生儿屏幕。在已知重复结果之前,没有公式/喂养更改。如果PHE在重复标本中仍明显升高,请参阅儿科代谢专家。可能需要进一步的诊断评估来排除BH 4缺陷。代谢专家将与代谢营养师协调进行PHE限制饮食。向SC新生儿筛查计划报告所有发现。新生儿介绍:无。然而,年龄,低出生体重和/或TPN可能会影响多种氨基酸水平,包括精氨酸,蛋氨酸,苯丙氨酸,缬氨酸和亮氨酸。治疗:生物蛋白质辅因子生物合成或再生的PKU/缺陷:PHE限制饮食的生命。特殊的代谢配方可供所有SC居民(并确认诊断),目前无需任何费用。BH 4缺陷需要其他诊断评估和治疗。
2023 年苯丙酮尿症基因治疗的最新进展
图 1 苯丙酮尿症 (PKU) 是由苯丙氨酸羟化酶 (PAH) 基因的隐性遗传变异引起的(图 A)。苯丙氨酸羟化酶 (PAH) 是一种同源四聚体,可催化苯丙氨酸 (Phe) 不可逆转化为酪氨酸 (Tyr)。该反应需要还原四氢生物蝶呤 (BH 4 )、铁和分子氧作为辅因子(未显示)。在没有 PAH 活性的情况下,苯丙氨酸会在组织中积聚,并以非酶促方式脱氨基为苯丙酮酸,并进一步氧化为其他苯酮,从而得名苯丙酮尿症 (PKU)。双等位基因 PAH 变体编码变体 PAH 信使 RNA (mRNA),然后导致不稳定、活性较差或无活性的 PAH 蛋白,以及肝脏中将 Phe 羟基化为 Tyr 的能力受损。基因疗法 (图 B) 旨在通过基因添加或基于 CRISPR/Cas 的基因或碱基编辑来恢复肝脏 PAH 表达;即,几种实现此目标的不同治疗方法正在小鼠身上进行临床前研究,包括 (1) 基因添加、(2) 通过脂质纳米颗粒 (LNP) 递送治疗性 mRNA、(3) 基因编辑/校正或 (4) 基因插入。目前,基因添加最常见的尝试是通过使用重组腺相关病毒 (rAAV) 载体或非病毒 (微环) 载体将 PAH 表达盒递送到肝细胞。 rAAV 基因组渗透到肝细胞核中,主要保持游离状态,不与宿主基因组相互作用,但表达治疗性转基因。在基因校正中,有几种不同的基因或碱基编辑技术可用于将病理变异位点校正回野生型序列。其中一些编辑方法存在校正频率低的问题;所有方法都必须针对每种特定的病理变异重新设计。基因插入通过将整个 PAH 表达盒永久插入肝细胞基因组中的某个位置,产生基因添加和基因校正的组合(有关更多详细信息,请参阅文本)。
表1:氨基酸疾病 推广者(A)或社区卫生工作者(CHW)培训和... 如何审查免疫记录和德克萨斯州学校疫苗要求 表8:血红蛋白病 TVFC/ASN重新注册 负责您的健康 Texasaim Osud教师BIOS 记录疾病的历史:水痘(水痘) 新的novavax covid-19疫苗可用于订购 TVFC/ASN疫苗损失 - 报告浪费或过期... 疫苗分配和订购系统(VAO) 您可能对狂犬病不了解的8件事,但应 表1:德克萨斯州心血管疾病和中风会员的出席会议于2024年5月6日星期一举行。 unidos contra la糖尿病 负责您的健康 hep b妈妈 咨询委员会名称
可能的PKU,良性的热丙氨酸血症,辅因子生物合成或辅因子再生中生物蛋白缺损中的生物蛋白缺损。苯丙氨酸略有升高; phe/tyr抬高。在24小时内建议血浆定量氨基酸,并立即与儿科代谢专家进行电话咨询。
ACE2 抑制剂筛选检测试剂盒
图 1:检测原理说明。血管紧张素 II 肽被 ACE2 裂解后释放出 L-苯丙氨酸,可通过两步反应和荧光产物检测进行测量。荧光信号与 ACE2 活性成正比增加。注意:如需更高灵敏度的检测,请参阅 Fluoro-Verse™ ACE2 抑制剂检测试剂盒 (#78847)。背景血管紧张素转换酶 2 (ACE2) 是一种外肽酶,可催化血管紧张素 II 转化为血管紧张素 1-7 和 L-苯丙氨酸。血管紧张素 II 是经典肾素血管紧张素系统 (RAS) 的一部分,这是一种调节体液平衡、血压和维持血管张力的激素系统。ACE2 在降低血压和心血管健康方面发挥作用,因此是一个有吸引力的治疗靶点。 ACE2 也是人类呼吸道冠状病毒 NL63、SARS (SARS-CoV) 和 2019-nCoV/SARS- CoV-2 的受体。应用酶动力学和高通量筛选 (HTS) 应用中的小分子抑制剂筛选。提供的材料
引用:McGrath KC、Li X、Twigg SM、Heather AK (2020) 载脂蛋白-AI 模拟肽 D-4F 和 L-5F 可减轻 C57BL/6 小鼠的肝脏炎症并增加胰岛素敏感性。PLoS ONE 15(1): e0226931。 https://doi.org/10.1371/ journal.pone.0226931
高密度脂蛋白 (HDL) 的抗炎和抗氧化特性的发现引发了一个问题:HDL 是否可用于治疗疾病中的炎症。胰岛素抵抗主要依赖于肝脏炎症,研究表明,组成性活性肝核因子 κB (NF- κ B)(驱动炎症反应的中枢介质)会导致小鼠模型中的胰岛素抵抗状态 [ 1 ]。我们之前证明,单独(无脂质)或作为含有 PLPC 的重组 HDL(rHDL)的一部分施用载脂蛋白 A-I (apoA-I) 可预防肝脏炎症并改善高脂喂养的 C57Bl/6 小鼠的胰岛素抵抗 [ 2 ]。虽然结果令人鼓舞,但 apoA-I 颗粒的产生很大且耗时。载脂蛋白 A-I (apoA-I) 模拟肽已被开发和设计,其功能类似于全长 apoA-I,但效力更强,药代动力学特征也比全长 apoA-I 更好 [ 3 , 4 ]。这些模拟肽比 rHDL 有许多优势,包括成本相对较低、生产简单,并且能够修改其结构以允许口服给药。ApoA-I 模拟肽的特点是其苯丙氨酸残基附着,苯丙氨酸残基的增加与疏水性的增加及其与磷脂结合的能力相关 [ 4 ]。根据序列中疏水性苯丙氨酸残基的数量,研究最深入的是 4F 和 5F apoA-I 模拟肽。它们具有与 apoA-I 相同的 A 类两亲性螺旋结构 [ 5 ]。D-4F 和 L-5F 的区别在于两亲性螺旋疏水面上存在的苯丙氨酸数量,并且 D-4F 由 D-氨基酸合成,而 L-5F 由 L-氨基酸合成。对于口服给药,与 L-氨基酸相比,D-氨基酸被发现更能抵抗酶促降解。然而,吸收后,D-氨基酸不会降解,这可能导致毒性和其他副作用 [ 6 ]。L-氨基酸在循环中的毒性较小,但它们不能抵抗口服的酶促降解。两者都曾在生物学研究中使用过,据报道具有强大的抗炎和抗氧化作用 [ 7 – 12 ]。我们表明,模拟治疗显着在本研究中,我们直接测试了使用 apoAI 模拟肽 D-4F 和 L-5F 治疗是否可以改善高脂饮食 (HFD) 喂养小鼠的胰岛素敏感性,从而降低肝脏炎症。
与Ashwagandha,甜菜根
Energy 1,213 KJ (290kcal) Carbohydrates 23.9 gm Sugar 3.1 gm Dietary fibre 3.6 gm Fat 7.72 gm saturated 2.65 gm Monounsaturated 0.675 gm polyunsaturated 2.08 gm Protein 57.47 gm Tryptophan 0.929 gm Threonin 2.97 gm Isoleucine 3.025 gm leucine 4.947 gm赖氨酸3.025克蛋氨酸1.149gm Cystine 0.662gm苯丙氨酸2.777GM酪氨酸2.854gm valine 3.512 GM精氨酸4.147 gm
肌电脑炎患者和健康志愿者的色氨酸代谢物的非靶向代谢组学和定量分析:使用高分辨率质谱法
摘要:肌腱脑脊髓炎/慢性疲劳综合征(ME/CFS)是一种慢性,复杂的疾病,其特征是严重且经常使身体和精神疲劳失败。到目前为止,科学家还没有完全指出疾病的生物学原因,但它影响了全球数百万的人。为了更好地了解ME/CFS,我们将38个ME/CFS患者血浆中的代谢网络与24名健康对照参与者进行了比较。除了测量包括色氨酸及其代谢产物在内的靶向物质以及酪氨酸,苯丙氨酸,B族维生素和harbosoxanthine的测量外,这涉及一种未靶向的代谢组学方法。我们观察到几种代谢途径的显着改变,包括维生素B3,精氨酸 - 丙啉和天冬氨酸 - 天冬酰胺途径,在未靶向的分析中。与对照组相比,有针对性的分析表明,ME/CFS患者中3-羟基氰酸,3-羟基基硝酸,低黄嘌呤和苯丙氨酸的水平变化。这些发现表明ME/CFS患者的免疫系统反应和氧化应激的潜在改变。关键词:高分辨率质谱,肌电脑脊髓炎(ME/CFS),神经退行性疾病,代谢组学,靶向分析,未靶向分析,生物标志物
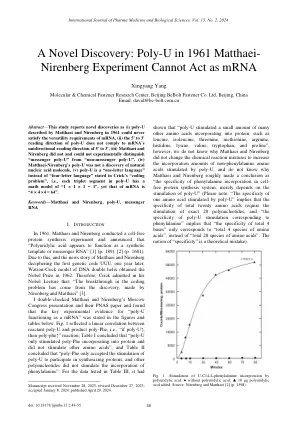
一种新颖的发现:1961年的Poly-U Matthaei-Nirenberg实验不能充当mRNA
表明,“ poly-u刺激了许多其他许多其他氨基酸纳入蛋白质,例如亮氨酸,异亮氨酸,苏胺,苏氨酸,精氨酸,精氨酸,组氨酸,赖氨酸,丝氨酸,色氨酸和脯氨酸””由poly-u刺激,也不知道为什么马特塞伊(Matthaei)和尼伦贝格(Nirenberg与苯丙氨酸相对应的聚-U刺激”意味着“总4个碱基的特异性”仅对应“总4种4种氨基酸”,而不是“总共20种氨基酸”。“特殊性”的概念是一个理论上的错误)。
通过调节肠道切除型造成的骨质疏松症的总黄酮类黄酮对减少肠道切除型造成骨质疏松的影响的综合宏基因组和代谢组分析,通过调节肠道微生物群和相关的代谢物
tfrd已在中国广泛用于治疗骨质疏松症(OP)。然而,尚未完全阐明TFRD对OP的特定分子机制。我们以前的研究也证明了TFRD可以减弱OP,临床当量剂量为67.5mg/ kg/ d是TFRD治疗的有效剂量。因此,这项研究使用67.5mg/kg作为TFRD与多磁术结合使用的剂量,以研究TFRD在OP处理中的作用机理。这项研究的目的是进一步阐明基于宏基因组和代谢组分分析的TFRD的分子机制来治疗OP。在这项研究中,使用苏木精 - 欧洲蛋白(H&E)染色,微计算机断层扫描(Micro-CT)和骨矿物质密度(BMD)分析来观察TFRD对Ovariectomized(OVX)的药理作用(OVX)。随后,进行了多组学分析,包括宏基因组学,未靶向和短链脂肪酸(SCFAS)代谢组学,以识别TFRD的抗骨质疏松机制是否与肠道微生物和相关代谢物有关。我们的结果表明,TFRD可以改善OVX大鼠小梁骨的微观和密度。17种差异物种,主要来自Akkermansia,bacteroides和phascolatcoltcontocterium Genus,OVX在SCFA中有14种相关的差分代谢产物和乙酸与TFRD相反。此外,根据未靶向的代谢组学分析的结果,发现几种代谢途径,例如苯丙氨酸代谢,苯丙氨酸,酪氨酸和色氨酸生物合成,因此可能在TFRD中起重要作用。为了进一步研究肠道微生物群和相关代谢产物之间的关系,使用了长矛人的相关分析,并表明肠道菌群(如akkermansia粘膜粘膜)可能与几种代谢物和代谢途径密切相关。