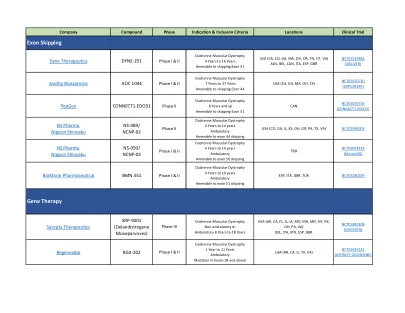
XiaoMi-AI文件搜索系统
World File Search System跳过率方法和实施指南
定义................................................................................................................. 4
在MetEx14中找到目标,跳过NSCLC
*蓝色值代表全局估计值,紫色值(在提供数据的情况下)代表亚洲人群的估计。ALK,肿瘤淋巴瘤激酶; BRAF,V-RAF鼠类肉瘤病毒癌基因同源物B; EGFR,表皮生长因子受体; HER2,人类表皮生长因子2; Kras,Kirsten Rat Sarcoma; Met,间质上皮过渡基因; NSCLC,非小细胞肺癌。1。Malapelle U等。br j癌。2024; 131:212–219; 2。Mahrous M等。cureus。2023; 15:e41992; 3。Chevallier M等。世界J Clin Oncol。2021; 12:217–237; 4。Ahn M-J等。临床肺癌。2022; 23:670–685; 5。Friedlander A等。生物标志物res。2024; 12:https://doi.org/10.1186/s40364-024-00566-0。
在学童中的自主动机,社会支持和体育锻炼:基于学校的绳索跳过体育参与的效果
结果:独立样本t检验表明,性别之间的MVPA具有统计学上的显着差异(P = 0.003 <0.05),与女孩相比,男孩在MVPA中表现出更高的参与度,相关性分析显示,几个关键变量之间存在显着的正相关。具体来说,社会支持表明与自主动机(r = 0.331,p <0.01)以及小学生在MVPA的订婚(r = 0.308,p <0.01)之间存在显着正相关。此外,自主动机与学童参与MVPA的正相关显着(r = 0.459,p <0.01)。调节分析表明,增加参与与社会支持对学童参与MVPA的相互作用产生了重大影响。
在突变小鼠品系中,基因通过跳过外显子重新启动转录和翻译,从而超越基因靶向策略
小鼠胚胎干细胞或受精卵中的基因破坏是鉴定体内基因功能的传统遗传学方法。然而,由于不同的基因破坏策略使用不同的机制来破坏基因,这些策略可能导致所得小鼠模型出现不同的表型。为了确定不同的基因破坏策略是否会影响所得突变小鼠的表型,我们对通过三种常用策略(确定性敲除 (KO) 优先和 CRISPR/Cas9)产生的 Rhbdf1 小鼠突变株进行了表征。我们发现 Rhbdf1 对不同的 KO 策略的反应不同,例如,通过跳过外显子并重新启动翻译来潜在地产生获得功能的等位基因,而不是预期的无效或严重的次等位基因。我们的分析还显示,使用 KO 优先策略产生的小鼠中至少有 4% 表现出相互冲突的表型,这表明外显子跳过是整个基因组中普遍存在的现象。此外,我们的研究强调,至少 35% 的小鼠和 45% 的人类蛋白质编码基因可能易于发生靶向 KO 优先和 CRISPR/Cas9 介导的意外翻译。我们的研究结果对基因组编辑在基础研究和临床实践中的应用具有重要意义。简介小鼠在基因上与人类密切相关,因此选择小鼠作为模型系统来破译约 20,000 个蛋白质编码基因的功能,以深入了解人类生物学和疾病。对于大规模小鼠诱变工作,通过小鼠胚胎干 (ES) 细胞中的同源重组进行基因靶向是一种有效且通用的技术。基因靶向涉及确定性无效设计(删除目标基因的整个基因组序列)或靶向敲除 (KO) 优先设计,这提供了多种优势,包括基因破坏和报告标记突变,此外,还允许以组织特异性或时间方式分析基因功能。最近,使用 CRISPR/Cas9 直接破坏受精卵中的基因已经取代了确定性无效和 KO-first 策略。为了确定不同的基因靶向策略是否会影响纯合突变小鼠的表型,我们系统地表征了由这三种 KO 策略(确定性无效、靶向 KO-first 和 CRISPR/Cas9)产生的 Rhbdf1 突变小鼠。Rhbdf1 基因编码 RHBDF1,并被认为在生长发育 [1]、炎症 [2] 和癌症 [3-5] 中起关键作用。确定性无效和靶向 KO-first 策略是强大的高通量方法,可用于 ES 细胞中的大规模基因靶向,以研究数千种哺乳动物蛋白质编码基因,从而更好地了解人类生物学和疾病 [6-8]。在使用确定性无效策略时,基于细菌人工染色体 (BAC) 的打靶载体替换靶基因的整个基因组序列 (补充图 1a),从而产生无效等位基因。相比之下,靶向 KO-first 方法 [9, 10] 是一种包括可根据所需结果选择的替代步骤的策略,具有高度的通用性,
标准处理在非小细胞肺癌中具有METEXON14跳过突变的有效性:一项现实世界研究
目的:使用METEXON14跳过突变(METEX14)的晚期非小细胞肺癌(ANSCLC)的标准疗法评估现实世界中的临床结果。方法:在肿瘤学家主导的病历回顾性综述中,对数据进行了摘要和分析,以分析2017年1月1日以后开始使用一线(1L)全身治疗的患者。结果:总共287例METEX14的ANSCLC患者,capmatinib的现实世界最佳总体反应率为73.4%(n = 146),免疫疗法(IO)单一疗法(n = 48),化学疗法为52.0%,化学疗法为52.0%(CT,N = 30)和52.0%的IO + CT(n = 63)。As compared with capmatinib, patients receiving IO (hazard ratio [HR]: 1.57; 95% CI: 0.77–3.20; p = 0.220), CT (HR: 2.41; 95% CI: 1.19–4.85; p = 0.014) and IO + CT (HR: 2.33; 95% CI: 1.35–4.04; p = 0.003) had higher进展速率。此外,接受CT的患者(HR:4.43; 95%CI:1.54–12.75; P = 0.006)和IO + CT(HR:3.53,95%CI:1.41-8.85; P = 0.007)的死亡率高于接受Capmatinib的患者的死亡率。结论:该研究表明,与1L设置的ANSCLC携带METEX14相比,与其他标准疗法相比,Capmatinib的临床结果更好。
国家健康与护理研究所
背景信息是准确的。但是,应包括以下几点以提供有关患者群体的相关信息,从而使这种情况的预后和未满足的医疗需求清楚:•与其他致癌基因驱动形式的NSCLC(例如ALK,EGFR和ROS1)的患者不同,具有METEX14 Skeex突变的患者通常是70岁或老年。大约60%的METEX14跳过突变患者是吸烟者,并且主要是女性,并且主要是非质量组织学。1-3•该节指出,晚期NSCLC患者的生存率较低(三分之一至五分之一的患者)。虽然对于整个NSCLC来说都是如此,但应注意的是,具有METEX14跳过突变的晚期NSCLC患者的预后特别差。Tong JH等人的一项大型队列研究。证明,NSCLC中METEX14跳过突变是一个独立的预后因素,与没有METEX14跳过突变的患者相比,它预测了较差的存活率。2•此外,应注意的是,包括免疫疗法在内的晚期NSCLC的当前治疗方法对于具有METEX14跳过突变的NSCLC患者并不总是有效的。在Sabari等人中。 2018,由免疫疗法治疗的NSCLC和METEX14跳过突变患者的ORR较低,反应持续时间短。 3在Sabari等人中。2018,由免疫疗法治疗的NSCLC和METEX14跳过突变患者的ORR较低,反应持续时间短。3