XiaoMi-AI文件搜索系统
World File Search SystemEM-2025-FEBR巨镜 - 分析和胚胎学-II.- ...
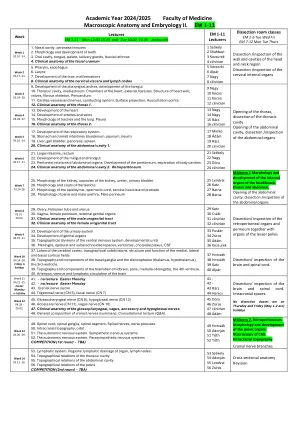
37。大脑皮层的裂片,地形细分,内侧,侧向皮质田的结构和功能38。地形和基底神经节和diencephalon(Thalamus,下丘脑)的成分,第三个心室。39。的地形和脑干的成分(中脑,PON,髓质长圆形),第四脑室。40。大脑的动脉,静脉和淋巴循环
重新利用canagliflozin靶向脑衰老
不断寻找缓慢衰老的药理和营养干预措施。热量限制(CR)是延长寿命的最深入研究的营养干预措施。抗糖尿病药物可改善葡萄糖控制,降低餐后葡萄糖水平并保持适当的葡萄糖稳态可能会增加寿命。- 葡萄糖辅助转运蛋白2抑制剂(SGLT2I)是通常用于治疗2型糖尿病(T2DM)的独特抗糖尿病药物。他们的多效性作用包括降低心血管疾病和全死亡率,这些死亡率与糖尿病无关[1]。干预措施测试计划(ITP)的最新研究表明,sglt2i和canagliflozin将雄性小鼠的中位生存率延长了14%,而雄性小鼠的延迟年龄相关病变对女性没有影响[2,3]。在最新研究中,Jayarathne等人。[4]试图在衰老过程中确定canagliflozin的神经保护特性。作者首先证明了Canagliflozin治疗改善了老年雄性小鼠中心胰岛素敏感性。长期的canagliflozin处理通过促进下丘脑和海马中的胰岛素信号传导的反应使对胰岛素的反应敏感,仅在老年遗传多样化的UM-HET3雄性小鼠中促进了胰岛素的反应。canagliflozin处理以性别特异性的方式进一步降低了MTOR信号传导,主要使老男性受益。这些发现突出了与全身性葡萄糖控制本身有关的Canagliflozin处理的保护特性。作者还证明,甘西列申素治疗显着降低了下丘脑和海马的神经炎症,并进一步改善了在老年男性而不是雌性小鼠的神经肌肉功能,运动活性和类似焦虑的行为[4]。这些研究突出了canagliflozin是衰老大脑的潜在神经保护剂。然而,尽管这些观察值具有重要意义,但与雌性动物相比,Canagliflozin的有益作用优先与男性相关,表明性二态性。从机械上讲,canagliflozin可以通过改变代谢稳态来通过改变其抗糖尿病性能来发挥其神经保护作用。同样,另一种糖尿病药物,阿卡罗糖(一种肠α-葡萄糖苷酶抑制剂)主要在雄性小鼠中延长寿命,并改善了与年龄相关的下丘脑神经炎症,主要是雄性中的下丘脑神经炎症
里昂功能基因组学研究所 (IGFL)
研究“甲状腺激素信号功能基因组学”团队的研究分为三大主题:1)了解激素影响皮质神经元成熟和功能的潜在机制;2)激素对下丘脑控制的能量代谢的影响;3)接触化学物质(特别是被怀疑会干扰甲状腺的杀虫剂)可能对神经发育造成的后果。
脂肪组织、食欲和肥胖
生长激素 (GH) 的表达和释放被认为主要受生长激素释放激素 (GHRH) 和生长抑素 (SST) 的反调节作用调节。我们实验室和其他实验室的几份报告表明,还有其他因素调节 GH 的产生,例如胰岛素样生长因子 1 (IGF-I)。我们之前使用 GH-Cre 重组酶靶向生长激素特异性 IGF-1R 敲除 (SIGFRKO) 小鼠模型,证明了 IGF-1 信号在 GH 产生的负反馈调节中的作用。然而,该模型表现出不完整的表型,表明下丘脑中存在其他调节途径。为了深入了解这一机制,我们开发了新的转基因小鼠模型,该模型保持了下丘脑-垂体 GH 轴的完整性,唯一的例外是下丘脑 GHRH 神经元和生长激素细胞均缺乏 IGF-IR,称为 GHRH-生长激素 IGF-1R 敲除 (G-SIFGRKO)。价值评估显示,直到 14 周龄,G-SIFGRKO 小鼠的线性生长正常,雄性和雌性 G-SIFGRKO 小鼠的生长速度与对照动物相比均显着降低。在 12-14 周龄进行的间接量热法评估表明,与对照组相比,G-SIFGRKO 小鼠的 O2 消耗量更高,CO2 产生量更低,并且能量消耗增加。G-SIFGRKO 小鼠的计算呼吸交换率显着降低,而移动或总活动量均未观察到变化。此外,葡萄糖和胰岛素耐受性测试表明 G-SIFGRKO 和对照组之间的葡萄糖代谢没有差异。总的来说,这些数据进一步证实了 IGF-1 信号在调节 GH 生成中的组合作用,并首次强调了一种新的 GHRH-IGF-1R 介导途径来调节身体生长和能量平衡。针对这一途径有可能更好地理解生长和代谢之间的交集以及肥胖的治疗方法。
肝脏在大鼠后HPA轴成熟和性二态性
下丘脑 - 垂体 - 肾上腺(HPA)轴的正常功能对于生存至关重要,并且为年龄,性别和上下文特定的作用编排了其发育。肝脏会影响HPA个体发育,整合了抑制或激活其发育的多种内分泌信号。本综述研究了多种内分泌系统中肝坐标产后变化中基因表达的发育变化如何促进大鼠HPA轴的成熟和性二态性。具体而言,它研究了睾丸雄激素产生的个体发育,生长增生的激素活性和下丘脑 - 垂体 - 甲状腺甲状腺轴的活性如何相交以影响肝蛋白样生长因子1的肝基因表达,类似糖皮质激素结合的球素,甲状腺素固定素 - 11-11- 11- 1和5α-还原酶类型1。这种分子变化的时机在哺乳动物物种之间有所不同,但它们在进化上是保守的,并且有望在广泛地控制稳态,尤其是在逆境中。重要的是,这些多样的内分泌系统以肝脏为Nexus,在整个产后发育过程中建立了HPA轴的基本组织,从而最终确定了成年期糖皮质激素的作用。
CRF结合蛋白在下丘脑室室中核中的活性对于泌乳大鼠的压力适应和正常的母体行为至关重要
为了确保孕产妇行为的无限制表达,需要最小化皮质激素释放因子(CRF)系统的活性。CRF结合蛋白(CRF-BP)可能对这种适应至关重要,因为它的主要功能是隔离可自由获得的CRF和尿素素1,从而抑制CRF受体(CRF-R)信号传导。到目前为止,几乎没有研究CRF-BP在母体大脑中的作用,并且在减少应力轴激活中的潜在作用尚不清楚。我们研究了下丘脑的室室核(PVN)内CRF-BP和CRF-R的基因表达。在泌乳大鼠中,与处女大鼠相比,PVOCOLULUR PVN中的CRH-BP表达明显更高,而PVN中的CRH-R1表达明显更低。急性CRF-BP在PVN中抑制CRF(6-33)在大坝中无应力的条件下增加了基底等离子体皮质酮的浓度。此外,虽然急性对CRF的急性内部输注增加了处女大鼠的皮质酮分泌,但它在媒介物(ver)中耐药的哺乳动物大鼠的效果无效,可能是由于CRF-BP的缓冲作用。的确,使用CRF的预处理(6-33)恢复了对泌乳大鼠中CRF的皮质酮反应,强调了CRF-BP在维持泌乳中衰减应激反应性中的关键作用。据我们所知,这是将下丘脑CRF-BP活性与下丘脑 - 垂体 - 肾上腺轴调节中的第一项研究。最后,慢性PVN抑制CRF-BP强烈降低了母体侵略,对母体动机和护理产生了适度的影响。在行为方面,在非压力条件下,PVN的急性CRF-BP抑制了毯子护理60分钟,在输注后90分钟舔/修饰与工具处理的大鼠相比,舔/润滑,同时增加了对入侵者的产妇侵略性。综上所述,在产后期间,CRF-BP在PVN中的完整活性对于应力轴的降低反应性以及适当的母体行为的全部表达至关重要。
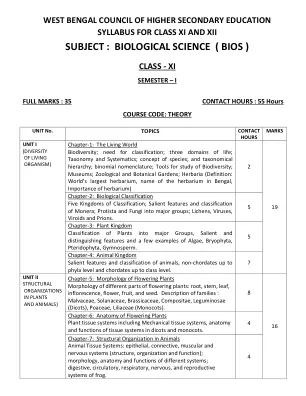
主题:生物科学(BIOS)
第11章:神经控制和协调的神经控制和协调机制;神经元和神经;人类神经系统 - 中枢神经系统;周围神经系统和内脏神经系统;大脑及其主要部分 - 脑皮质,丘脑,下丘脑和边缘系统;中脑,PON,髓质,小脑和脊髓(仅功能); P.N.S.的分布和功能模式和自主神经系统;神经冲动的产生和传导;反射动作和反射弧;感官器官 - 感官感知,概述眼睛和耳朵的结构和功能;疾病 - 帕金森氏症和阿尔茨海默氏病。
雌雄主导和从属慈鲷鱼的执行功能和大脑形态
图 2 大脑形态。(a)为计算大脑区域体积而准备的椭圆体大脑图像:T,端脑;OT:视顶盖;Cb:小脑;Hy,下丘脑;Bs,脑干;W,宽度;H,高度;L,长度。(b)对数转换和标准化身体尺寸 (SL) 的对数转换大脑测量值的回归线和 95% 置信区间 (N = 43)。(c)从统计模型中提取的估计值和 95% 置信区间,作为社会地位和性别的函数,并根据身体尺寸 (SL) 进行校正。*p < .05。
GHRH 与糖尿病和代谢
摘要尽管胰岛素疗法已存在一个多世纪,血糖监测也取得了进展,但糖尿病及其并发症仍然是一个沉重的负担。目前的药物治疗不持久,治疗结束后症状经常复发,而且不同患者的反应也不同。此外,许多药物的有效性会随着时间的推移而减弱,这凸显了对替代疗法的需求。维持 β 细胞质量和促进 β 细胞再生提供了更可治愈的治疗方法,而如果无法再生,细胞替代疗法可能是一种选择。对于这两种策略,提高 β 细胞存活率都至关重要。生长激素释放激素 (GHRH) 最初被发现是因为它能够刺激垂体产生和释放生长激素 (GH)。除下丘脑外,GHRH 还在外周组织中产生,其受体 GHRHR 在垂体、胰腺、脂肪组织、肠道和肝脏等组织中表达。多项研究表明,GHRH 及其类似物可增强体外和动物模型中产生胰岛素的胰腺 β 细胞的存活率。这些有益作用有力地支持了 GHRH 激动剂和拮抗剂在临床治疗人类代谢疾病或增强用于移植的细胞中 β 细胞存活率方面的潜力。在本综述中,我们将讨论下丘脑和下丘脑外 GHRH 在生理和病理背景下的代谢中的作用,以及其潜在机制。此外,我们还将讨论 GHRH 类似物对治疗代谢疾病的潜在有益作用。