XiaoMi-AI文件搜索系统
World File Search SystemACS:与内皮功能障碍和基础交感神经活动增高的关系
急性冠状动脉综合征 (ACS) 的特点是,在先前无症状的个体中,通常在 24 小时内迅速出现不稳定性心绞痛 (USA)、ST 段抬高型心肌梗死 (STEMI) 或非 ST 段抬高型心肌梗死 (Non-STEMI) 的症状或表现。这是由于心脏血流突然减少所致 [1]。内皮功能障碍在 ACS 的发病机制中起着至关重要的作用 [2]。健康的内皮对于预防血栓形成至关重要,因为它具有抗血栓、抗血小板和促纤溶特性,同时还能根据需要维持血管张力 [3]。内皮功能障碍的特点是内皮失去这些保护功能。相反,它会促进血栓形成状态、血小板聚集和动脉粥样硬化斑块的形成,尤其是在有高血压、糖尿病和吸烟等风险因素的个体中 [3- 7,8]。
内皮细胞 Slit2 在心脏发育过程中引导 Robo1 阳性交感神经支配
。CC-BY 4.0 国际许可证永久有效。它以预印本形式提供(未经同行评审认证),作者/资助者已授予 bioRxiv 许可,可以在该版本中显示预印本。版权所有者于 2025 年 1 月 22 日发布了此版本。;https://doi.org/10.1101/2025.01.22.634222 doi:bioRxiv 预印本
含咖啡因的咀嚼口香糖可改善交感神经活动并模拟
随机跨界双盲研究设计。经过三天的饮食控制,参与者在试验当天的下午到达实验室,以安静的状态收集唾液样本,并配备了心率监测器。参与者以3 mg/kg的体重(CAF试验)咀嚼含咖啡因的口香糖或含含咖啡因(PL试验)的安慰剂的参与者10分钟,然后将其吐出。参与者然后接受了15分钟的动态热身。在热身结束时,参与者进行了2轮特定于摔跤的模拟比赛,并记录了模拟比赛中的跌倒数量。模拟匹配后,再次从参与者那里收集唾液样本。分析唾液样品的咖啡因α-淀粉酶浓度。两个试验之间的差异
手稿ID:ZUMJ-2409-3599 doi:10.21608/ZUMJ.2024.323682.3599评论文章寄生虫交感神经多动症:临床特征,识别
抽象背景:在患有严重创伤性脑损伤的个体中,阵发性交感神经多动症发作(也称为自主风暴)并不罕见。发烧,心动过速,高血压,呼吸症,多汗症和肌张力姿势是它们的一些显着特征。这些情节可以自行开始或被刺激带来。尽管它们的发病机理尚不清楚,但它们的症状无疑表明激活或抑制交汇区域。这些咒语经常被误认为是癫痫发作,从而导致不必要的抗癫痫药物治疗。足够的水合,排除模仿疾病(感染,肺栓塞,脑积水,癫痫),提供有效的镇痛药,并避免触发时避免触发因素,是管理偏离性交感神经多余的一般准则。最有益的药理药物是硫酸吗啡和非选择性β受体阻滞剂,例如普萘洛尔。处理难治性实例时,鞘内巴氯芬可能是有用的。尽管它们的有效性较不恒定,但溴o不般的和可乐定对某些患者可能是有益的。结论:PSH是一个很常见的,但通常忽略了急性弥漫性或多灶性脑疾病的并发症。最常见的是遭受严重创伤性脑损伤的年轻,无意识的人。反复发作,心动过速,呼吸症,高血压,汗水以及偶尔发烧和肌张力的姿势的突然发作是病情的标志。有临床诊断。减少可能引起发作并引发预防和流产药物的任何外部刺激(例如静脉注射吗啡,加巴喷丁,普萘洛尔和可乐定)也是治疗的一部分。早期和足够的PSH治疗可能会降低随后问题的风险,例如肌肉染色,营养不良和脱水。关键字:阵发性交感神经多动症,创伤性脑损伤,重症监护病房
心脏交感神经元是在遗传确定的心律失常性心肌病
摘要心律失常性心肌病(AC)是一种家族性心脏病,主要是由年轻人和运动员中的大多数与压力相关的心律失常猝死造成的突变,这是大多数与压力相关的心律失常猝死。ac心脏显示纤维脂肪损伤,产生心律不齐并引起收缩功能障碍。身体/情绪压力与心律不齐之间的相关性支持交感神经元(SNS)参与该疾病,但这先前尚未得到证实。在这里,我们结合了分子,体外和离体分析,以确定AC连接的DSG2下调在SN生物学上的作用,并评估Desmoglein-2突变体(DSG2 MUT/MUT)小鼠中心脏交感神经神经支配。分子测定法表明SNS表达DSG2,这表明DSG2携带的载体会含有SNS中的突变蛋白。共焦
皮层内脑-心脏相互作用:交感迷走神经变化的 EEG 模型源研究
希望,H.(2010)。 Holm 的顺序 Bonferroni 程序。 Antonacci , Y.、Barà , C.、Zaccaro , A.、Ferri , F.、Pernice , R. 和 Faes , L. (2023)。时变信息测量:应用于脑心相互作用的信息存储的自适应估计。网络生理学前沿,3,1242505。Asadzadeh, S., Rezaii, T., Beheshti, S., Delpak, A., & Meshgini, S. (2020)。系统评价卵源定位技术及其在脑异常诊断中的应用。神经科学方法杂志,339,108740。Averta, G.、Barontini, F.、Catrambone, S.、Haddadin, G.、Held, JP、Hu, T.、Jakubowitz, E.、Kanzler, CM、Kühn, J.、Lambarcy, O.、Leo, A.、Obermeier, E. 和 Ricciardi, E. (1999)。.、Schwarz, A.、Valenza, G.、Bicchi, A. 和 Bianchi, M. (2021)。 U-limb:关于健康和中风后手臂运动控制的多模式、多中心数据库。 GigaScience,10(6),giab043。 Babo-Rebelo、M.、Wolpert、N.、Adam、C.、Hasboun、D. 和 Tallon-Baudry、C. (2016)。心脏监测功能是否与默认网络和右前岛叶中的自我相关?伦敦皇家学会哲学学报。 B 系列,生物科学,371 (1708),20160004。Bagur, S., Lefort, J. M., Lacroix, M. M., de Lavilléon, G., Herry, C., Chouvaeff, M., Billand, C., Geoffroy, H., & Benchenane, K. (2021)。呼吸驱动的前额叶振荡可以独立于启动而调节由条件性恐惧引起的冻结的维持。自然通讯, 12(1), 2605. Barà, C., Zaccaro, A., Antonacci, Y., Dalla Riva, M., Busacca, A., Ferri, F., Faes, L., & Pernice, R. (2023)。用于评估心跳引起的皮质反应的信息存储的局部和整体测量。生物医学信号处理和控制,86,105315。Benarroch,EE(1993)。中央自主神经网络:功能组织、功能障碍和观点。在《梅奥诊所学报》(第 68 卷,第 988-1001 页)。爱思唯尔。 Benarroch,EE(2012)。中枢自主神经控制。在自主神经系统入门书中(第 9 - 12 页)。爱思唯尔。 Candia-Rivera,D.(2023 年)。根据庞加莱图得出的交感神经-迷走神经活动测量值来模拟大脑-心脏的相互作用。方法X、10、102116。Candia-Rivera, D.、Catrambone, V.、Barbieri, R. 和 Valenza, G. (2022)。双向皮质和周围神经控制对心跳动力学的功能评估:热应力的脑心研究。神经图像, 251, 119023。Candia-Rivera, D., Catrambone, V., Thayer, J. F., Gentili, C., & Valenza, G. (2022)。心脏交感迷走神经活动引发大脑 - 身体对情绪唤起的功能性反应。美国国家科学院院刊,119(21),e2119599119。 Candia-Rivera、D.、Catrambone、V. 和 Valenza、G. (2021 年)。脑电图电参考在评估脑-心功能相互作用中的作用:从方法论到用户指南。《神经科学方法杂志》,360,109269。Candia-Rivera, D.、Norouzi, K.、Ramsøy, TZ 和 Valenza, G. (2023)。精神压力下上升式心脑通讯的动态波动。《美国生理学-调节、整合和比较生理学杂志》,324 (4),R513 – R525。Catrambone, V.、Averta, G.、Bianchi, M. 和 Valenza, G. (2021)。走向脑-心计算机接口:使用多系统方向估计对上肢运动进行分类的研究。神经工程杂志,18 (4),046002。Catrambone, V.、Greco, A.、Vanello, N.、Scilingo, EP 和 Valenza, G. (2019)。通过合成数据生成模型进行时间分辨的定向脑-心脏相互作用测量。生物医学工程年鉴,47,1479 – 1489。Catrambone, V.、Talebi, A.、Barbieri, R. 和 Valenza, G. (2021)。时间分辨的脑-心脏概率信息传递估计
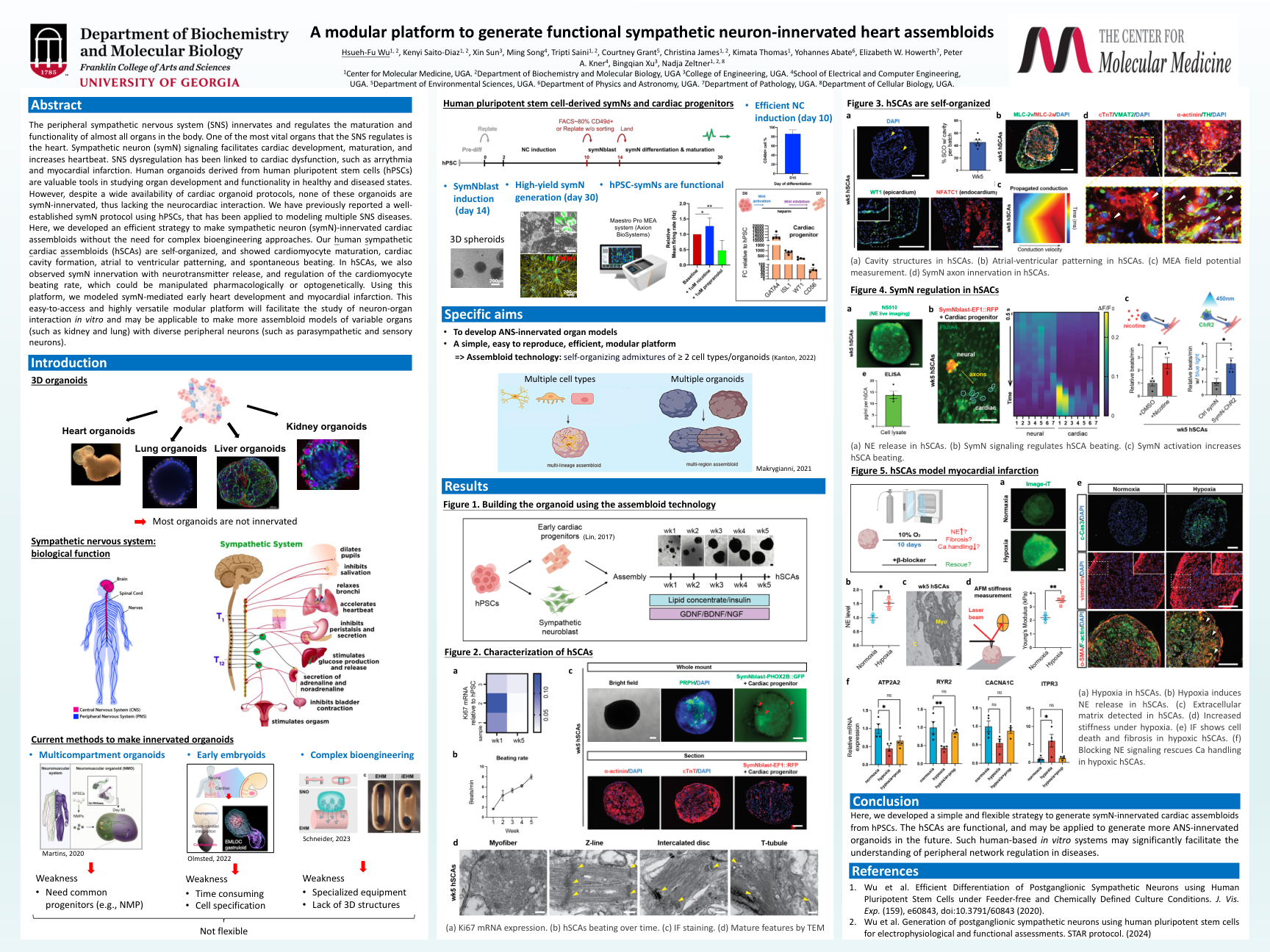
用于生成功能性交感神经元支配的心脏聚集体的模块化平台
外周交感神经系统 (SNS) 支配并调节体内几乎所有器官的成熟和功能。SNS 调节的最重要器官之一是心脏。交感神经元 (symN) 信号传导促进心脏发育、成熟并增加心跳。SNS 失调与心脏功能障碍有关,例如心律失常和心肌梗死。源自人类多能干细胞 (hPSC) 的人类类器官是研究健康和患病状态下器官发育和功能的宝贵工具。然而,尽管心脏类器官方案广泛可用,但这些类器官均不受 symN 支配,因此缺乏神经心脏相互作用。我们之前曾报道过一种使用 hPSC 的完善的 symN 方案,该方案已应用于模拟多种 SNS 疾病。在这里,我们开发了一种有效的策略来制造交感神经元 (symN) 支配的心脏组装体,而无需复杂的生物工程方法。我们的人类交感神经心脏组装体 (hSCA) 是自组织的,并表现出心肌细胞成熟、心腔形成、心房到心室模式和自发跳动。在 hSCA 中,我们还观察到 symN 神经支配与神经递质释放,以及心肌细胞跳动率的调节,这些可以通过药理学或光遗传学进行操纵。利用这个平台,我们模拟了 symN 介导的早期心脏发育和心肌梗死。这个易于访问且用途广泛的模块化平台将促进体外神经元-器官相互作用的研究,并可能适用于制作更多具有各种周围神经元(如副交感神经元和感觉神经元)的不同器官(如肾脏和肺)的组装体模型。
6.01.56心力衰竭患者的心肌交感神经神经成像原始政策日期:2016年1月1日生效日期:11月1日,20
调节状态在2008年,Adreview®(Iobenguane I 123)注射(GE Healthcare)通过美国食品和药物管理局(FDA)新药申请过程(22-290)批准,用于检测原发性或转移性细胞瘤或神经细胞瘤或神经细胞瘤或神经细胞瘤作为辅助测试。5, The FDA (2013) approved a supplemental new drug application (22-290/S-001) for AdreView and expanded the labeled indication to include scintigraphic assessment of sympathetic innervation of the myocardium by measurement of the H/M ratio of radioactivity uptake in patients with New York Heart Association (NYHA) class II or class III heart failure and LVEF less than 35%.6,理由背景心力衰竭估计在美国有620万成年人患有心力衰竭。在2018年,根据2022年心脏和中风统计更新的数据,在2018年的379,800次死亡证明中提到了心力衰竭,六分之一的心力衰竭和射血分数减少在诊断的18个月内导致疾病恶化恶化,这些人更有可能是黑人,> 80岁,> 80岁,> 80岁,> 80岁,> 80岁,合并症率提高了。2,黑人个体在未来发展心力衰竭的风险最高,其次是西班牙裔,白人和美国人,反映了这些人群中高血压,糖尿病和社会经济地位的发生率的差异。黑人个体在未持有心肌梗塞之前的入射心力衰竭的比例最高(75%)。心力衰竭的根本原因包括冠状动脉疾病,高血压,瓣膜疾病和原发性心肌病。These conditions reduce myocardial pump function and decrease left ventricular ejection fraction (LVEF).一种补偿这种降低心肌功能的早期机制是激活交感神经系统。最初增加的交感神经活动有助于通过增加心率和心肌收缩力来补偿心力衰竭,以维持血压和器官灌注。但是,随着时间的流逝,这会给心肌增加额外的压力,增加冠状动脉灌注要求,从而导致缺血性心脏病和/或心肌损伤恶化。作为弥补心肌功能降低的心脏的能力,会导致心力衰竭的临床症状。增强的交感神经活动的另一种有害作用是增加对潜在致命性心律不齐的敏感性。与心力衰竭相关的过度活跃的交感神经涉及心脏交感神经系统的主要神经递质的神经元释放增加。响应交感神经刺激,含有NE的囊泡被释放到神经元突触裂口中。释放的NE与突触后β1,β2和α受体结合,增强了腺基环化酶活性,并带来了所需的心脏刺激作用。去甲肾上腺素被带回储存或分解代谢处置的突触前空间,终止了摄取-1途径的突触反应。NE的释放增加通常伴随着NE的再摄取减少,从而进一步增加了NE水平。诊断成像鸟嘌呤是一种假神经递质,是NE的类似物。它也被摄取-1途径所采用。碘123个二苯甲酰瓜甘油(123 I-MIBG或MIBG)是用放射性碘标记的化学修饰的鸟嘌呤。碘123元碘苯甲烷基鸟氨酸移入突触裂缝中,然后以类似于NE的方式将其置于突触前神经空间中。但是,与NE不同,MIBG未被分解代谢,因此将其集中在心肌交感神经末端。可以使用常规的伽马摄像机对此集中的MIBG进行成像。3,注射后几个小时内MIBG的浓度是交感神经活性的反映,这反过来又可能与心力衰竭的严重程度相关。
人机协作中的社交感知
人工智能 (AI) 的进步预示着未来的团队将由人类和智能机器(如机器人或虚拟代理)组成。为了使人机协作团队 (HAT) 取得成功,人类团队成员需要接受他们的新 AI 同伴。在本研究中,我们借鉴了人类新人接受度的三部分模型,该模型包括三个部分:反思、知识利用和心理接受。我们假设社会感知的两个方面——热情和能力——是人类接受新 AI 队友的关键预测因素。研究 1 使用视频短片设计,参与者想象将八个 AI 队友中的一位添加到参考团队中。研究 2 在实验室团队中利用了绿野仙踪方法。除了测试感知温暖和能力对接受性成分的影响外,研究 2 还探讨了接受性成分对感知 HAT 可行性的影响。虽然两项研究都发现感知温暖和能力会影响接受性,但我们发现能力对于知识利用和心理接受尤为重要。此外,研究 2 的结果表明,心理接受与感知 HAT 可行性呈正相关。讨论了对未来 AI 队友社会认知研究的启示。
糖尿病中的肾交感性多动症是通过无途径的5-HT1D受体激活调节的
摘要:由交感纤维高度支配的肾脏脉管系统有助于心脏血管稳态。这种肾交感神经流在正常血糖大鼠中被5-HT抑制。考虑到糖尿病会诱导心血管并发症,我们旨在确定糖尿病状态是否在肾脏水平上修改了甲肾上腺素能的输入及其在大鼠中的血清素能调节。Alloxan糖尿病大鼠被麻醉(Pentobarbital; 60 mg/kg I.P.)并准备左肾脏的原位自动灌注,以连续测量系统性血压(SBP),心率(HR)和肾脏灌注压力(RPP)。对肾交感神经流的电刺激在RPP中诱导频率依赖性增加(∆)(分别为23.9±2.1、59.5±1.9和80.5±3.5 mm Hg,分别为2、4和6 Hz时),在没有修改HR或SBP的情况下,它们高于正态capecialgemic Rats中的频率。5-HT和5-CT(5-HT 1/5/7激动剂)的液内推注会减少电诱导的∆ RPP。仅L-694,247(5-HT 1D激动剂)对交感神经诱导的血管收缩进行了5-CT抑制作用,而它没有改变外源性去甲肾上腺素诱导的∆ RPP。5-CT抑制仅被静脉注册废除推注。Guanylyl环酶的抑制剂ODQ(i.v.),完全逆转了L-694,247抑制作用。总而言之,糖尿病在肾脏水平上引起交感神经诱导的加压反应的增强。良好的5-HT 1D受体抑制糖尿病大鼠甲肾上腺素能诱导的血管收缩。