XiaoMi-AI文件搜索系统
World File Search System为什么电力市场模型产生不同的结果
欧洲电力行业是世界上最大的上限和贸易计划的主要部门,是碳定价最受研究的例子之一。特别是,数值模型通常用于研究碳价格和排放的未来不确定的未来发展。通常通过灵敏度分析来解决参数不确定性,但从现有的单模研究中尚不清楚模型本身的潜在不确定性。在这里,我们通过运行一个结构化模型比较实验来研究这种与模型相关的不确定性,在该实验中,我们将五个数值功率部门模型暴露于对齐的输入参数中,从而结合了Stark模型差异。以2030年的碳价格为27欧元,这些模型估计,与2016年相比,欧洲电力部门的排放量将减少36-57%。大多数这种变化可以通过模型考虑煤炭和褐煤发电厂的退役的程度来解释。更高的碳价格为57欧元和87欧元的碳价格分别降低了45-75%和52-80%。这些范围的下端可以归因于仅分配模型捕获的短期燃油开关。较高的减少量对应于其他考虑对可再生能源的基于市场投资的模型。通过进一步研究以高碳价格的剩余排放中的跨模型变化,我们将联合热量和功率的表示形式确定为模型结果之间差异的另一个至关重要的驱动力。
人类少突胶质细胞的快速有效产生髓生成人类皮质神经元
(未通过同行评审认证)是作者/资助者。保留所有权利。未经许可就不允许重复使用。此预印本版的版权持有人于2025年3月1日发布。 https://doi.org/10.1101/2025.02.28.640804 doi:biorxiv preprint
研究人员意识到有效产生高级...
早在2016年,USTC的研究人员实验表明,非局部性可以通过单粒子的情境性通过两粒子相关性产生,这些相关性不会违反任何贝尔的不平等,并产生了三维纠缠。在2020年,分别实现了通过11 km纤维的高维纠缠的32维量子纠缠和有效的分布,以奠定可伸缩量子网络的坚实基础。
2025; 15(8):3610-3626。 doi:10.7150/thno.105069研究论文白介素35产生的B细胞通过分泌外ososom
背景:同种异体造血干细胞移植(Allo-HSCT)是用于侵袭性血液学恶性肿瘤的有效治疗方法。但是,患上移植物抗宿主病(GVHD)的风险是Allo-HSCT的重大障碍。GVHD是一种使人衰弱的状况,具有高死亡率,当前的GVHD治疗选择受到限制,皮质类固醇是标准治疗方法。然而,类固醇的不良影响使长时间使用变得困难,因此需要开发更安全的疗法。IL-35产生的B细胞(I35-BREGS)已成为自身免疫性疾病期间免疫的关键调节剂。在这项研究中,我们研究了I35-BREGS免疫疗法是否可以抑制和减轻GVHD。方法:我们对经历了同种HSCT的小鼠进行了单一剂量的I35-BREG(1.5×10 6),并在转移后90天内监测了GVHD小鼠的疾病严重程度以及GVHD小鼠的存活。我们发现i35-bregs分泌含有膜结合的IL-35(I35-外观)的外泌体,并研究了是否可以将EX-VIVO产生的i35-外病体用作GVHD的独立免疫疗法。I35-BREG诱导的细胞因子或检查点蛋白(PD-1,LAG-3,CTLA-4)的表达。通过接近连接测定法(PLA),免疫组织化学/共聚焦显微镜和α倍折叠式培物建模的表征是通过接近连接测定法(PLA)的表征。与IL-35是分泌的细胞因子的观点相反,我们在这里表明i35-bregs通过膜结合的IL-35减轻GVHD,并通过分泌i35-效果。结果:单剂量为1.5×10 6 I35-BREG降低了GVHD的严重程度和延长的GVHD存活率,超过70%的I35-BREG处理的小鼠在转移后第90天超过第90天,同时观察到在第90天,同时观察到100%的死亡率,在未经培训的小鼠中,由45日在未经培养的小鼠中。此外,i35-BREGS或EX-VIVO产生的i35-陈述诱导同种反应性的T细胞,以上调与T细胞疲劳和厌食的检查点蛋白质,并抑制同种反应性反应,并抑制抑制GVHD的感染性耐受性机制。重要的是,I35-BREGS或I35-诊断物通过增加涂有免疫抑制i35-示例的旁观者淋巴细胞来抑制GVHD。结论:这项研究表明,I35-BREG和I35-诊断在缓解GVHD中起着至关重要的作用。I35-BREG和I35-异型体免疫疗法的结合可能是治疗GVHD和其他炎症性疾病的有效策略。
水文历史和洪水脉冲控制铁和硫代谢成分,与沿海湿地中库群岛实验中的温室气体产生相关性
。cc-by-nc-nd 4.0国际许可证(未经同行评审证明)获得的是作者/资助者,他授予Biorxiv授予Biorxiv的许可,以永久显示预印本。这是该版本的版权持有人,该版本发布于2025年3月5日。 https://doi.org/10.1101/2025.03.03.03.641170 doi:Biorxiv Preprint
产生的蛋白质激活天然杀伤细胞
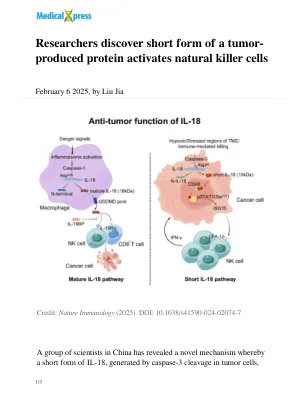
在这项研究中,研究人员专注于IL-18。他们发现肿瘤细胞可以通过caspase-3裂解产生新型的IL-18形式,该裂解与传统的成熟IL-18途径无关。与成熟的IL-18不同,这种短形式不会退出细胞,而是进入细胞核,在该细胞核中促进了STAT1和ISG15分泌的磷酸化,从而增强了NK细胞抗肿瘤功能。