XiaoMi-AI文件搜索系统
World File Search System丘脑底核神经元局部场诱发电位中深部脑刺激伪影的噪声消除
本研究介绍了一种噪声消除技术,用于 MER 机器通过丘脑底核深部脑刺激/或刺激器 (STN-DBS) 在局部场电位 (LFP) 中进行电刺激获取的丘脑底核 (STN) 神经元微电极信号。我们提出了一种新方法,用于消除由不同于典型 LFP (低频电位) 信号的脉冲发生器触发的诱导刺激伪影。该方法经过处理和准确性测试,并计算用于体外状态的执行。结果表明,该方法可以很好地抑制刺激伪影。并且还在帕金森病 (PD) 受试者 (患者) 的体内状态下进行了测试。它用于处理从 PD 手术中收集的 LFP 信号,以初步探索 STN、DBS 参数 (刺激强度、刺激电压、频率和幅度脉冲宽度) 内 beta 波段同步变化的定量依赖性。研究结果表明,DBS 过程可以克服过度的β频率(30Hz)活动,并且随着 DBS 电流在 1-3V 范围内增加,刺激频率在 60-120Hz 范围内增加,减少程度也随之增加。该方法为探索诱导电刺激对帕金森脑活动的即时效果提供了科学研究和技术支持,并可作为未来技术的研究工具。
运动引起的伪影在评估HR-PQCT扫描中的影响:观察者间和内部变异性的评估
建立的用于诊断肩cap骨骨折的成像方法是X射线,骨扫描,磁共振成像(MRI)和计算机断层扫描(CT),MRI是裂缝检测最敏感和最具体的方法。CT也具有很高的特异性,但灵敏度较低。但是,它通常比MRI更优于MRI,因为它更便宜且更容易获得(1,4,5)。高分辨率外围定量计算机断层扫描(HR-PQCT)代表检测scaphoid骨折的创新选择(6-8)。由于第一个结果直到最近才发布,因此在该领域尚未广泛建立其使用。最初,HR-PQCT旨在测量骨密度并量化骨骼的三维微构造(9)。由于几个原因,包括技术问题,扫描获取和评估缺乏标准化以及与成本相关的有限可用性,其临床价值仍处于边缘状态(10)。然而,近年来,HR-PQCT在许多科学领域都取得了重大进展,例如,在评估流变学疾病对关节表面的影响(11,12)(11,12),骨骼微体系结构和骨骼强度对次生骨质骨的骨骼和代谢性骨骼的影响(10),以及对骨骼的影响(10)的作用,以及对骨骼的效果,以及对骨骼的效果(均具有抗抗病性的作用)(均具有抗抗病性的作用(愈合(14-16)和远端半径裂缝机制的研究(17,18)。
用压电纤维担架中的傅里叶域光学相干断层扫描中的伪影
收到2007年9月26日; 2008年2月15日修订; 2008年2月18日接受;发表于2008年3月4日(文档ID 87957);发表于2008年3月31日,我们描述了一种扫描源源式光学相干断层扫描(OCT)系统,该系统启动了高速全速成像。我们实施了一个压电纤维担架,以在连续的A扫描之间产生定期的相移,从而引入了横向调制。然后,通过在轴向方向处理数据之前,在横向方向上执行傅立叶过滤来解决深度歧义。DC工件也被删除。关键因素是压电纤维担架可用于以高重复速率生成离散的相移。提出的实验设置是先前报道的B-M模式扫描光谱域OCT的一个改进版本,因为它不会产生其他伪像。这是一个简单且低成本的解决方案,可轻松应用伪影。©2008美国光学协会OCIS代码:110.4500,170.4500,100.5070。
研究论文 用于生物医学设备的具有伪影抑制功能的神经记录和刺激芯片
神经假体系统包括神经/肌肉刺激器和神经记录电路。该系统中的这些刺激器和记录器几十年来广泛应用于许多医学领域,如人工耳蜗/视网膜假体、细胞激活和心脏起搏器[1–5]。功能上,神经刺激用于激活假体,唤醒感觉功能[6],而神经记录可以感知神经信号或完成刺激效果的评估[7–9]。将神经刺激器和神经记录器结合起来,形成闭环控制的同步神经记录和刺激系统,以恢复受伤个体的基本功能[10–16],例如用于癫痫发作检测和抑制的系统[17,18]。如图1所示,在用于癫痫发作检测和抑制的闭环神经记录和刺激系统中,神经记录用于检测脑内的癫痫信号,电刺激用于
训练小波域损失的训练生成图像超分辨率模型可以更好地控制伪影
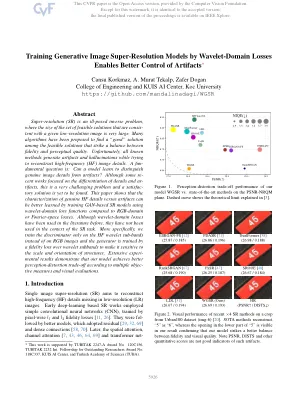
抽象的超分辨率(SR)是一个不当的反问题,其中具有给定低分辨率图像的可行解决方案集的大小非常大。已经提出了许多算法,以在可行的解决方案中找到一种“好”解决方案,这些解决方案在忠诚度和感知质量之间取得了平衡。不幸的是,所有已知方法都会生成伪影和幻觉,同时试图重建高频(HF)图像细节。一个有趣的问题是:模型可以学会将真实图像细节与文物区分开吗?尽管有些重点侧重于细节和影响的分化,但这是一个非常具有挑战性的问题,并且尚待找到满意的解决方案。本文表明,与RGB域或傅立叶空间损耗相比,使用小波域损失功能训练基于GAN的SR模型可以更好地学习真正的HF细节与伪像的表征。尽管以前在文献中已经使用了小波域损失,但在SR任务的背景下没有使用它们。更具体地说,我们仅在HF小波子带上而不是在RGB图像上训练鉴别器,并且发电机受到小波子带的忠诚度损失的训练,以使其对结构的规模和方向敏感。广泛的实验结果表明,我们的模型根据多种措施和视觉评估实现了更好的感知延续权权衡。
通过添加 EMG 源 (ERASE) 去除肌电图 (EMG) - 一种基于 ICA 的新型算法,用于从 EEG 中去除肌电伪影 - 第 1 部分
摘要。脑电图 (EEG) 记录经常受到肌电图 (EMG) 伪影的污染,尤其是在运动过程中记录时。现有的去除 EMG 伪影的方法包括独立成分分析 (ICA) 和其他高阶统计方法。然而,这些方法不能有效地去除大多数 EMG 伪影。在这里,我们提出了一种改进的 ICA 模型来去除 EEG 中的 EMG 伪影,称为通过添加 EMG 源去除 EMG (ERASE)。在这种新方法中,将来自颈部和头部肌肉的真实 EMG 的额外通道(参考伪影)作为 ICA 的输入添加,以便将 EMG 伪影的大部分功率“强制”到几个独立成分 (IC) 中。使用自动程序识别和拒绝包含 EMG 伪影的 IC(“伪影 IC”)。首先使用模拟和实验记录的 EEG 和 EMG 验证 ERASE。仿真结果表明,ERASE 从 EEG 中去除 EMG 伪影的效果显著优于传统 ICA。此外,它的假阳性率低,灵敏度高。随后,研究人员收集了 8 名健康参与者移动双手时的 EEG 数据,以测试该方法的实际效果。结果表明,ERASE 成功去除了 EMG 伪影(使用真实 EMG 作为参考伪影时,平均可去除约 75% 的 EMG 伪影),同时保留了与运动相关的预期 EEG 特征。我们还使用模拟 EMG 作为参考伪影测试了 ERASE 程序(约 63% 的 EMG 伪影被去除)。与传统 ICA 相比,ERASE 从 EEG 中去除的 EMG 伪影平均多 26%。这些发现表明,ERASE 可以显著分离 EEG 信号和 EMG 伪影,而不会丢失底层 EEG 特征。这些结果表明,使用额外的真实或模拟 EMG 源可以提高 ICA 在去除 EMG 伪影方面的有效性。
通过添加 EMG 源 (ERASE) 去除肌电图 (EMG) — 一种基于 ICA 的新型算法,用于从 EEG 中去除肌电伪影
脑电图 (EEG) 记录经常会受到肌电图 (EMG) 伪影的污染,尤其是在运动期间记录时。现有的去除 EMG 伪影的方法包括独立成分分析 (ICA) 和其他高阶统计方法。然而,这些方法不能有效去除大多数 EMG 伪影。在这里,我们提出了一种改进的 ICA 模型来去除 EEG 中的 EMG 伪影,这称为通过添加 EMG 源去除 EMG (ERASE)。在这种新方法中,来自颈部和头部肌肉的真实 EMG 的额外通道(参考伪影)被添加作为 ICA 的输入,以便将 EMG 伪影的大部分功率“强制”到几个独立成分 (IC) 中。使用自动程序识别和拒绝包含 EMG 伪影的 IC(“伪影 IC”)。首先使用模拟和实验记录的 EEG 和 EMG 验证 ERASE。模拟结果表明,ERASE 比传统 ICA 更有效地从 EEG 中去除 EMG 伪影。此外,它的假阳性率低,灵敏度高。随后,在 8 名健康参与者移动双手时收集了他们的 EEG,以测试该方法的实际效果。结果表明,ERASE 成功去除了 EMG 伪影(平均而言,当使用真实 EMG 作为参考伪影时,大约 75% 的 EMG 伪影被去除),同时保留了与运动相关的预期 EEG 特征。我们还使用模拟 EMG 作为参考伪影测试了 ERASE 程序(大约 63% 的 EMG 伪影被去除)。与传统 ICA 相比,ERASE 从 EEG 中去除的 EMG 伪影平均多 26%。这些发现表明,ERASE 可以实现 EEG 信号和 EMG 伪影的显著分离,而不会丢失底层的 EEG 特征。这些结果表明,使用额外的真实或模拟 EMG 源可以提高 ICA 从 EEG 中去除 EMG 伪影的有效性。结合自动化 IC 伪影剔除,ERASE 还可最大程度地减少潜在的用户偏差。未来的工作将侧重于改进 ERASE,使其也可用于实时应用。
使用合成数据自动检测临床数据仓库中脑 T1 加权磁共振图像中的运动伪影
临床数据仓库 (CDW) 包含数百万患者的医疗数据,为开发计算工具提供了绝佳的机会。磁共振图像 (MRI) 对图像采集过程中的患者运动特别敏感,这将导致重建图像中出现伪影(模糊、重影和振铃)。因此,CDW 中的大量 MRI 被这些伪影破坏,可能无法使用。由于扫描次数太多,无法手动检测它们,因此有必要开发工具来自动排除(或至少识别)带有运动的图像,以充分利用 CDW。在本文中,我们提出了一种从研究到临床数据的新型迁移学习方法,用于自动检测 3D T1 加权脑 MRI 中的运动。该方法包括两个步骤:使用合成运动对研究数据进行预训练,然后进行微调步骤,以将我们的预训练模型推广到临床数据,这依赖于 4045 张图像的标记。目标是 (1) 能够排除具有剧烈运动的图像,(2) 检测轻微的运动伪影。我们的方法在第一个目标上实现了出色的准确率,平衡准确率几乎与注释者的准确率相似(平衡准确率 > 80 %)。然而,对于第二个目标,其表现较弱,远低于人类评分者。总体而言,我们的框架将有助于在医学成像中利用 CDW,并强调对基于研究数据训练的模型进行临床验证的重要性。
双向脑机接口应用中同时进行皮层脑电刺激和记录的最佳伪影抑制
摘要 目的。基于皮层电图 (ECoG) 的脑机接口 (BCI) 是恢复神经功能障碍患者运动和感觉功能的有前途的平台。这种双向 BCI 操作需要同时记录 ECoG 和刺激,这在存在强刺激伪影的情况下具有挑战性。如果 BCI 的模拟前端在超低功耗模式下运行,这个问题会更加严重,这是完全植入式医疗设备的基本要求。在本研究中,我们开发了一种新方法,用于在刺激伪影到达模拟前端之前抑制它们。方法。利用基本的生物物理考虑,我们设计了一种伪影抑制方法,该方法采用在主刺激器和记录网格之间传递的弱辅助刺激。然后通过约束优化程序找到该辅助刺激偶极子的确切位置和幅度。在模拟和幻影脑组织实验中测试了我们方法的性能。主要结果。通过优化程序找到的解决方案在模拟和实验中都与最佳抵消偶极子相匹配。在模拟和脑幻影实验中分别实现了高达 28.7 dB 和 22.9 dB 的伪影抑制。意义。我们开发了一种简单的基于约束优化的方法来查找产生最佳伪影抑制的辅助刺激偶极子的参数。我们的方法在刺激伪影到达模拟前端之前对其进行抑制,并可能防止前端放大器饱和。此外,它可以与其他伪影缓解技术一起使用,以进一步减少刺激伪影。
脑电信号伪差自动检测与滤波的初步研究*
摘要 —EEG 记录中最大的问题之一是伪影造成的信号污染,因为这些干扰会阻碍对真实神经信息的分析。因此,在研究 EEG 之前,在尽可能多地保留大脑数据的同时消除伪影是一个关键步骤。为了解决颅面伪影的自动去除问题,本文提出了一个两阶段程序:前一个阶段是检测阶段 - 同时应用 MLP 神经网络和动态阈值法来检测 EEG 的污染区域,而后一个阶段是去除阶段 - 结合 CCA 和 EEMD 算法仅去除伪影数据。实验结果表明,两种检测方法相当,但动态阈值检测略优于 MLP。此外,组合技术可以完全去除散布在所有 EEG 通道中的伪影。本研究将扩展到需要更复杂模型的眼部伪影。索引术语 —癫痫、EEG、伪影检测、伪影去除