XiaoMi-AI文件搜索系统
World File Search System疫苗类型和免疫抑制疗法而非诊断对风湿病患者接种 COVID-19 疫苗后的抗体反应有重要影响
摘要 目的 开发足够的 COVID-19 疫苗是抗击全球 SARS-CoV-2 大流行的重大突破。然而,疫苗接种效果在自身免疫性风湿病 (AIRD) 患者中可能会降低。本研究旨在确定导致 AIRD 患者体液疫苗接种反应减弱的因素。方法 使用替代病毒中和试验和针对 SARS-CoV-2 受体结合域 (RBD) 的抗体检测来测量 308 名完全接种疫苗的 AIRD 患者的疫苗接种反应。此外,还调查了 296 名免疫功能正常的参与者作为对照组。统计调整分析包括可能影响抗体反应的协变量。结果 AIRD 患者的抗体反应与免疫功能正常的个体相比较低(中和能力中位数 90.8% vs 96.5%,p<0.001;抗 RBD-IgG 中位数 5.6 S/CO vs 6.7 S/CO,p<0.001)。较低的抗体反应受免疫抑制疗法类型的显著影响,但不受风湿病诊断的影响,接受利妥昔单抗治疗的患者产生的抗体水平最低。接受霉酚酸酯、甲氨蝶呤或 Janus 激酶抑制剂治疗的患者的疫苗接种反应也降低。其他负面影响因素包括接种 AZD1222、高龄和前两次接种间隔较短。结论某些免疫抑制疗法与接种疫苗后较低的抗体反应有关。应考虑疫苗类型、年龄和接种间隔等其他因素。我们建议对有风险的 AIRD 患者进行抗体检测,并强调对这些患者进行加强疫苗接种的重要性。
2025; 15(5):1966-1986。 doi:10.7150/thno.103175研究论文TBX3塑造免疫抑制微环境并诱导免疫疗法抗性
背景:识别预测免疫疗法功效的生物标志物并发现联合疗法的新靶标是改善膀胱癌(BLCA)患者预后的关键要素。方法:首先,我们使用来自多个公共数据库的数据探索了正常和Pan-Cancer组织中TBX3的表达模式以及TBX3与免疫微环境之间的相关性。然后,我们组合了各种技术,包括大量RNA测序,单细胞RNA测序,高通量细胞因子阵列,功能实验,Procartaplex多重免疫测定和组织全景组织量化测定,以证明TBX3将Immunosupsporcement tamorsument(bla)塑造为bla s inrosement(bla)。结果:我们将TBX3确定为与BLCA中的免疫抑制微环境相关的关键因素。我们发现TBX3主要在恶性细胞中表达,其中TBX3高肿瘤细胞增加了TGFβ1的分泌,从而促进了与癌症相关的成纤维细胞(CAF)浸润,从而形成了一种免疫抗抑制性的微节流。我们进一步证明,TBX3通过与TGFβ1启动子结合来增强TGFβ1的表达,并阻止TGFβ1抵消TBX3的免疫抑制作用。此外,TBX3通过降低GZMB + CD8 + T细胞的比例来降低CD8 + T细胞的杀菌效率,并敲击TBX3与抗PD-1处理相结合的TBX3增加了CD8 + T细胞的浸润增加了VIVO中的CD8 + T细胞浸润和降低CAF。最后,我们发现TBX3预测了现实世界中免疫疗法队列和多个公共队列中的免疫疗法功效。我们还验证了TBX3 +恶性细胞与CD8 + T细胞之间的反比关系以及组织微阵列中与CAF的正相关关系。结论:总而言之,TBX3通过诱导免疫抑制微环境促进BLCA的进展和免疫疗法抗性,而靶向TBX3可以增强BLCA免疫疗法的功效。
引用:Grint DJ、McDonald HI、Walker JL 等。美国免疫抑制患者意外注射活带状疱疹疫苗的安全性
► ► 本研究使用电子健康记录在大型国家队列中调查了免疫抑制期间接种带状疱疹活疫苗的安全性。 ► ► 这是第一项涵盖英国国家指导中列为疫苗接种禁忌症的免疫抑制原因的全部情况的研究,这些原因来自多个初级和二级保健来源。 ► ► 初级和二级保健记录都用于彻底确定水痘-带状疱疹病毒相关疾病,包括确定非特异性皮疹或未指明病因的脑炎的敏感性分析。 ► ► 仅使用出生年份作为年龄合格来分析疫苗接种率,因此分母根据部分合格的出生队列进行了调整。 ► ► 免疫抑制没有根据严重程度区分,但临床医生可能有选择地接种疫苗,在当前疫苗接种实践之外应用这些发现时需要谨慎。
引用:Grint DJ、McDonald HI、Walker JL 等。美国免疫抑制患者意外注射活带状疱疹疫苗的安全性
► ► 本研究使用电子健康记录在大型国家队列中调查了免疫抑制期间接种带状疱疹活疫苗的安全性。 ► ► 这是第一项涵盖英国国家指导中列为疫苗接种禁忌症的免疫抑制原因的全部情况的研究,这些原因来自多个初级和二级保健来源。 ► ► 初级和二级保健记录都用于彻底确定水痘-带状疱疹病毒相关疾病,包括确定非特异性皮疹或未指明病因的脑炎的敏感性分析。 ► ► 仅使用出生年份作为年龄合格来分析疫苗接种率,因此分母根据部分合格的出生队列进行了调整。 ► ► 免疫抑制没有根据严重程度区分,但临床医生可能有选择地接种疫苗,在当前疫苗接种实践之外应用这些发现时需要谨慎。
微生物组 - 生物分析分析揭示了香草planifolia Andrew(EVPA)提取物对免疫抑制小鼠的免疫保护作用
摘要:已经证明了中枢和周围炎症参与主要抑郁症(MDD)的发病和预后。抑郁症患者中促炎细胞因子(介体(IL)-1β,IL-6,IL-18和TNF-α)的增加可能会引起神经炎症过程和周围炎症,而这些机制,这些机制又可能有助于GUT Microbobobiota Dysbibiosis。一起,神经炎症和肠道营养不良会诱导色氨酸代谢的改变,最终导致5-羟色胺合成,神经可塑性相关机制的障碍以及谷氨酸介导的介导的兴奋性。本综述旨在强调涉及MDD病理生理学的炎症机制(神经炎症,周围炎症和肠道营养不良),并探索这种精神疾病的新型抗炎治疗方法。几条证据表明,除了抗抑郁药,体育锻炼,益生菌和营养素(agmatine,抗坏血酸和维生素D)外,还具有抗炎作用,可能有助于其抗抑郁剂。对于探索这些替代疗法对MDD的治疗益处的进一步研究是必要的。
NKG2A+ CD8+ T细胞浸润确定了透明细胞肾细胞癌对免疫疗法的免疫抑制和劣等反应
抽象免疫检查点抑制剂(ICI)治疗已成为各种癌症类型的重要治疗选择。尽管治疗是有效的,但ICI可以过度刺激患者的免疫系统,从而导致潜在的严重免疫相关性不良事件(IRAE),包括肝炎,结肠炎,肺炎和心肌炎。最初的治疗支柱包括施用皮质类固醇。几乎没有证据表明如何治疗类固醇(SR)IRAE。它主要基于小型案例系列或单个病例报告。此系统评价总结了有关SR-IRAES的可用证据。我们在PubMed进行了系统的文献搜索。此外,我们在评估中还包括了欧洲医学肿瘤学学会,癌症免疫疗法,国家综合癌症网络和美国临床肿瘤学会指南。所有选定出版物的研究人群都必须包括患有肝炎,结肠炎,肺炎或心肌炎的患者,在免疫疗法治疗期间或之后,皮质类固醇治疗不足。我们的文献搜索不仅限于任何特定的癌症诊断。案例报告也包括在内。关于危及生命的SR-IRAE的数据有限,大多数出版物是单个病例报告。大多数出版物研究了SR结肠炎(n = 26),其次是肝炎(n = 21),肺炎(n = 17)和心肌炎(n = 15)。SR情况的指南建议未精确定义。有大多数数据用于治疗SR肝炎和英夫利昔单抗的大多数数据,其次是维多珠单抗治疗SR结肠炎。关于SR肺炎,MMF和静脉内免疫球蛋白(IVIG)的大多数数据是关于英夫利昔单抗的数据矛盾的。在SR心肌炎中,大多数证据都可以用于使用Abatacept或抗心理细胞球蛋白(ATG)(有或不带有MMF)或与Abatacept一起使用。 本评论强调了对SR肝炎,结肠炎,肺炎和心肌炎的迅速识别和治疗的必要性。 根据我们的搜索,我们建议作为第一线治疗 - (1)SR肝炎的MMF,(2)用于SR结肠炎的英夫利昔单抗,其次是Vedolizumab,(3)MMF和IVIG,用于SR肺炎和(4)Abatacept或Abatacept或Atg(均与MMF)或Ruxolitib s abacecardib sr abaceptitib(均为Abatacept或Atg)。 如果在3天内对皮质类固醇没有足够的反应,应立即启动这些其他免疫抑制剂。在SR心肌炎中,大多数证据都可以用于使用Abatacept或抗心理细胞球蛋白(ATG)(有或不带有MMF)或与Abatacept一起使用。本评论强调了对SR肝炎,结肠炎,肺炎和心肌炎的迅速识别和治疗的必要性。根据我们的搜索,我们建议作为第一线治疗 - (1)SR肝炎的MMF,(2)用于SR结肠炎的英夫利昔单抗,其次是Vedolizumab,(3)MMF和IVIG,用于SR肺炎和(4)Abatacept或Abatacept或Atg(均与MMF)或Ruxolitib s abacecardib sr abaceptitib(均为Abatacept或Atg)。如果在3天内对皮质类固醇没有足够的反应,应立即启动这些其他免疫抑制剂。
微生物组-代谢组学分析揭示香草兰提取物(EVPA)对免疫抑制小鼠的免疫保护作用
摘要:本研究探讨了香草兰提取物(EVPA)对环磷酰胺(Cy)诱导的小鼠免疫抑制的免疫保护作用。结果表明,EVPA可显著减轻Cy诱导的免疫损伤,改善小鼠体重、脏器指数和结肠损伤。进一步对微生物多样性的分析发现,EVPA主要增加了有益菌Verrucomicrobiota、乳酸杆菌科和乳酸杆菌属的丰度,同时降低了Akkermansiaceae、Akkermansia、Romboutsia和乳球菌属的丰度,从而改善了Cy引起的微生态失调。代谢组学分析显示,EVPA 治疗后,微生物代谢物水平发生了显著变化,包括尿胆原、甲酰胺嘧啶核苷三磷酸、Cer (d18:1/18:0)、泛酰巯基乙胺和 LysoPC (15:0/0:0)。这些改变的代谢物与鞘脂代谢、卡巴培南生物合成、泛酸和辅酶A生物合成、甘油磷脂代谢以及卟啉代谢相关的途径有关。此外,某些微生物组与差异代谢物之间存在显著相关性。这些发现为 EVPA 对肠道菌群和代谢的免疫调节作用提供了新的见解,为其更广泛的应用奠定了基础。
额外的 mRNA COVID-19 疫苗剂量证明
或其他可能抑制免疫反应的药物:高剂量皮质类固醇(即每天≥20毫克泼尼松或等效药物)、烷化剂、抗代谢物、移植相关的免疫抑制药物、归类为严重免疫抑制的癌症化疗药物、肿瘤坏死因子(TNF)阻滞剂或其他具有免疫抑制或免疫调节作用的生物制剂“
实践工具 #2 – CEV/免疫抑制的定义
临床极度脆弱 (CEV) 标准是由一组省级专家制定的,他们负责照顾患有癌症、囊性纤维化、器官移植和肾病等疾病的患者,目的是确定哪些人应优先接种疫苗。CEV 类别的患者将收到 Bonnie Henry 博士的证明信,证明他们处于这一状态。患者通常知道自己是否是 CEV,并能回答原因。CEV 分为三组:1、2 和 3。第 1 组是 12 岁及以上的患者,他们因血液系统恶性肿瘤等疾病而严重免疫抑制,正在接受积极治疗或接受实体器官移植。第 2 组是 12 岁及以上的中度免疫抑制患者。第 3 组是 18 岁及以上的患有不同疾病的患者,他们没有免疫抑制,但患 COVID-19 并发症的风险很高。CEV 类别是在 2020 年制定的,患者不会从这些名单中删除,因为他们仍然需要后续接种疫苗。然而,如果被归类为 CEV 的患者不再受到免疫抑制或处于风险中,则可能不符合治疗条件。请查阅使患者符合治疗条件的精确 CEV 定义,并特别注意时间段和注意事项。
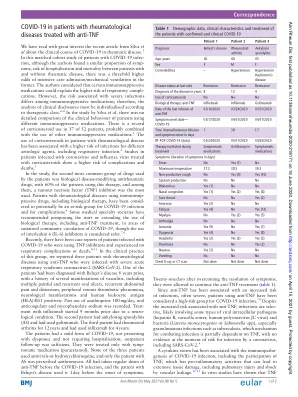
接受抗 TNF 治疗的风湿病患者中 COVID-19
我们饶有兴趣地阅读了Silva等人最近发表的关于风湿病中COVID-19临床病程的文章。1 在这项对COVID-19感染患者的匹配队列研究中,虽然作者发现患有和未患有风湿病的患者的症状比例、住院风险和死亡风险相似,但前者进入重症监护/机械通气的几率高出三倍。作者认为某些免疫抑制药物可以解释呼吸道并发症风险较高。然而,不同免疫抑制药物与严重感染相关的风险不同;因此,临床披露的分析必须根据治疗类别进行个性化。2–4 在Silva等人的研究中,没有对使用不同免疫抑制药物的患者的临床行为进行详细比较。52名患者中有37名有使用皮质类固醇的记录,可能与使用其他免疫抑制药物相结合。 1 风湿病患者使用皮质类固醇与感染不同病原体(包括呼吸道感染)的风险增加有关。 2 研究表明,感染冠状病毒和流感病毒的患者使用皮质类固醇治疗后,并发症和死亡的风险更高。 5