XiaoMi-AI文件搜索系统
World File Search System荧光标记的维多珠单抗可用于可视化炎症性肠病中的药物分布和粘膜靶细胞
摘要 目的 改善 IBD 患者选择和生物疗法(如维多珠单抗)的开发需要彻底了解作用机制和靶标结合,从而提供个性化的治疗策略。我们的目的是可视化静脉注射荧光标记的维多珠单抗 vedo-800CW 的宏观和微观分布,并使用荧光分子成像 (FMI) 识别其靶细胞。 设计 进行了 43 次 FMI 程序,包括内窥镜检查期间的宏观体内评估,然后进行宏观和微观体外成像。在 A 期,患者在内窥镜检查前接受 4.5 毫克、15 毫克 vedo-800CW 或无示踪剂的静脉注射。在 B 期,患者接受 15 毫克 vedo-800CW,然后接受未标记的(亚)治疗剂量的维多珠单抗。结果 FMI 定量显示炎症组织中 vedo-800CW 荧光强度呈剂量依赖性增加,15 mg(153.7 au(132.3–163.7))是最适合的示踪剂剂量,而 4.5 mg(55.3 au(33.6–78.2))则为最合适剂量(p=0.0002)。此外,在给予治疗剂量的未标记维多珠单抗后给予 vedo-800CW 时,荧光信号降低了 61%,表明炎症组织中的靶标已饱和。荧光显微镜和免疫染色显示,维多珠单抗渗透到发炎的粘膜中并与几种免疫细胞类型相关,最显著的是与浆细胞相关。结论这些结果表明 FMI 有望确定炎症靶组织中药物的局部分布并识别药物靶细胞,为靶向药物在 IBD 中的应用提供了新的见解。试验注册号 NCT04112212。
内源性钙蛋白酶抑制剂calpastatin减弱了鼠鼠bar综合征的轴突变性
图1内源性HCAST表达可保护急性离体损伤模型中的轴突完整性。三角形(TS)的神经肌肉制剂(WT,n = 3)和Hcast(n = 3)小鼠用抗绞中AB(AGAB)在体内进行内部化研究(A,B),以及(损伤)或没有(对照)正常人(nHs)(nhs)的position(Corsem and Huspect)(CORCE)(CORCE)(cosect)(conterum and)(nhs),以供应(nhs),以供应(nhs),以供介绍。a)WT和Hcast TS运动神经末端(MNT)在37 C下孵育60分钟时,表面AGAB显着降低,而不是0分钟。(b)在用Triton X-100通透性后,在60分钟组中,MNT的总AGAB强度在两种基因型中都恢复正常,这表明AGAB内在化。(c)与对照相比,受伤的WT和Hcast TS的MNT的补体(绿色,E)强度显着增加。(d)神经丝(NF-H,洋红色,E)与对照相比,受伤的WT组织中MNT处的免疫染色强度显着降低,但受到Hcast受伤组织的对照水平的保护。(e)远端神经染色的说明性图像。btx(星号,橙色)和髓磷脂碱性蛋白(MBP,箭头,橙色)分别用于识别Ranvier(Nor)的Mnt和远端节点。虚线的大纲表示没有NF-H染色的位置。比例尺=5μm。 dotplots =平均±S.E.M.在比较治疗效果的数据上进行了未配对的一尾t检验(A,B&C); *表示p <.05。双向方差分析比较治疗(对照与损伤)或基因型(WT vs Hcast),然后对D.的数据进行了Tukey的事后多重比较测试。 * p <.05,***表示p <.001
p38抑制剂对鸡肌干细胞增殖的影响,并分化为肌肉和脂肪
目的:抑制p38有丝分裂原激活的蛋白激酶(MAPK)信号通路延迟分化并增加大多数物种中肌肉干细胞的增殖。在这里,我们旨在研究p38抑制剂(p38i)治疗对鸡肌干细胞增殖和分化的影响。方法:在胚胎第18天,从Hy-Line棕色鸡肉胚胎的肌肉组织中收集鸡肉干细胞,然后通过预制方法分离。细胞在补充二甲基亚氧化二甲基氧化二甲基氧化物或1、10、20μMP38I的生长培养基中培养4天,然后取代多达4个传递。通过分化培养基诱导了3天的分化。每次处理3次。结果:配对框7基因和肌源性因子5基因的增殖和mRNA表达以及p38-preated培养物中肌源分化标志物基因肌生成蛋白的mRNA表达明显高于对照(p <0.05),但在肌蛋白重链中的免疫染色和mRNA表达并不重要(MHC)。分化细胞培养物中累积的脂质液滴的油红O染色显示,p38-WERACETAL培养物中的脂质密度高于对照。然而,两组之间的掺杂标记基因基因过氧化物酶体增殖物激活受体伽马的表达并没有显着差异。结论:鸡肌干细胞中的p38抑制作用可改善细胞的增殖,但是对肌原性分化和脂质积累的影响需要进行其他分析。需要对鸡肉P38-MAPK途径进行进一步的研究,以了解肌肉和脂肪发育机制。
2025; 15(4):1338-1352。 doi:10.7150/thno.100451研究论文RPS23RG1抑制MDGA2的Sort1介导的溶酶体降解以防止自动
基本原理:含有糖基磷脂酰肌醇锚固2(MDGA2)的突触蛋白MAM结构域的突变与自闭症谱系障碍(ASD)有关。因此,阐明MDGA2的调节机制可以帮助开发有效的ASD治疗方法。方法:进行液相色谱串联质谱法以鉴定与RPS23RG1和MDGA2相互作用的蛋白质,然后进行共免疫沉淀测定,以确认蛋白质蛋白质蛋白相互作用。RPS23RG1和Sort1水平被siRNA下调,以研究其对MDGA2降解的影响,并进行了免疫印迹和免疫染色测定的其他应用。溶酶体分离,以进一步确定MDGA2的溶酶体降解。RPS23RG1基因敲除小鼠和MDGA2 +/-小鼠进行各种行为测试,以研究其ASD样表型。在RPS23RG1敲除小鼠中递送表达MDGA2的AAVS,RPS23RG1衍生的肽在MDGA2 +/-小鼠中递送以研究其救援效果。结果:我们发现RPS23RG1和Sort1都与MDGA2相互作用。mdga2主要通过Sort1介导的溶酶体降解途径降解。RPS23RG1与Sort1竞争MDGA2结合以抑制MDGA2降解。此外,我们表明RPS23RG1敲除小鼠表现出降低的MDGA2水平和类似ASD的行为,而MDGA2水平的恢复会减弱RPS23RG1 KO小鼠的社会缺陷。此外,我们确定了用于MDGA2相互作用的RPS23RG1的关键区域,发现源自该区域的肽不仅结合MDGA2并促进MDGA2水平,而且还挽救了MDGA2 +/-小鼠中的社会缺陷。结论:我们的发现突出了RPS23RG1在拮抗MDGA2的Sort1介导的溶酶体降解中的关键作用,并提出了靶向RPS23RG1-MDGA2轴以用MDGA2缺乏处理ASD的潜力。
研究报告卟啉念珠菌lps和放线症Naeslundii条件培养基增强了低分子量的释放,转录>
摘要。背景:糖原合成酶-3激酶(GSK3)是与阿尔茨海默氏病(AD)中与神经纤维缠结有关的Tau高磷酸化的主要贡献者之一。目的:确定两个牙周细菌始终确认在AD尸体式大脑中始终确定的GSK-3激活的机制。方法:收集了牙龈卟啉单胞菌FDC381和放线菌Naeslundii ATCC10301条件培养基。imr-32细胞与条件培养基(ATCC33277)在既定的细胞培养条件下指定的PG.LPS(LPS)的牙龈疟原虫(ATCC33277)挑战48小时。进行了GSK-3的基因表达和蛋白质分析。结果:qPCR证明,用PG.LP处理的IMR-32细胞中GSK-3基因过表达,变化为2.09倍(P = 0.0005),而A. Naeslundii处理的细胞显示出1.41倍的变化(P = 0.004)。Western印迹在PG.LPS(P = 0.01)和A. Naeslundii条件培养基(P = 0.001)挑战的细胞中,对每种处理的37 kDa频段(p = 0.001)证明了在整个培养基中具有可变强度的每种处理。与pg.lps和a。naeslundii挑战的IMR-32细胞的GSK-3免疫组织化学表现出细胞质和核定位。结论:暴露于各种细菌因子上调GSK-3的基因表达。GSK-3的Western印迹确认了PG.LPS(37 kDa频带p = 0.01)和A. Naeslundii条件条件培养基(37 kDa频带p = 0.001)的裂解片段的存在。免疫染色显示GSK-3的细胞质和核定位。因此,通过其转录活性,裂解,碎片,a。naeslundii介导的GSK-3激活的pg.lps和未知因子。体内的这些毒力因素似乎对大脑健康有害。
肌萎缩性侧硬化症(ALS)的新治疗靶
所有这些在细胞中都起着非常重要的作用。核膜是围绕细胞核的双层结构,在保护细胞核免受细胞质和保护细胞核中的DNA免受外部影响方面发挥作用。核膜是控制重要过程的一个场所,例如细胞中的DNA复制,转录和修复。核膜对于维持核的形状也很重要,并且在稳定核的结构中也起作用。 核孔是嵌入核膜中的复合物,并用作在细胞核和细胞质之间运输材料的途径。细胞核中所需的蛋白质和RNA通过核孔传输,相反,在细胞核中合成的RNA和核糖体亚基中的RNA转运到细胞质。该传输非常严格控制,对于单元的正常运行至关重要。 如果这些结构无法正常运行,细胞将无法执行正常的基因表达或蛋白质合成,从而对细胞功能造成严重损害。因此,核膜和核孔是细胞寿命支持的极其重要的结构。 到目前为止,已经有几份有关ALS中核膜和核孔的报道,但是讨论的解释和意义一直在继续。在该研究组中,我们建立了IPS细胞(Ichiyanagi N等。运动神经元与干细胞报告的分化2016(Setsu S等人Biorxiv 2023),此外,使用ALS患者的验尸组织(脊髓)来阐明核鞘和核孔的病理。 3。进行了研究内容和结果(1)免疫染色,以评估运动神经元(18个月大)野生型小鼠和FUS-FUS-ALS模型小鼠的运动神经元(聊天量)(聊天定型)中核膜(层层B1,lamin a/c)的形态。 FUS-ALS模型小鼠中的运动神经元显示出与核膜相对应的部分的亮度和圆度降低(图1)。此外,核孔的形态学评估(NUP62)显示核孔中存在缺陷。这些结果证实,在FUS-ALS模型小鼠中,核膜和核孔受损。
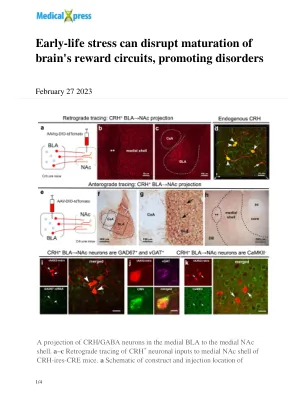
早期的压力会破坏大脑奖励电路的成熟,促进疾病
AAV2 -RETRO -CAG -FLEX -TDOMATO -WPRE病毒,可允许逆行进入投影神经元,从而为NAC提供传入的输入。b示例局部感染的CRH +轴突末端的共聚焦显微照片在内侧NAC壳中。c逆行跟踪将内侧BLA识别为CRH + NAC输入的强大来源。d 3D图像(z-stack;0.5μm步长)确认在AAV-RETRO感染细胞(红色)的BLA中定位,共表达内源性CRH(绿色);双重标记的神经元=黄色。e - 从BLA到内侧NAC壳的CRH +轴突投影的g顺行追踪。e,AAV1-DIO-TDTOMATO构建体和病毒遗传实验设计。f病毒注射仅限于中央杏仁核(CEA)的BLA,G,通过在BLA CRH +神经元中的TDTomato选择性表达显示。h bla-origin CRH +轴突和内侧NAC壳中的端子。i - K病毒注射到BLA中的内侧NAC壳逆转录感染的SOMATA。i将荧光原位杂交(FISH)与BLA中CRH +细胞中的GAD67 mRNA进行免疫染色。箭头指向共定位的GAD67 mRNA和病毒 - 重复蛋白标记。j a bla→NAC细胞(红色)共表达内源性CRH(绿色)和VGAT(Magenta),但K不会共表达谷氨酸能标记Camkii。** = Calleja的主要岛,AC前委员会,DB对角线带。i和k中的比例尺= 10 µm。在至少两个独立的垃圾中评估了在小鼠中评估发现发现,病毒注射,投射评估和免疫组织化学的。信用:自然通讯(2023)。doi:10.1038/s41467-023-36780-x
在子宫内电穿孔中,多d缩的基因组 -
位于小鼠大脑皮层中的原生质星形胶质细胞(PRA)紧密并置,在成人阶段形成了明显连续的三维基质。到目前为止,没有免疫染色策略可以将它们单一单一的策略和在成熟动物和皮质生成过程中的形态进行分割。皮质PRA起源于背胸膜中的祖细胞,可以轻松地使用整合载体的子宫电穿孔来靶向。这里提出了一项方案,该方案将这些细胞用可抑制基因组融合的颜色(魔术)标记策略标记,该策略依赖于PiggyBac/ tol2换位和CRE/ LOX重组以随机表达明显的荧光蛋白(蓝色,氰基,黄色和红色),以特定于特异性的亚细胞界面。这种多色命运映射策略使在胶片发生开始之前与颜色标记物的结合可以标记附近的皮质祖细胞,并跟踪其后代,包括星形胶质细胞,从胚胎到各个细胞水平的成人阶段。半parse标记通过调整电穿孔矢量的浓度和颜色对比度的浓度,该颜色可通过多种基因组整合的颜色标记(魔术标记或MM)提供,使星体胶质细胞个性化并将其领土和复杂的形态单一单一单一单一单独化。是一个全面的实验工作流程,包括电穿孔程序的详细信息,通过共聚焦显微镜进行多通道图像堆栈以及计算机辅助的三维分割,这将使实验者能够评估单个PRA的体积和形态。总而言之,魔术标记的电穿孔提供了一种方便的方法,可以单独标记许多星形胶质细胞并在不同的发育阶段访问其解剖特征。该技术对于分析各种小鼠模型中的皮质星形胶质细胞形态特性将是有用的,而无需诉诸于具有转基因报告基因的复杂杂交。
摘要 PDF 海报
摘要:发生在前脑室下区 (SVZ) 和齿状回颗粒下区 (SGZ) 的成年神经发生受年龄、性激素和其他细胞和分子因素等参数的影响。我们之前发表的关于雄性 F344 大鼠的研究表明,神经发生衰退在 13 至 15 个月大期间尤为明显。我们还确定,这种与年龄相关的神经发生衰退的特殊模式是由氧化还原敏感转录因子核因子 (红细胞衍生 2) 样 2 或 NRF2 表达减少所介导的。在本研究中,我们旨在了解年龄增长和性激素 17β-雌二醇 (E2) 和孕酮 (P4) 对雌性大鼠神经干祖细胞 (NSPC) 的 NRF2 表达和再生功能的影响。在此背景下,我们已确定与雄性大鼠相比,雌性大鼠的 NSPC 功能与年龄相关的衰退的时间进展不同,并且发生得更早,主要在 7-9 个月大时。为了进一步研究这种 NSPC 衰老现象,我们分析了 2、6、9 和 14 个月大雌性 F344 大鼠。在 4 个衰老阶段,我们分别纳入完整大鼠 (Sham) 和卵巢切除大鼠 (OVX),以评估 E2/P4 的重要性。对实验组执行以下行为任务以研究 SVZ 和 SGZ NSPC 功能 - 精细嗅觉辨别、模式分离和 Morris 水迷宫中的平台反转。结果显示,与 OVX 相比,假手术动物的神经发生得到显著保护,尤其是在 6 月龄和 9 月龄时。这些结果也得到了发情阶段研究结果的支持,其中假手术大鼠在发情或发情前期阶段(循环中 E2 和 P4 增加)的表现优于其他阶段。目前,我们正在通过对不同 NSPC 亚型标志物(特别是 GFAP/Nestin、Sox2 和 Dcx)和增殖标志物(BrdU、MCM2)进行双重或三重免疫染色,以及 NRF2 及其下游靶标(如 NAD(P)H 醌脱氢酶 1 (NQO1))来检查四个年龄组中 NSPC 中 NRF2 表达和活性的变化。总之,这些
一例引人注目的记忆障碍病例的神经病理学为人类记忆提供了启示
肯特·科克伦 (KC) 在 30 岁时因摩托车事故导致颅内创伤,导致其出现严重的失忆症,此后近三十年来研究人员一直在对他进行研究。KC 在言语和非言语领域均患有严重的前行性遗忘症,同时伴有选择性逆行性遗忘症,无法记住受伤前经历的个人事件(情景记忆),而对个人和世界事实的记忆(语义记忆)以及内隐记忆则相对保留。这种保留和受损的记忆模式延伸到对大规模环境的空间记忆,以及对未来的想象和决策。62 岁时死后大脑检查结果包括中度弥漫性萎缩、左侧眶额挫伤、左侧大脑后动脉梗塞和左前额分水岭梗塞。值得注意的是,双侧海马均有严重的神经元丢失和神经胶质增生。左侧海马前部和后部受到严重影响,但 CA2、CA4 和齿状回 (DG) 局部未受损。左侧穹窿伴有退化。右侧海马前部几乎完全破坏,后部相对保存,主要是 CA4 和 DG。双侧海马旁回和左侧丘脑前部也出现神经元丢失和神经胶质增生。β-淀粉样蛋白、磷酸化 tau 或 TDP-43 免疫染色未发现共存的神经退行性现象。内侧颞叶结构受损程度与 KC 严重的顺行性和逆行性遗忘症相符,但意外发现 CA2/CA4 和 DG 保存完好。 KC 的案例表明,在广泛的脑损伤后,相对明显的功能分离仍然可能存在,结构受损的脑区不太可能对完整的认知功能至关重要。这样一来,本文提出的研究结果为 KC 对我们理解记忆的临床解剖关系做出了重要贡献。