XiaoMi-AI文件搜索系统
World File Search System双盲,安慰剂控制的lurasidone单药治疗,用于治疗双极I抑郁>
双相情感障碍是一种慢性精神病,估计的终身患病率在0.2%至1.0%之间。1,2它在全球残疾的前20名原因中排名,也是发达国家残疾的十大原因之一。3由于双相情感障碍而导致的社会和职业功能的障碍是广泛的。在失去工作的日子,就业损失以及重新开始就业的困难中观察到对工作功能的影响。4,5躁郁症患者发现的总体健康相关生活质量与其他严重和慢性医学疾病相当。6躁郁症已显示可将个体的预期寿命降低约9年。7这是许多因素的结果,包括较高的合并症率(例如肥胖,糖尿病和心血管疾病)和自杀。8 - 10美国双相情感障碍的年度经济负担估计直接成本约为310亿美元,间接成本额外为1,200亿美元。11在日本,许多患有躁郁症的人报告时间
Kura Oncology 和 Kyowa Kirin 宣布 Ziftomenib 单药治疗注册试验结果呈阳性,并且
– Kura 管理层将于今天美国东部时间下午 4:30 举办虚拟投资者活动 – 圣地亚哥和东京,2025 年 2 月 5 日和 6 日 – Kura Oncology, Inc. (Nasdaq: KURA,“Kura”) 和 Kyowa Kirin Co., Ltd. (TSE: 4151,“Kyowa Kirin”) 今天宣布了 KOMET-001 的积极顶线结果,这是 ziftomenib 的 2 期注册导向试验,ziftomenib 是一种高度选择性、每日一次的口服研究性脑膜炎抑制剂,用于治疗复发/难治性 (R/R) NPM1 突变型 (NPM1-m) 急性髓细胞白血病 (AML) 患者。 KOMET-001 的顶线数据已提交给即将于 2025 年第二季度举行的医学会议进行展示,Kura 有望在 2025 年第二季度向美国食品药品监督管理局 (FDA) 提交 ziftomenib 的新药申请 (NDA)。两家公司宣布将在 2024 年联合将 ziftomenib 商业化,同时还宣布他们计划启动一项单一方案,该方案包含两项独立驱动、随机、双盲、安慰剂对照、注册性 3 期试验,以评估 ziftomenib 联合强化和非强化联合方案对新诊断的 NPM1-m 和 KMT2A 重排 (KMT2A-r) 患者的效果
剂量和给药指南
警告和注意事项 综合管理以降低 HIV-1 感染风险: • 使用 APRETUDE 作为综合预防策略的一部分,包括遵守给药时间表和安全性行为(包括使用避孕套),以降低性传播感染 (STI) 的风险。APRETUDE 并非总是能有效预防 HIV-1 感染。HIV-1 感染风险包括但不限于无避孕套性行为、过去或当前的性传播感染、自我认定的 HIV 风险、性伴侣 HIV-1 病毒血症状态不明或在高流行地区或网络中的性活动。告知、辅导和支持个人使用其他预防措施(例如,持续正确使用避孕套;了解伴侣的 HIV-1 状态,包括病毒抑制状态;定期检测性传播感染)
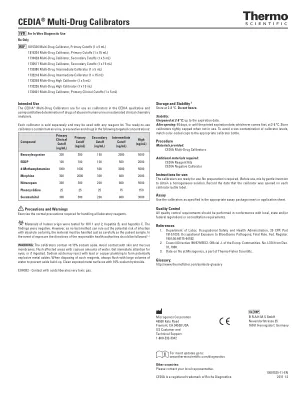
Cedia®多药校准器
警告:校准器含有≤0.13%叠氮化钠。避免接触皮肤和粘膜。带有大量水的冲洗区域。立即注意眼睛,或者摄入。叠氮化钠可能与铅或铜管道反应,形成潜在的爆炸金属叠氮化物。处置此类试剂时,请始终用大量的水冲洗以防止叠氮化物积聚。用氢氧化钠含10%的清洁裸露的金属表面。
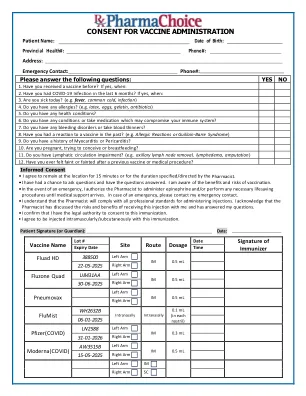
疫苗给药的同意
请回答以下问题:是否1。您以前收到过疫苗吗?如果是,何时:2。过去6个月中,您是否感染了19号感染?如果是,何时:3。你今天生病了吗?(例如发烧,普通感冒,感染)4。您有什么过敏吗?(例如乳胶,鸡蛋,明胶,抗生素)5。您有任何健康状况吗?6。您是否有任何条件或服用可能损害免疫系统的药物?7。您是否患有出血性疾病或服用血液稀释剂?8。过去您对疫苗有反应吗?(例如过敏反应或Guillain-Barre综合征)9。您有心肌炎或心包炎的病史吗?10。您是否怀孕,试图怀孕或母乳喂养?11。您是否患有淋巴循环障碍?(例如腋窝淋巴结去除,淋巴水肿,截肢)12。在先前的疫苗或医疗程序后,您是否曾经感到昏昏欲睡或晕倒?
治疗药物类
o临床痴呆评级(CDR)全球评分为0.5 o客观证据的筛查中的认知障碍证据在24到30 O之间的筛查分数在24至30 O之间的PET扫描对淀粉样蛋白β斑块或脑脊髓液(CSF)测试的淀粉样蛋白β斑块或大脑测试呈阳性是淀粉样蛋白的阳性阳性•在1年内,在1年内进行了启动(在1年内)的脑部MRI MRI MRI MRI MRI MRI在1年内进行了启动。输注(首次剂量为10mg/kg)和第12次输注(第六剂量为10mg/kg)•患者在治疗开始后的1年内没有任何以下任何一项:预处理局部浅表性副作用,10或更多的脑出血或更多的脑出血或更多的脑出血> 1 cm•患者的治疗方法有很多疾病的良好疾病的良好疾病,该疾病的良好疾病的依据,该疾病已被固定在1年前,该疾病已被固定为1年,抑制剂,除非禁忌。 •为了重新批准,与治疗前基线相比,患者必须对治疗做出反应,这可以通过改善,稳定或减缓认知或功能障碍的速度来证明,并且患者没有发展为中度或严重疾病(在中度或重度AD中没有足够的证据)。 NMDA受体拮抗剂美容片o临床痴呆评级(CDR)全球评分为0.5 o客观证据的筛查中的认知障碍证据在24到30 O之间的筛查分数在24至30 O之间的PET扫描对淀粉样蛋白β斑块或脑脊髓液(CSF)测试的淀粉样蛋白β斑块或大脑测试呈阳性是淀粉样蛋白的阳性阳性•在1年内,在1年内进行了启动(在1年内)的脑部MRI MRI MRI MRI MRI MRI在1年内进行了启动。输注(首次剂量为10mg/kg)和第12次输注(第六剂量为10mg/kg)•患者在治疗开始后的1年内没有任何以下任何一项:预处理局部浅表性副作用,10或更多的脑出血或更多的脑出血或更多的脑出血> 1 cm•患者的治疗方法有很多疾病的良好疾病的良好疾病,该疾病的良好疾病的依据,该疾病已被固定在1年前,该疾病已被固定为1年,抑制剂,除非禁忌。•为了重新批准,与治疗前基线相比,患者必须对治疗做出反应,这可以通过改善,稳定或减缓认知或功能障碍的速度来证明,并且患者没有发展为中度或严重疾病(在中度或重度AD中没有足够的证据)。NMDA受体拮抗剂美容片