XiaoMi-AI文件搜索系统
World File Search System利用重组DNA技术进行饲料添加剂安全性确认的申请...
2025年1月13日农林水产省食品消费者局针对利用重组DNA技术生产的饲料添加剂的安全性确认申请,现面向社会公开征集意见及信息。 展望未来,我们计划在考虑所提交的意见和信息之后对该提议做出决定。 请注意,我们无法对所提交的每条意见进行单独回复。 1. 征求公众意见的目的、目的及背景 (1)根据《关于保证饲料安全及提高饲料品质的法律》(1953年法律第35号)第3条第1款以及《关于饲料和饲料添加剂成分标准等的部令》(1976年农林渔业部法令第35号)附件2-2,使用通过重组DNA技术获得的生物体生产的饲料添加剂(以下称为“使用重组DNA技术生产的饲料添加剂”)需要由农林渔业部长确认其安全性。 农林水产部长对安全性进行确认的程序,在《依据饲料及饲料添加剂成分标准部令对重组DNA技术生产的饲料及饲料添加剂的安全性进行确认的程序》(2002年11月26日农林水产省告示第1780号,以下简称“本告示”)中进行了规定,其中规定,农林水产部长在确认安全性时,必须听取农业物资委员会对食用该重组DNA技术生产的饲料添加剂的牲畜的安全性的意见(本告示第3条第2款)。 (2)最近,利用重组DNA技术生产的下列饲料添加剂已根据本通报提交了安全性确认申请。农资审议会听取了意见后,答复称,上述饲料添加剂被牲畜摄取后,不存在安全性问题。
基于汽车软件的系统的质量,安全性和安全性
亚历山大·克洛茨(Alexander Klotz)是Vitesco Technologies技术合规性(TC)负责人。他负责公司技术合规性管理系统(TCM)和全球TC策略,该战略旨在检测和减轻与不合规产品(硬件和/或软件)和系统相关的风险。符合VDA产品合规性定义,Vitesco TCMS涵盖了法规,全球标准和考虑相关方面,以推导“最先进”。在他以前在大陆上的职位,亚历山大·克洛兹(Alexander Klotz)领导了印度技术中心(TCI),这是大陆公司的主要研发中心,为全球所有汽车业务部门提供服务。在印度的三年半期间,TCI发展到了大陆最大的研发地点之一。他于2001年加入公司,在高级产品开发,系统工程,车辆测试,项目管理,客户和产品策略以及创新方面担任领导职务。他的经验包括在美国和日本的作业,并涵盖了与安全相关产品,例如ESC,ADA和Interior产品,例如仪表组和HUD。亚历山大在德国布劳恩斯奇格(Braunschweig)的技术大学Carolo Wilhelmina技术大学学习了机械工程和工商管理(德国外交部Wirtschaftsingenieur)。
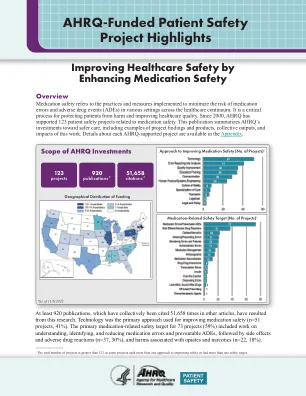
通过提高药物安全性来改善医疗保健安全性
主要发现/影响:最终报告中的建议包括一致使用术语、视觉提示、最少文本、格式、内容和报告标准以促进可用性。专家建议 (1) 一个透明、系统和证据驱动的流程,由专家共识小组分级建议并由国家组织监督;(2) 明智地将 DDI 归类为禁忌症,以及 (3) 进行更多研究以确定安全减少重复和不太相关的警报的方法。项目可交付成果(即工作组白皮书、建议、网络研讨会、会议/会议记录)可以为 DDI CDS 提供有意义的改进,从而减少警报疲劳、改善工作流程、减少用药错误并提高患者安全性。
增强自动驾驶汽车的安全性和安全性-IJRPR
由人工智能和传感器技术的进步推动的自动驾驶汽车的出现正在重塑现代运输的景观。[1]提高安全性,效率和减少交通事故的承诺引发了对自动驾驶汽车开发的浓厚兴趣和投资。[2,3]但是,由于这些车辆在现实世界中驾驶,因此确保其安全性和安全性已成为最重要的问题。本研究论文旨在研究与增强自动驾驶汽车安全性和安全性相关的复杂挑战。[4]虽然潜在的好处是可观的,但必须克服许多障碍,以实现一个未来,即自动驾驶车辆与传统的运输方式无缝共存[5]。本介绍通过概述自动驾驶汽车技术的快速发展,并阐明对安全和保障措施进行全面检查的需求,从而设定了舞台。[6,7]
基于汽车软件的系统的质量,安全性和安全性
亚历山大·克洛茨(Alexander Klotz)是Vitesco Technologies技术合规性(TC)负责人。他负责公司技术合规性管理系统(TCMS)和全球TC策略,该战略旨在检测和减轻与非规范产品(硬件和/或软件)和系统相关的风险。符合VDA产品合规性定义,Vitesco TCMS涵盖了法规,全球标准和考虑有关推导“最新艺术”的相关方面。在他以前在大陆上的职位,亚历山大·克洛兹(Alexander Klotz)领导了印度技术中心(TCI),这是大陆公司的主要研发中心,为全球所有汽车业务部门提供服务。在印度的三年半期间,TCI成长为大陆的最大研发地点之一。他于2001年加入公司,在高级产品开发,系统工程,车辆测试,项目管理,客户和产品策略以及Inno vation领域担任领导职务。他的经验包括在美国和日本的作业,并涵盖了与安全相关产品,例如ESC,ADA和Interior产品,例如仪表组和HUD。亚历山大在德国布劳恩斯奇格(Braunschweig)的技术大学Carolo Wilhelmina技术大学学习了机械工程和工商管理(德国外交部Wirtschaftsingenieur)。