XiaoMi-AI文件搜索系统
World File Search Systemcenobamate对认知的负面影响
方法:我们通过整合多个OMICS数据集对CRC中81个寿命相关基因的影响进行了全面分析。这种分析导致了两种不同的分子亚型的鉴定,并揭示了各个层的寿命相关基因的改变与肿瘤微环境(TME)内的临床病理特征,预后和细胞浸润特性有关。这些模型的培训和验证队列来自TCGA-COAD,TCGA-READ和GSE35279数据集。随后,我们开发了风险评分模型,并采用了Kaplan -Meier方法来估计总体生存(OS)。最终,我们建立了一个基于五个寿命相关基因的预后模型:BEDN3,EXOC3L2,CDKN2A,IL-13和CAPN9。此外,我们评估了风险评分与免疫细胞浸润,微卫星不稳定性和干细胞指数等因素之间的相关性。
医疗政策 - 人类 FIT-DNA 分析(即...
样本作为结直肠癌筛查技术的描述/背景筛查粪便或粪便 DNA(Cologuard TM )检测可检测出结直肠癌和癌前息肉脱落细胞中所含改变 DNA 的分子标记。DNA 检测旨在检测极少量的 DNA 标记,以识别结直肠癌或癌前结直肠肿瘤。该技术是目前可用的筛查方法的另一种潜在替代方案,例如粪便潜血检测、粪便免疫化学检测 (FIT) 和结肠镜检查。目前可用的粪便 DNA 检测结合了 FIT 和 DNA 分析,在本综述中称为 FIT-DNA,尽管其他出版物也使用术语粪便 DNA (sDNA)-FIT 和多目标粪便 DNA (mt-sDNA)。 Cologuard TM 是一种专有的体外诊断多目标 FIT-DNA 测试,它使用一种结合了 DNA 和粪便免疫化学测试技术的设备,旨在分析个人粪便样本中与结直肠癌和癌前结直肠肿瘤相关的标记物。结直肠癌几种细胞基因改变与结直肠癌 (CRC) 有关。在提出的多步骤致癌模型中,肿瘤抑制基因 p53 和原癌基因 KRAS 改变最为频繁。还检测到了腺瘤性结肠息肉 (APC) 基因和表观遗传标记物 (例如特定基因的高甲基化) 的变异。CRC 还与林奇综合征 (以前称为遗传性非息肉病 CRC) 患者和散发性结肠癌患者亚组中微卫星序列 (称为微卫星不稳定性) 中的 DNA 复制错误有关。粪便样本中脱落的肠细胞可检测到肿瘤相关基因变异和表观遗传标记。由于癌细胞会脱落到粪便中,因此已开发出检测粪便样本中分离的脱落 CRC 细胞 DNA 中这些基因变异的检测方法。
332新型TGF-β在转移性结直肠上的特征...
具有微卫星稳定或不匹配修复的患者的背景熟练(MSS/PMMR)转移性结直肠癌,免疫检查点阻断不起作用。正在设计策略,即免疫疗法与其他新型药物或放射疗法结合起来,以增强PD-L1的增强,改变肿瘤微环境(将“冷肿瘤“热”)和/或释放新抗原以增强免疫检查点阻滞的功效。我们选择了YTTrium-90 Radioem-libization(Y90-RE)与固定剂量的免疫疗法相结合,并在Y90-RE前和Y90-RE后作为一种治疗策略作为一种治疗策略,作为临床试验的一部分,用于临床试验的转移性结直肠癌患者,这些患者患有肝脏中率高或肝脏占主导地位或肝脏替代转移剂。Methods This clinical trial will be conducted as a single-cen- ter, open-label, Phase I/2 trial to evaluate the feasibility and safety of Yttrium-90 radioembolization (Y90-RE) in combina- tion with a fixed dose of of immunotherapy (durvalumab - 750 mg) in subjects with liver-predominant, metastatic color- ectal cancer (mCRC), which is不匹配维修熟练/微卫星稳定(PMMR/ MSS)。如临床试验所述。gov,这项临床试验的目的是更多地了解有关免疫疗法的副作用,并在肝脏中对癌症进行了放射性治疗,称为YTTRIUM-90 Radiombolization(Y90-RE)。一种免疫疗法药物,杜瓦鲁马布每2周静脉注射一次。我们正在研究哪种剂量的杜瓦卢马布对这种辐射治疗的组合对人来说是安全的。没有安慰剂。主要目标是研究这种方法的安全性和可行性。这项研究中的患者将接受杜瓦卢马布(Durvalumab),该患者是实验性的,未经美国食品药品监督管理局(FDA)批准转移性结直肠癌。显微镜放遗分子颗粒(Therasphere®)将用于放射性栓塞,以将Y90药物输送到肝脏。研究中的每个人都在Y90-radioembolization并肩作用(表1)。
双重免疫疗法在GI癌中的好处
缩写化学疗法:化学疗法; CI:置信间隔; CR:完全响应; CRC:大肠癌; ctDNA:循环肿瘤DNA; CTLA:细胞毒性T淋巴细胞相关的抗原-4; DMMR:有效的DNA不匹配修复; GI:胃肠道; HCC:肝细胞癌;人力资源:危险比; ICI:免疫检查点抑制剂; IPI:ipilimumab; Len:Lenvatinib; MCRC:转移性结直肠癌; MO:月份; MRD:最小残留疾病; MSI-H:微卫星不稳定性高; NE:无法评估; Nivo:Nivolumab; NR:未报告; NSCLC:非小细胞肺癌; OS:总体生存; PD(L):程序性细胞死亡蛋白(配体)1; PFS:无进展的生存; Q3W:每3周一次; Q4W:每4周一次; SOR:Sorafenib; TRAE:与治疗相关的不良事件。
胆道癌的免疫治疗:值得重新审视
在过去十年中,免疫检查点抑制剂(ICI)的开发阻断了程序性死亡受体 1(PD-1)和细胞毒性 T 淋巴细胞抗原 4(CTLA-4)与其特定配体的相互作用,对肿瘤内科产生了突出的影响。1 有研究表明,程序性死亡配体 1(PD-L1)蛋白表达、错配修复缺陷(dMMR)、肿瘤突变负荷(TMB)和不稳定微卫星(MSI)表型是免疫治疗反应的预测生物标志物。2 简而言之,dMMR / MSI-high 表型与接受 ICI 治疗的患者更高的总体反应率(ORR)和无进展生存期(PFS)相关;同样,许多具有较高 TMB 的实体瘤对免疫疗法的反应也更好。 3 基于这些数据,美国 FDA 于 2017 年批准了抗 PD-1 药物 pembrolizumab,用于治疗任何 dMMR 或 MSI 高恶性肿瘤,无论组织学类型如何。4
未知主要起源癌的全面基因组分析:考虑库比斯科研究设计的回顾性分子分类
背景。未知原始起源(CUP)的癌占新诊断的晚期恶性肿瘤的2% - 5%,并以化学疗法作为护理标准。Cupisco(NCT03498521)是一项正在进行的随机试验,该试验使用全面的基因组亲膜(CGP),将杯赛患者分配给基于基因组亲实现的靶向或免疫疗法治疗臂。,我们对CGP的杯子病例进行了重新观察分析,以确定有多少有资格进入实验性杯状臂的可能有资格。材料和方法。使用基于混合捕获的基础CDX分析(平均覆盖范围,> 600倍)分析了基础库数据库中基础科目数据库中的腺癌和未分化的杯子标本。确定了基因组改变,微卫星不稳定性(MSI),肿瘤突变负担(TMB),杂合性(GLOH)的基因组丧失(GLOH)和程序性死亡 - 结构1(PD-L1)阳性。
RAS 突变和个性化癌症治疗
缩写 Adeno,腺癌;AE,不良事件;CRC,结直肠癌;CUP,原发部位不明的癌症;DCR,疾病控制率;dMMR,错配修复缺陷;EGFR,表皮生长因子受体;EHC,肝外胆管癌;FDA,食品药品管理局;GI-neuro,胃肠神经内分泌;HER2,人类表皮生长因子受体 2;IHC,肝内胆管癌;m,中位数;MDS-MPN,骨髓增生异常-骨髓增生性肿瘤;MOA,作用方式;MSI,微卫星不稳定性;NCCN,国家综合癌症网络;NGS,下一代测序;NSCLC,非小细胞肺癌;ORR,客观缓解率;PDAC,胰腺导管腺癌;PD-L1,程序性死亡配体 1; SOC,标准治疗;Sq,鳞状;TMB,肿瘤突变负担;TRAE,治疗相关不良事件;TTR,缓解时间。
DNA 和 RNA 基 NGS 检测的互补使用优化了临床相关易位的检测,从而实现了全面的基因组分析
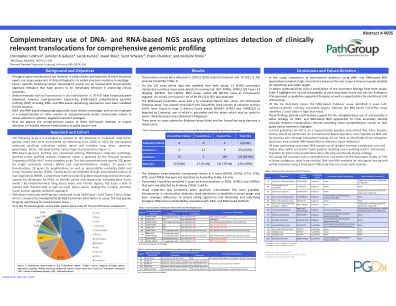
定向肿瘤分析解决方案 Endeavor 由 Personal Genome Diagnostics (PGDx) elio™ 组织完整检测提供支持。该检测全面查询 505 个基因的单核苷酸变异 (SNV) 和插入/缺失 (indel)、23 个基因的易位、28 个基因的扩增以及微卫星不稳定性 (MSI) 和肿瘤突变负担 (TMB)。通过个性化重排末端分析 (PARE) 检测易位,这是一种由 PGDx 开发的专有方法,结合深度测序和生物信息学方法,以识别指示基因融合事件的配对末端测序。1 通过全面覆盖外显子和内含子区域,该检测能够捕获特征明确和新颖的融合事件,使其成为一种高度敏感、与融合伴侣无关的检测方法。• 使用 PathGroup 的实体肿瘤融合检测进行基于 RNA 的分子分析,
lenvatinib(kisplyx)®RMP摘要
lenvima/kisplyx被授权为单一治疗,用于治疗患有局部晚期DTC的成年患者,并治疗未接受过全身治疗的晚期或无法切除的HCC患者。kisplyx与依维莫司(Everolimus)结合使用,用于治疗晚期RCC患者。kisplyx与Pembrolizumab结合使用,用于对患有中间/不利风险特征的晚期(不可切除或转移性)肾细胞癌的成年患者的一线治疗。lenvima与pembrolizumab结合使用,用于治疗成年患者的晚期子宫内膜癌患者,这不是微卫星不稳定性高(MSI-H)或DNA不匹配修复缺陷(DMMR),这些修复缺乏(DMMR)在先前的基于全身性铂治疗并不能候选治疗或放射性的疾病后具有疾病进展。它包含lenvatinib中性化作为活性物质,每天口服一次。
一种可扩展的高通量靶向下一代测序检测方法,用于对实体肿瘤进行全面的基因组分析
测序运行,从收到样本到报告的周转时间不到 7 天。结果表明,可扩展的检测方法可以准确且可重复地检测出 40ng DNA 中的小变异、拷贝数变异、微卫星不稳定性 (MSI) 和肿瘤突变负担 (TMB),以及 20ng RNA 中的多个基因融合,包括已知和未知的伴侣和剪接变体。对 717 个肿瘤样本和参考材料进行了测序,其中 96 个癌症相关基因存在已知变异,以评估检测性能。所有变异类别均能以一致且可报告的变异等位基因百分比可靠地检测到,总体准确度和精确度 > 99%。我们的结果表明,高通量 CGP 检测是一种准确的分子变异检测方法,支持肿瘤学的精准治疗。支持系统和可扩展的工作流程可以每周高效解释和及时报告数百个患者癌症基因组,并具有出色的分析性能。