XiaoMi-AI文件搜索系统
World File Search System减肥胰高血糖素样肽-1(GLP1)激动剂
政策声明 本政策涉及 Saxenda 和 Wegovy 的使用。值得注意的是,本政策不针对其他未获得 FDA 批准的减肥适应症的胰高血糖素样肽-1 激动剂。建议事先授权 Saxenda 的药房福利覆盖范围。建议对符合所提供诊断的标准和初始/延长批准中的覆盖条件的人进行批准。不建议批准的条件列于推荐的授权标准之后。本政策中未列出的用途的请求将根据具体情况进行有效性证据和医疗必要性的审查。所有初始治疗的批准均在下面所述的初始批准期限内提供;如果允许重新授权,则需要对治疗做出反应才能继续治疗,除非下文另有说明。自动化:无。推荐授权标准 I. 建议对符合以下标准的人进行 Saxenda 覆盖范围:FDA 批准的适应症
Ei Yamada,总裁兼首席执行官 Tie2 受体激动剂 (AV-...
AV-001 最初由多伦多 Sunnybrook 医院的 Sunnybrook 研究所发现和设计,目前由 Vasomune Therapeutics, Inc. 根据与 AnGes, Inc. [TYO: 4563] 的联合开发协议进行开发。AV-001 是一种新型研究药物,靶向 Tie2 受体,Tie2 受体是一种跨膜蛋白,在血管内皮细胞表面表达最高。AV-001 激活非冗余 Tie2-血管生成素信号轴,并通过刺激多个下游通路,通过增强内皮细胞稳定性、恢复正常屏障防御和阻止血管渗漏使血管正常化。血管功能障碍是细菌和病毒性急性呼吸窘迫综合征、脓毒症、出血性休克、急性肾损伤、中风和血管性痴呆患者的潜在疾病病理生理学因素。重要的是,在多项临床前研究中,AV-001 加强了内皮细胞与细胞之间的连接并促进了内皮细胞的存活,与未经治疗的对照组相比,这减少了肺水肿,改善了肺功能,从而显著提高了存活率。
胰高血糖素样肽-1(GLP-1)受体激动剂
RA、Einhorn D、Galindo RJ、Gardner TW、Garg R、Garvey WT、Hirsch IB、Hurley DL、Izuora K、Kosiborod M、Olson D、Patel SB、Pop-Busui R、Sadhu AR、Samson SL、Stec C、Tamborlane WV Jr、Tuttle KR、Twining C、Vella A、Vellanki P、Weber SL。美国临床内分泌学会临床实践指南:制定糖尿病综合护理计划 - 2022 年更新。Endocr Pract。2022 年 10 月;28(10):923-1049。doi:10.1016/j.eprac.2022.08.002。
胰像肽-1受体激动剂等胰高血糖素的组合...
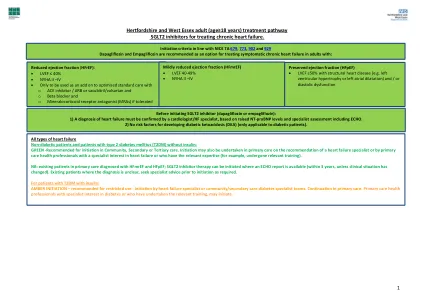
所有类型的心力衰竭非糖尿病患者和2型糖尿病患者(T2DM)没有胰岛素:绿色 - 申请社区,中等或第三次护理的启动。也可以根据心力衰竭专家的建议或具有对心力衰竭的专家或具有相关专业知识的专家(例如,相关培训)的专家兴趣的初级保健专业人员的建议进行。 nb:被诊断为HFMREF和HFPEF的初级保健中的现有患者;可以在可用的回声报告(在3年内,除非临床状况发生变化)之内开始SGLT2抑制剂治疗。 现有诊断尚不清楚的现有患者,请根据需要在启动之前寻求专业建议。 胰岛素T2DM患者:琥珀色启动 - 建议用于限制使用 - 心力衰竭专家或社区/二级护理糖尿病专家团队。 在初级保健中延续。 对糖尿病或接受过相关培训的专业兴趣的初级保健专业人员可能会发起。。nb:被诊断为HFMREF和HFPEF的初级保健中的现有患者;可以在可用的回声报告(在3年内,除非临床状况发生变化)之内开始SGLT2抑制剂治疗。现有诊断尚不清楚的现有患者,请根据需要在启动之前寻求专业建议。胰岛素T2DM患者:琥珀色启动 - 建议用于限制使用 - 心力衰竭专家或社区/二级护理糖尿病专家团队。在初级保健中延续。对糖尿病或接受过相关培训的专业兴趣的初级保健专业人员可能会发起。
T2DM SGLT2抑制剂GLP1激动剂讲义(2023年7月)
1定义2申请2.1首席审计师2.2首席审计师2.3审计计划2.4首席审计师有权委派2.5审计2.5审计2.6审计报告2.6审计报告3首席检查员4督察4的授权权限5校长6任命检查员的权力6任命检查员的权力任命主管7委托人7委托授权的人8权力为竞争者的竞争者8.2竞争者8.2竞争者8.2竞争者8.2竞争者8.2竞争者8.2 9咨询委员会10允许10.1首席检查员对未遵守代码的权力,
胰高血糖素样肽-1受体激动剂和钠...
心力衰竭和认知障碍是由于全球人口老龄化而需要解决的公共卫生问题。经常共存的条件与促进年龄和多种多发病密切相关。流行病学证据表明,在患病率,年龄分布和死亡率方面,心血管疾病和神经退行性过程具有相似的方面。2型糖尿病越来越多地代表了与心脏代谢病理相关的危险因素,而且与神经系统疾病相关。2型糖尿病的病理生理特征及其代谢并发症(高血糖,高胰岛素血症和胰岛素抵抗)在心力衰竭和认知功能障碍的发展和发展中起着至关重要的作用。这种联系已经开放了一种潜在的新策略,在这种策略中,新型的抗糖尿病药物(例如胰高血糖素样肽-1受体(GLP-1R)激动剂和硫化葡萄糖共转运蛋白2(SGLT2)抑制剂,能够减少心血管疾病的总体损害,并降低了其他保护性效应,因此能够降低其他保护性损害。GLP-1R激动剂和SGLT2抑制剂的多效性作用已得到广泛研究。他们通过减少炎症,氧化应激,离子
一种新颖的定义TLR3激动剂为有效的疫苗佐剂
由Toll样受体3(TLR3)识别的合成双链RNA类似物是疫苗的有吸引力的辅助候选者,尤其是针对细胞内病原体或肿瘤,因为它们具有增强T细胞和抗体反应的能力。尽管Poly(I:C)是具有有效辅助性的代表性DSRNA,但由于异质分子大小,活性不一致,稳定性和毒性不一致,其临床应用受到限制。为了克服这些局限性,我们通过使用PCR偶联的双向体外转录开发了一种新型的基于DSRNA的TSRNA TLR3激动剂(NVT)。琼脂糖凝胶电泳和反相HPLC分析表明,NVT是一个单个275 kDa均匀分子。nvt似乎在6个月的加速存储条件下不受影响,因为其外观,浓度和分子大小不受影响。此外,在良好的实验室实践下对毒性的临床前评估表明,NVT是一种安全物质,没有任何严重毒性迹象。NVT刺激了TLR3,并增加了病毒核酸传感器TLR3,MDA-5和RIG-1的表达。当肌肉内注射到C57BL/6小鼠中时,椭圆蛋白(OVA)和NVT高度增加了树突状细胞(DC)的迁移(DC),巨噬细胞和中性粒细胞与单独使用OVA相比。此外,NVT基本上诱导了直流成熟和激活的表型标记,包括MHC-II,CD40,CD80和CD86以及IFN-B的产生。同时,NVT增加了Th1型T细胞的水平,例如IFN-G + CD4 +和IFN-G + CD8 +细胞,响应OVA刺激。此外,NVT表现出适当的辅助性,因为它升高了OVA特异性IgG,尤其是IgG2C(Th1-型)的较高水平,但IgG1较低(Th2-Type)。总的来说,我们建议具有适当安全性和有效性的NVT是一种新颖而有希望的辅助疫苗,尤其是那些需要T细胞介导的免疫力的疫苗,例如病毒和癌症疫苗。
胰高血糖素样肽-1 受体激动剂在妊娠期的使用
胰高血糖素样肽-1受体激动剂是用于治疗2型糖尿病和肥胖症的肽类似物。该类药物中的第一种药物艾塞那肽于2005年获批,这些药物,特别是索马鲁肽,近年来因其对血糖控制、减肥和心血管健康的显著效果而越来越受欢迎。由于这些药物成功减肥,许多之前被诊断为月经稀发且无法怀孕的女性在服用这些药物时经历了意外怀孕。然而,目前临床医生在为意外怀孕期间接触这些药物的患者提供咨询时可用的数据很少。在一些研究中,研究人员对怀孕期间接触胰高血糖素样肽-1受体激动剂的小动物进行了研究,发现这些药物对后代有不良影响,包括胎儿生长迟缓、骨骼和内脏异常以及胚胎死亡。虽然没有对人类进行前瞻性研究,但病例报告、队列研究和基于人群的研究并未显示婴儿先天性异常的模式。最近一项大型观察性、基于人群的队列研究检查了 938 例受 2 型糖尿病影响的妊娠,并比较了围孕期接触胰高血糖素样肽-1 受体激动剂和胰岛素的结果。作者得出结论,服用胰高血糖素样肽-1 受体激动剂的患者发生重大先天畸形的风险没有显著增加,尽管没有关于母亲血糖控制或糖尿病胎儿病变的信息。由于糖尿病胚胎病变与母亲高血糖程度直接相关,而不是糖尿病本身的诊断,因此如果没有这些信息就无法得出这一结论。此外,关于胎儿生长受限、胚胎或胎儿死亡或其他潜在并发症的证据很少。目前,应告知患者,没有足够的证据预测妊娠期间使用胰高血糖素样肽-1 受体激动剂会产生任何不良反应或不会产生不良反应。我们建议所有患者在服用胰高血糖素样肽-1 受体激动剂时采取避孕措施,以防止意外怀孕。
胰高血糖素样肽-1激动剂的现实世界分析(...
GLP-1A治疗持续性,以确定在365天分析期间GLP-1A供应中是否发生了≥60天的差距,而GLP-1A供应的最后一天被定义为该会员的中断日期。如果没有60天的治疗差距,则将成员定义为GLP-1A治疗持续的年度。依从性是通过涵盖的天数(PDC)方法的比例定义的,在365天期间每天评估GLP-1A供应的每天,并将供应量划分为365天。PDC为≥0.8(习惯阈值)的成员被定义为依从性,而PDC <0.8的成员被定义为非贴贴。
类似胰高血糖素的肽-1激动剂事先授权政策
不是治疗的建议,绝不应用作治疗指南。在某些市场中,可以使用委托供应商指南来支持医疗必要性和其他覆盖范围的确定。c Inda n n o n ot formulary c超老化:o verview在该政策中所解决的胰素性肽-1(GLP-1)受体激动剂和GLP-1/依赖性胰岛素胰岛素多肽-1(GIP)激动剂在该政策中所解决的胰岛素疗法均表明是饮食和锻炼的辅助性,以改善与gocemection inty-type inty类型2的助攻。1-8 liraglutide,Trulicity和Bydureon bcise还针对≥10岁的患者的2型糖尿病还指出。3,7,8 Liraglutide,Ozempic和Trulicity还标记了与2型糖尿病成人心血管(CV)降低心血管风险有关的适应症。5,7,8