XiaoMi-AI文件搜索系统
World File Search System测试一种新型靶向放射疗法 123I-ATT001,该疗法直接作用于之前治疗后复发的胶质母细胞瘤患者的脑肿瘤
仅限第 1 部分的次要结果测量:1. 为确定 123I-ATT001 的生物分布和药代动力学,将从第 1 部分的前 6 名患者采集血液和尿液样本。血液样本将在每次服药后 1 小时、4 小时和 24 小时采集,也可选择在首次服药后 48 小时采集。尿液样本仅在首次服药后 24 小时采集。2. 为确定 123I-ATT001 的辐射剂量(每个器官暴露于辐射):2.1. 全身和大脑 SPECT/CT 成像将在每次服药后 1 小时进行 2.2. 每次服药后 4 小时进行全身和大脑 SPECT 2.3. 仅大脑 SPECT 将在注射首次剂量后 24 小时进行 2.4. 可选择在注射首次剂量后 48 小时拍摄大脑 SPECT 图像 2.5.注射第四剂后 4 小时 ±30 分钟将进行仅脑部 SPECT 检查
观点:透皮给药贴剂中的材料和电子差距
透皮给药系统提供了一种通过皮肤表面输送药物的非侵入性方法,从而避免了与代谢分解、初始给药后无法控制的生物分布以及患者依从性有限的问题相关的问题。最常见的透皮给药工具是透皮贴剂 (TDP),它是一种灵活的药用粘性贴剂,可以放置在任何可用的皮肤表面进行靶向给药。从这个角度来看,我们总结了透皮给药贴剂的最新进展,并强调了可以通过先进的传感器开发填补的空白。© 2024 作者。由 IOP Publishing Limited 代表电化学学会出版。这是一篇开放获取的文章,根据知识共享署名 4.0 许可条款分发(CC BY,https://creativecommons.org/licenses/by/4.0/),允许在任何媒体中不受限制地重复使用作品,前提是正确引用原始作品。 [DOI:10.1149/2754-2726/ad8b5a]
通过合成的 PEG12-KL4 肽将针对 PD-L1 和 EGFR 的 siRNA 共同递送至肺部,作为治疗非小细胞肺癌的潜在策略
背景:小干扰 RNA (siRNA) 在治疗各种肺部疾病方面具有巨大潜力,但缺乏安全有效的肺部 siRNA 递送系统阻碍了其进入临床。促进细胞增殖的表皮生长因子受体 (EGFR) 和在抑制细胞毒性 T 细胞活性中起关键作用的程序性细胞死亡配体 1 (PD-L1) 是治疗非小细胞肺癌 (NSCLC) 的两个重要靶点。在这里,我们探索了合成肽 PEG 12-KL4 将 siRNA 递送到小鼠的各种 NSCLC 细胞和肺组织的潜力。方法:使用 PEG 12-KL4 将针对 EGFR 和 PD-L1 的 siRNA 转染到 NSCLC 细胞中。使用免疫印迹法评估 siRNA 在 HCC827 和 NCI-H1975 NSCLC 细胞中的沉默效果。采用 CD8 + T 细胞介导的 NSCLC 细胞杀伤来证明 PD-L1 siRNA 敲低的功能效果。使用荧光 siRNA 来可视化细胞中的 siRNA 摄取,并在 BALB/c 小鼠中进行生物分布研究。结果:我们的结果表明,PEG 12 -KL4 可有效介导各种 NSCLC 细胞中 EGFR 和 PD-L1 的 siRNA 敲低。重要的是,PEG 12 -KL4 肽比商用 Lipofectamine 2000 试剂能够更好地实现 siRNA 递送。我们假设 PEG 12 -KL4 肽使 siRNA 能够逃脱或绕过内体降解,如共聚焦荧光成像所示。值得注意的是,在 NCI-H1975 细胞中联合敲低 EGFR 和 PD-L1 比单独敲低 PD-L1 产生更好的效应 T 细胞介导的癌细胞杀伤效果。此外,静脉给药后 PEG 12 -KL4/siRNA 复合物的生物分布表明肺部输送不良,荧光 siRNA 积聚在肝脏中。相反,气管内输送 PEG 12 -KL4/siRNA 复合物导致荧光 siRNA 在肺部被检测到,肾脏排泄延迟。结论:总之,我们证明了使用 PEG 12 -KL4 共同输送靶向 EGFR 和 PD-L1 的 siRNA 是可行的,并且代表了治疗 NSCLC 的一种有前途的未来策略,其中肺部 siRNA 输送有利于静脉给药。
开发CD163靶向的PET放射性示例,该pet radiotracer在动脉粥样硬化中驻留巨噬细胞
组织居民巨噬细胞是辅助巨噬细胞的补充,以促进动脉粥样硬化的进展。对它们的存在和动态变异的非侵入性检测对于理解其在急剧发病机理中的作用至关重要。这项研究的目的是开发一种靶向的PET放射性示踪剂,用于成像多种小鼠动脉粥样硬化模型中的CD163阳性(CD163 1)巨噬细胞,并评估CD163作为人类动脉粥样硬化的生物标志物的潜力。方法:使用噬菌体显示鉴定CD163结合肽,并与64 Cu radiolabeling的Nodaga螯合剂([[64 CU] CU-ICT-01)结合。过表达的U87细胞用于测量[64 Cu] Cu-ICT-01的结合属性。在尾静脉注射后多个时间点对野生型C57BL/6小鼠进行了生物分布研究。在多个小鼠动脉粥样硬化模型中评估了[64 cu] cu-ict-01的敏感性和特异性cu-ict-01 1巨噬细胞在动脉粥样硬化斑块上上调的巨噬细胞。免疫染色,流量细胞仪和单细胞RNA测序,以表征CD163在组织居民巨噬细胞上的表达。人类颈动脉粥样硬化斑块用于测量CD163 1驻留巨噬细胞的表达,并测试[64 Cu] Cu-Ict-01的结合质量。结果:[64 Cu] Cu-Ict-01显示出高度与U87细胞的结合。生物分布研究表明,注射后1、2和4H的所有主要器官的肾脏迅速清除率较低。在APOE 2 /2小鼠模型中,[64 Cu] Cu-Ict-01示例敏感和特定检测CD163 1巨噬细胞以及跟踪动脉粥样硬化病变进展的能力;这些发现在LDLR 2 /2和PCSK9小鼠模型中进一步确认。免疫染色显示CD163 1巨噬细胞的表达升高。流式细胞仪和单细胞RNA测序确认CD163在组织居民宏观上的特定表达。人体组织表征表现出CD163 1巨噬细胞在动脉粥样硬化病变上的高表达,而离体自动二仪显示[64 CU] CU-ICT-01与人CD163的特定结合。结论:这项工作报告了PET放射性示意剂结合CD163 1巨噬细胞的发展。CD163 1在人斑块上驻留的巨噬细胞的表达升高,表明CD163的潜力是易受攻击的斑块的生物标志物。在成像CD163中[64 Cu] Cu-Ict-01的敏感性和特异性1巨噬细胞在转化环境中进行进一步研究。
靶向GD2-阳性肿瘤的药物缀合物
抽象背景是神经节苷脂靶向的免疫疗法和抗体 - 药物结合物(ADC)在近年来表现出临床成功,但近年来尚未进行研究以开发抗GD2 ADC针对实体瘤。这是第一个分析在宽的细胞系中临床相关的抗GD2 ADC的细胞毒性活性的研究,其GD2表达不同及其在GD2-阳性固体癌的小鼠模型中的作用。方法是基于GD2特异性抗体CH14.18生成的抗GD2 ADC,该抗体批准用于治疗神经母细胞瘤和常用药物单甲基极氨基蛋白E(MMAE)或F(MMAF),通过Thiol-Maleimide cleachiol-Maleimide Chine偶联。抗体是在哺乳动物表达系统中产生的,并分析了其与GD2的特异性结合。与母体抗体相比,研究了小鼠ADC的抗原结合特性和ADC的生物分布。在神经母细胞瘤,神经胶质瘤,肉瘤,黑色素瘤和乳腺癌的GD2阳性和GD2阴性肿瘤细胞系中评估了ADC的细胞毒性作用。在B78-D14黑色素瘤和EL-4淋巴瘤合成小鼠模型中研究了它们的抗肿瘤作用。结果CH14.18-MMAE和CH14.18-MMAF ADC保留了母体抗体的抗原结合特性。在两种ADC的不同原点的细胞系中观察到细胞毒性作用对GD2表达水平的直接依赖性,对于GD2表达较高的细胞,IC50低于1 nm,对于GD2-阴性细胞没有细胞毒性效应。在分析的细胞系中,CH14.18- MMAF在过表达GD2的细胞中更有效,而CH14.18-MMAE在表达较低GD2水平的细胞中具有更突出的活性。与母体抗体相比,ADC在B78-D14黑色素瘤模型中具有相似的生物分布曲线,在注射后48小时时,肿瘤中的ID/G达到7.7%。与对照组相比,用CH14.18-MMAE或CH14.18-MMAF治疗的组平均肿瘤大小分别小的2.6倍和3.8倍。在EL-4淋巴瘤模型中也证实了抗GD2 ADC的抗肿瘤作用。结论这些发现验证了靶向神经节苷脂GD2在处理多种GD2表达实体瘤的ADC的潜力。
Petri-Med:基于卫星的监测,对地中海海中的微生物浮游生物生物多样性
对微生物浮游生物生物多样性的评估和监测对于获得对海洋环境的健康状况的良好评估至关重要。PETRI-MED项目通过制定新的策略来根据卫星观测来监测微生物浮游生物群落组成和功能来解决这一必要。培养皿将专注于地中海作为具有深远的生态和文化重要性的全球生物多样性热点。Petri-Med项目的主要目标包括(i)基于创新的卫星指标的开发,以确定微生物浮游生物社区的生物多样性状态和趋势,(ii)鉴定微生物浮游生物分布和多样性的微生物浮游生物分布和(iii)的自然连接式的生物群体及其多样性范围的范围,包括生物群体的自然连接,包括生物群的自然连接,包括生物范围。通过关注海洋健康和/或生物地球化学状态的关键指标。这样做,培养皿将主要依赖卫星光学放射测量(即海洋颜色,OC),从而利用最新OC欧洲数据集的时间和空间特征(即,由copernicus sentinel-3和欧洲航天机构的OC-CCI)具有偏僻的隔离式观察(即copernicus Sentinel-3和欧洲航天机构),并具有偏僻的海拔(AS-Art Space)。电流建模和基因组技术。为了实现合并遥感,生物地球化学/物理建模以及原位测量测量的雄心勃勃的目标,Petri-Med将依靠人工智能(AI)。PETRI-MED的总体目标是使决策者和利益相关者获得必要的知识,以根据定量的实时指标对生态系统管理采用优先级别方法。这包括保护和实施保护策略和政策,以保护生物多样性,量化各个层面实施的行动的影响,并为海洋保护区(MPA)(MPA),关键生物多样性领域以及生态或生物学上重要的海洋领域提供系统的,事实支持的事实支持。此外,彼得索(Petrimed)试图评估MPA管理对气候变化的可行性,从而确保在面对环境挑战时为保护海洋生态系统的保护策略。总而言之,PETRI-MED代表了一种全面而创新的方法,可以促进我们对地中海中微生物浮游生物生物多样性的理解。通过卫星技术,法学技术和AI的整合,该项目为有效的海洋生态系统管理和保护策略提供了宝贵的见解和工具。
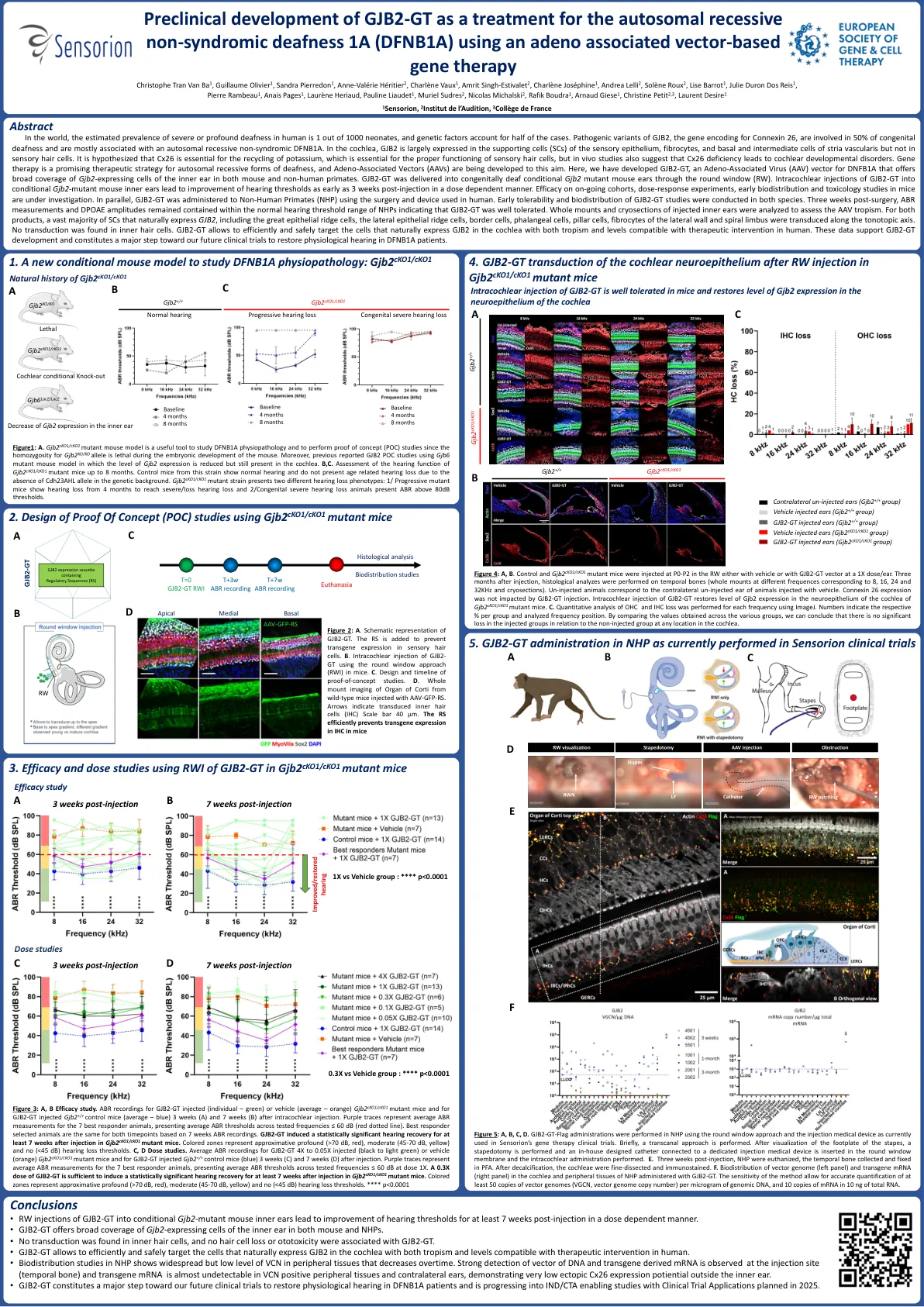
GJB2-GT作为... 的临床前开发 sens-501常染色体隐性非... 的基因治疗
在世界上,人类严重或深刻的耳聋的估计患病率是1000名新生儿中的1个,遗传因素占了一半的病例。 GJB2的致病变异,编码连接蛋白26的基因,涉及50%的先天性耳聋,主要与常染色体隐性遗传性非伴有伴有伴有dfnb1a有关。 在耳蜗中,GJB2在感官上皮,纤维细胞,基底和中间细胞的血管毛血管的辅助细胞(SC)中主要表达,但在感觉毛细胞中却没有。 据推测,CX26对于钾的回收至关重要,这对于感觉毛细胞的正确功能至关重要,但是体内研究还表明CX26缺乏会导致耳蜗发育障碍。 基因疗法是一种有前途的聋哑形式的有前途的治疗策略,并且正在为此目的而开发与腺相关的载体(AAV)(AAVS)。 在这里,我们开发了GJB2-GT,这是DNFB1A的腺相关病毒(AAV)载体(AAV)载体,可在小鼠和非人类灵长类动物中均提供GJB2表达内耳gjb2表达细胞的广泛覆盖范围。 gjb2-gt通过圆形窗口(RW)传递到先天性聋哑的GJB2突变小鼠耳朵中。 对条件GJB2的gjb2-GT对有条件的小鼠内耳的注射会导致听力阈值在注射后3周以剂量依赖的方式改善。 对持续的队列,剂量反应实验,早期生物分布和毒理学研究的功效正在研究中。 并行,使用人类使用的手术和装置将GJB2-GT用于非人类灵长类动物(NHP)。在世界上,人类严重或深刻的耳聋的估计患病率是1000名新生儿中的1个,遗传因素占了一半的病例。GJB2的致病变异,编码连接蛋白26的基因,涉及50%的先天性耳聋,主要与常染色体隐性遗传性非伴有伴有伴有dfnb1a有关。在耳蜗中,GJB2在感官上皮,纤维细胞,基底和中间细胞的血管毛血管的辅助细胞(SC)中主要表达,但在感觉毛细胞中却没有。据推测,CX26对于钾的回收至关重要,这对于感觉毛细胞的正确功能至关重要,但是体内研究还表明CX26缺乏会导致耳蜗发育障碍。基因疗法是一种有前途的聋哑形式的有前途的治疗策略,并且正在为此目的而开发与腺相关的载体(AAV)(AAVS)。在这里,我们开发了GJB2-GT,这是DNFB1A的腺相关病毒(AAV)载体(AAV)载体,可在小鼠和非人类灵长类动物中均提供GJB2表达内耳gjb2表达细胞的广泛覆盖范围。gjb2-gt通过圆形窗口(RW)传递到先天性聋哑的GJB2突变小鼠耳朵中。对条件GJB2的gjb2-GT对有条件的小鼠内耳的注射会导致听力阈值在注射后3周以剂量依赖的方式改善。对持续的队列,剂量反应实验,早期生物分布和毒理学研究的功效正在研究中。并行,使用人类使用的手术和装置将GJB2-GT用于非人类灵长类动物(NHP)。在这两种物种中均进行了GJB2-GT研究的早期耐受性和生物分布。 手术后三周,ABR测量和DPOAE振幅保留在NHP的正常听力阈值范围内,表明GJB2-GT耐受性良好。 分析了注射的内耳的整个安装和冷冻切片,以评估AAV的偏向主义。 对于这两种产品,绝大多数自然表达GJB2的SC,包括大上皮脊细胞,侧皮脊细胞,边界细胞,圆锥细胞,柱状细胞,侧壁的纤维细胞,侧壁和螺旋状肢体的纤维细胞沿着负轴轴线进行传播。 在内毛细胞中未发现转导。 GJB2-GT允许有效,安全地靶向自然表达GJB2在耳蜗中的细胞,并具有与人类治疗干预兼容的水平。 这些数据支持GJB2-GT开发,并构成了我们未来的临床试验迈出的重大步骤,以恢复DFNB1A患者的生理听力。在这两种物种中均进行了GJB2-GT研究的早期耐受性和生物分布。手术后三周,ABR测量和DPOAE振幅保留在NHP的正常听力阈值范围内,表明GJB2-GT耐受性良好。分析了注射的内耳的整个安装和冷冻切片,以评估AAV的偏向主义。对于这两种产品,绝大多数自然表达GJB2的SC,包括大上皮脊细胞,侧皮脊细胞,边界细胞,圆锥细胞,柱状细胞,侧壁的纤维细胞,侧壁和螺旋状肢体的纤维细胞沿着负轴轴线进行传播。在内毛细胞中未发现转导。GJB2-GT允许有效,安全地靶向自然表达GJB2在耳蜗中的细胞,并具有与人类治疗干预兼容的水平。这些数据支持GJB2-GT开发,并构成了我们未来的临床试验迈出的重大步骤,以恢复DFNB1A患者的生理听力。
dgcr2靶向用于将药物和成像试剂递送到人β细胞的成像试剂
digeorge综合征临界区域基因2(DGCR2)蛋白已被认为是胰腺中的β细胞特异性蛋白,但到目前为止,缺乏适用于靶向药物或分子成像的可用高亲和力粘合剂。杂物分子属于一类小亲和力蛋白,具有出色的分子成像特性。在这里,我们进一步验证了胰腺和干细胞(SC)衍生的β细胞中DGCR2的存在,然后描述靶向人DGCR2的几种候选候选物的产生和选择。使用内部开发的定向进化方法,生成了新的DGCR2结合分子并评估了热稳定性和亲和力。杂物分子变体进一步开发为将成像试剂传递到β细胞的靶向剂。Affibody分子Z DGCR2:AM106显示纳摩尔亲和力,合适的稳定性和生物分布,对胰岛的毒性可忽略不计,将其作为用于进一步开发的合适铅候选者,作为用于特定药物递送和对Beta细胞成像的特定递送的工具。
血脑屏障微流控体外三维动态模型用于研究免疫细胞的迁移
摘要:为了研究新化学和生物实体的生物分布,血脑屏障 (BBB) 的体外模型可能成为药物发现早期阶段的重要工具。在这里,我们展示了我们设计的内部三维 BBB 生物芯片的概念验证。这种三维动态 BBB 模型由内皮细胞和星形胶质细胞组成,它们在模拟血流的流动条件下共培养在聚合物涂层膜的相对两侧。我们的结果证明了 BBB 非常有效,证据是 (i) 跨内皮电阻 (TEER) 增加了 30 倍,(ii) 紧密连接蛋白的表达显著增加,以及 (iii) 与静态体外 BBB 模型相比,我们的技术解决方案具有较低的 FITC-葡聚糖渗透性。重要的是,我们的三维 BBB 模型有效地表达了 P-糖蛋白 (Pg-p),这是脑源性内皮细胞的标志性特征。总之,我们在此提供了一种完整的整体方法和对整个 BBB 系统的见解,可能在临床和制药领域带来转化意义。
通过超声转化阿霉素的化学结构和生物纳米活性,以选择性杀死癌细胞
纳米果通常结合活性治疗剂的功能和纳米级载体,以控制肿瘤中药物的药物,生物分布和细胞靶向肿瘤中的药物,同时在健康组织中具有细胞毒性作用。[1]从硅设计到临床试验的新药或纳米果的开发,仍然具有挑战性,冗长且昂贵,对于新的治疗剂而言,不确定性高度不确定性,以使市场进入市场并最终使患者受益。[2]临床试验中的大多数化学治疗纳米果或批准用于使用的纳米果是基于脂质或胶束配方,并结合了标准的非聚体抗癌药物,例如阿霉素(DOX),伊立替康,伊里诺特克氏菌,帕克里塔克塞尔,帕克利塔克塞尔和cisplatin和cisplatin。[3]高级且复杂的纳米载体,例如碳和聚合物的纳米圆柱,中孔无机材料,金属有机框架以及DNA和