XiaoMi-AI文件搜索系统
World File Search System干细胞报告
精原干细胞 (SSC) 是生产转基因动物的资源。然而,对 SSC 的基因操作取得的成功有限。在这里,我们展示了通过慢病毒 (FV-LV) 使用融合蛋白 (F) 将基因有效转移到 SSC 中,融合蛋白是一种参与病毒体/细胞膜融合的仙台病毒 (SV) 包膜蛋白。FV-LV 比传统 LV 更有效地转导培养的 SSC。虽然感染 SV 的 SSC 无法产生后代,但用 FV-LV 转导的 SSC 具有生育能力。体内微注射表明 FV-LV 不仅可以穿透曲细精管的基底膜,还可以穿透血睾屏障,从而成功转导生精细胞和睾丸体细胞。用表达针对 Kit 或 Sycp3 的药物诱导型 CRISPR/Cas9 的 FV-LV 转染培养的 SSC 在移植和体内药物治疗后表现出精子发生受损。因此,FV-LV 为涉及 SSC 和精子发生的基因的功能分析提供了一种有效的方法。
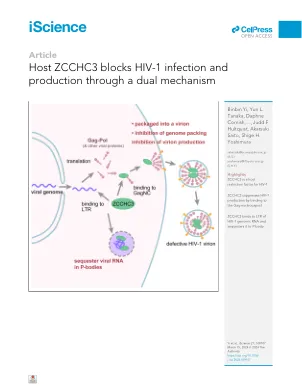
主机ZCCHC3通过双重机制阻止了HIV-1感染和生产
总结大多数哺乳动物细胞通过表达激活免疫系统的各种限制因子和传感器来防止病毒感染和增殖。已经鉴定出抑制人类免疫缺陷病毒1型(HIV-1)的几种宿主限制因子,但大多数人都被病毒蛋白拮抗。在这里,我们以CCHC型锌 - 纤维纤维蛋白3(ZCCHC3)为抑制HIV-1和其他逆转录病毒的产生的新型HIV-1限制性FACER,但似乎并未被病毒蛋白直接拮抗。它通过通过锌 - 纤维基序与GAG Nucleocapsid(GAGNC)结合起作用,该基序抑制了病毒基因组募集并导致基因组较高的病毒体产生。ZCCHC3还通过中间折叠结构域与病毒基因组上的长时间重复结合,将病毒基因组隔离为P体,从而导致病毒复制和产生减少。这种独特的双作用抗病毒机制构成了ZCCHC3的上调,这是一种新型的潜在治疗策略。
黄热病毒和黄热病疫苗
• 科:黄病毒科;黄病毒属。• 形态:有包膜的球形颗粒,直径 40-60 纳米,具有二十面体核衣壳对称性和表面突起;病毒体含有三种结构蛋白:C(衣壳)、E(主要包膜蛋白)和 M(膜),并产生七种非结构蛋白。M 蛋白是病毒成熟过程中产生的前体 (pr)M 蛋白的小蛋白水解片段。黄热病毒有一种血清型,与七种基因型有关。• 核酸:线性、正义、单链 RNA,长 11 kb • 物理化学特性:在 >56°C 下加热 10 分钟灭活;37°C 下半衰期为 7 小时;对脂质溶剂、去垢剂、乙醚、胰蛋白酶、氯仿、甲醛和β-丙内酯敏感;暴露于辐射后传染性降低,在pH 1 – 3时失活。
FLUZONE® 高剂量四价
FLUZONE ® 高剂量四价疫苗 [流感病毒疫苗四价 A 型和 B 型(裂解病毒体)] 是一种用于肌肉注射的灭活流感病毒无菌水悬浮液。FLUZONE ® 高剂量四价疫苗含有 4 种在鸡胚中繁殖的流感病毒。收集含病毒的液体并用甲醛灭活。使用连续流离心机在线性蔗糖密度梯度溶液中浓缩和纯化流感病毒。然后使用非离子表面活性剂辛基酚聚氧乙烯醚(辛基酚-9、Triton® X-100)对病毒进行化学破坏,产生“裂解病毒”。然后通过对磷酸盐缓冲氯化物盐水进行透析过滤进一步纯化裂解病毒。 FLUZONE ® 高剂量四价疫苗每 0.7 毫升剂量含有 240 微克 (μg) 血凝素,推荐比例为四种流感病毒株(A/H3N2、A/H1N1、B/Yamagata 类和 B/Victoria 类)各含 60 μg HA。
病毒
病毒在结构上比单细胞微生物更小,更简单,并且它们仅包含一种核酸(无论是DNA或RNA)。由于病毒没有核糖体,线粒体或其他细胞器,因此它们完全取决于其细胞宿主的能量生产和蛋白质合成。它们仅在宿主感染的宿主细胞内复制。与任何微生物不同,在合适的细胞中,许多病毒可以从基因组中繁殖,即单个核酸分子,即单独的核酸是传染性的。在易感细胞外,像细菌孢子一样的病毒颗粒是代谢惰性的。另一方面,在细胞中复制时,它表现出生命的所有特征。新的微生物群称为可过滤病毒。过滤研究表明,病毒颗粒(病毒体)的范围从最小的单细胞微生物(300 nm)的大小到比最大的蛋白质分子(20 nm)大的物体。在较简单的病毒中,病毒粒子由一个核酸分子组成,该核酸被蛋白质涂层包围。衣壳及其封闭的核酸一起构成核素。
apobecs:我们的善变的朋友?
载脂蛋白B mRNA编辑催化多肽(APOBEC)家族指定多种胞苷脱氨酶。在哺乳动物中,至少5个基因编码Apobecs 1,2,3,4,而激活诱导的胞苷脱氨酶(AID)[1,2]。A1酶是第一个被重新认可的酶,并且在特定宿主mRNA的组织特异性编辑中起着至关重要的作用[3],但是尚未确定在病毒基因的诱变中的确认作用。人类已经扩增了APOBEC3(A3)基因座,以产生7个成员:A3A,A3B,A3C,A3D,A3D,A3F,A3G,A3G和A3H。所有APOBEC蛋白似乎与单链RNA或DNA或两者都结合[1,2]。apo-bec酶在细胞学上脱氨酸单链核酸,导致C-TO-U突变。当这些突变发生在重复病毒的减去链上时,结果是病毒和链的g- to-a转变。由于这些过渡通常会导致胡说八道或误导性突变,因此基本病毒基因产物的合成被阻断,传染性颗粒产量下降[1,2]。在反应中,病毒产生多种基因,干扰A3蛋白的功能。通常,这些是蛋白质拮抗剂,包括HIV-1 VIF的众所周知的例子,它充当了E3连接酶诱导某些A3脱氨酸酶的蛋白酶体降解的适配器[4-7]。此示例提供了明确的证据,表明A3基因的功能是干扰病毒复制。A3s在淋巴样和髓样细胞中似乎以较高的量表示[8-10],这表明这些酶是病毒入侵的前线防御者。然而,其他细胞类型(例如乳腺细胞)也表达A3 [11]。由于某些A3被包装到病毒颗粒中,因此,A3S的病毒体掺入为摄入牛奶传播病毒的新生儿提供了额外的概念。尽管逆转录病毒DNA的脱氨基可能是病毒抑制的主要机制,但已经观察到了脱氨基依赖性的APOBEC活性模式[12,13]。由于A3S与包装到病毒体中的单链RNA结合,因此这些脱氨酶为病毒DNA合成提供了路障[13-15]。A3G还与HIV-1反向转纹酶(RT)相互作用,以干扰DNA复制[16]。不同的APOBEC可能已经演变为允许与RT以外的逆转录病毒酶结合。A3酶也已显示可分别抑制含DNA和RNA的病毒,例如人乳头状瘤病毒和冠状病毒[13-15]。APOBEC与其他病毒聚合酶的结合将为阻断各种病毒的复制提供充足的机会。
C-JUN的磷酸化状态和DNA结合活性取决于结合位点的细胞内浓度
腺病毒5 WA蛋白复合物是从病毒体中分离出来的,作为双链wra分子,由每条链的5'末端共同连接到Imknawn功能的Virion蛋白上。可以用大肠杆菌异核酸酶III消化WA-蛋白质复合物,以产生类似于WA复制中间体的NOLECULES,因为它们包含长长的单个绞线区域,以5'tenmini结合到最高的蛋白质。非核酸酶III消化大大降低了原酶消化腺病毒5 WNA的感染性。hawever,当至少2400个核苷酸被重重载时,KA蛋白复合物的感染性不会显着改变。这表明末端蛋白可以通过细胞外切核酸酶保护5'终止的单链fran消化。DNA-蛋白质复型从宿主范围突变体制备,其左4%的突变映射与外切核酸外切酶III消化,与野生型限制性片段杂交,将左8%的GENANE片段与HELA细胞旋转。具有野生型表型的病毒以高频回收。
聚合物微阵列快速识别竞争性...
聚合物微阵列可快速识别病毒样颗粒(VLP)的竞争性吸附剂 Andrew J. Blok, 1 Pratik Gurnani, 1 Alex Xenopoulos, 2 Laurence Burroughs, 3 Joshua. Duncan, 4,5 Richard A. Urbanowicz, 4,5 Theocharis Tsoleridis, 4,5 Helena Müller, 6 Thomas Strecker, 6 Jonathan K. Ball, 4,5 Cameron Alexander 1 和 Morgan R. Alexander 3 1 诺丁汉大学药学院分子治疗与制剂系,诺丁汉,NG7 2RD,英国。 2 EMD Millipore,80 Ashby Road,贝德福德,马萨诸塞州 01730,美国。 3 诺丁汉大学药学院先进材料与医疗技术系,NG7 2RD,英国。 4 诺丁汉大学医学与健康科学学院沃尔夫森全球病毒研究中心,NG7 2RD,英国。5 诺丁汉生物医学研究中心,诺丁汉女王医疗中心南区 C 楼,NG7 2UH 6 菲利普斯大学马尔堡病毒学研究所,德国马尔堡 摘要 SARS-CoV-2 的出现凸显了全球对平台技术的需求,以便快速开发诊断、疫苗、治疗和个人防护设备 (PPE)。然而,许多当前的技术需要对特定材料-病毒体相互作用的详细机制知识才能使用,例如帮助纯化疫苗成分,或设计更有效的 PPE。在这里,我们展示了一种用于筛选细菌-表面相互作用的聚合物微阵列方法,可以筛选出具有所需材料-病毒体相互作用的聚合物。包括荧光团在内的非致病性病毒样颗粒在水性缓冲液中暴露于阵列,作为唾液/痰液中携带到表面的病毒体的简单模型。测量拉沙病毒和风疹病毒颗粒的竞争性结合,以探测所选共聚物的相对结合特性。这为开发一种有望用于病毒结合的新材料的方法提供了第一步,下一步是开发这种方法来评估绝对病毒吸附和评估活病毒活性的衰减,我们建议将其作为材料放大步骤的一部分,在生物实验室安全 4 级设施中进行,并使用更复杂的介质来代表生物流体。正文 诊断中选择性生物分子识别的常用策略通常利用抗原-抗体相互作用,例如常见的 ELISA 免疫测定。1, 2 虽然这些测定通常可以获得高选择性,但存在许多缺点限制了它们的更广泛使用,包括制造成本(每种抗原都需要开发一种特定的抗体)以及通常对热敏感的试剂的储存和运输。当目标应用需要与相关生物分子类别而不是特定的单个分析物相互作用时,这些缺点变得更加重要。先前的研究已经使用低成本聚合物来修饰纳米晶体 3 和色谱材料 4,5,目的是引入对病毒靶标的广谱结合亲和力。然而,即使是从少量单体衍生的无数假定共聚物结构也意味着迄今为止,仅探索了可用于聚合物亲和剂和生物分子螯合剂的化学空间的一小部分。聚合物微阵列已经开发出来,以便同时研究单个表面上数千种化学上独特的材料的生物材料亲和力 6-13 。这种高通量方法现已用于识别用于一系列生物医学应用的材料,例如抑制细菌生物膜形成 13 和具有可控行为的干细胞生长 8 。聚合物微阵列可通过喷墨或接触印刷轻松制造,并结合少量商用光固化单体的原位聚合。6 在本研究中,我们提出了一种基于聚合物微阵列平台的方法,用于快速识别源自市售单体的材料,这些材料能够对病毒样颗粒进行差异吸附
限制 COVID-19 室内空气传播的指南
当前美国经济的复苏取决于保持社交距离,尤其是“六英尺规则”,这项准则对于防止室内空间中不断混合的载有病原体的气溶胶飞沫几乎无法起到保护作用。如今,人们已广泛认识到 COVID-19 空气传播的重要性。虽然最近已经开发出风险评估工具,但尚未提出任何安全准则来防范这种传播。我们在此基于空气传播疾病的模型,以得出室内安全准则,该准则将对“累积暴露时间”设定上限,即居住者人数与其在封闭空间中待的时间的乘积。我们展示了这个界限如何取决于通风和空气过滤率、房间尺寸、呼吸频率、居住者的呼吸活动和口罩使用情况以及呼吸道气溶胶的传染性。通过综合最具代表性的室内传播事件的可用数据和呼吸道飞沫大小分布,我们估计感染剂量约为 10 个气溶胶传播的病毒体。因此,可以推断新病毒(严重急性呼吸综合征冠状病毒 2 [SARS-CoV-2])的传染性比其前身(SARS-CoV)高一个数量级,这与 COVID-19 的大流行状态一致。针对教室和养老院提供了案例研究,并提供了电子表格和在线应用程序以方便使用
教学大纲
定位。4。基于细胞/细胞器的靶向:线粒体,核靶向,淋巴管/M细胞,肝实质细胞/巨噬细胞,肝细胞和骨髓细胞。5。靶向的物理化学方法:刺激反应:磁性,热和pH辅助药物输送系统,化学药物输送(前药),脂质 - 药物/聚合物药物缀合物。6。基于载体的靶向药物输送方法:功能化的脂质体,聚合物和脂质纳米颗粒,液晶纳米颗粒,聚合物胶束,功能化碳纳米管和无机纳米颗粒。7。基因输送:基因递送的障碍,基于病毒和非病毒载体的新方法,用于特定基因的基因递送,其优势和局限性,siRNA递送。8。纳米载体的高级表征技术:纳米级表征技术,纳米颗粒的生物物理表征和体内成像技术荧光伽玛闪烁图,X射线。9。杂物主题:乳液,转移体,齿状体,双胞胎体,病毒体等的新兴作用等。用于药物/大分子递送。10。纳米毒理学和调节问题:纳米载体的毒性和调节障碍,肺中的纳米毒性。