XiaoMi-AI文件搜索系统
World File Search System水配位聚合物配合物
1维(1D)配位聚合物指的是通过金属结合配体组中掺入金属离子或主链中的金属离子的大分子。,由于金属配体键的性质,它们比传统聚合物具有调节聚合物结构和功能的内在优势。因此,它们具有智能和功能结构以及伴随剂和治疗剂的巨大潜力。水溶性的1D配位聚合物和组件是协调聚合物的重要亚型,具有与生物和医疗应用等水性系统中苛刻应用的独特兴趣。本评论重点介绍了水溶性1D协调聚合物和组件的最新进展和研究成就。概述涵盖了1D配位聚合物的设计和结构控制,它们的胶体组件,包括纳米颗粒,纳米纤维,胶束和囊泡,以及制造的散装材料,例如膜无液体冷凝器,安全墨水,水凝胶驱动器和智能面料。最后,我们讨论了这些坐标国家聚合物结构和材料中几个的潜在应用,并在水性坐标聚合物的领域中展现出前景。
结合miR-200- ...
摘要:在体外产生的类似胚泡的结构非常重要,因为它们概括了早期胚胎发生的特定特征或过程,因此与使用天然胚胎相比,避免了道德问题,并提高了可伸缩性和可及性。在这里,我们结合了细胞重编程和机械刺激,以创建与天然胚胎表型相似的3D球形骨料。具体而言,皮肤成纤维细胞被重编程,利用miR-200家族特性在体细胞中诱导高可塑性状态。随后,使用临时诱导方案将miR- 200个编程的细胞驱动朝向滋养外胚层(TR)谱系驱动,或者封装在聚二氟乙烯微生物反应器中,以维持和促进多能性,以促进多脂蛋白,从而产生内部细胞质量(ICM)样球体。然后将所获得的Tr样细胞和ICM样球体共培养在同一微晶状体中,然后转移到微孔中,以鼓励囊性形成。值得注意的是,上述方案应用于从年轻和老年供体获得的成纤维细胞上,其结果突出了miR-200'的能力成功地重编程了具有可比性类囊体率的年轻和老年细胞,无论供体的细胞年龄如何。总的来说,此处描述的方法代表了一种新的策略,用于创建人工类囊体,用于在辅助繁殖技术领域中用于研究植入后和早期植入后机制。
企业相关产业废弃物收集运输案件1起
2024年3月27日 — 1 范围 本规范规定了日本航空自卫队滨松空军基地的业务相关工业废弃物的收集和运输。 2 参考文献 2.1 总则 本规范引用了下列文献:
利用位点特异性共价 Cas12a-crRNA 结合物提高基于 CRISPR-Cas12a 的基因组编辑效率
凌欣宇, 1 , 5 常丽英, 1 , 5 陈鹤琪, 1 高晓琴, 1 尹建航, 2 , 3 左毅, 1 黄玉佳, 1 张波, 4 胡佳芝, 2 , 3 和刘涛 1 , 6 , * 1 北京大学药学院天然药物及仿生药物国家重点实验室, 北京市海淀区学院路 38 号, 100191, 中国 2 北京大学生命科学学院细胞增殖分化教育部重点实验室, 基因组编辑研究中心, 北京 100871, 中国 3 北京大学北大-清华生命科学联合中心, 北京 100871, 中国 4 中国医学科学院北京协和医学院北京协和医院医学研究中心, 北京 100730, 中国 5 上述作者贡献相同 6 主要联系人*通讯地址:taoliupku@pku.edu.cn https://doi.org/10.1016/j.molcel.2021.09.021
角蛋白 1 靶向肽-阿霉素结合物在三阴性乳腺癌小鼠模型中的评估
摘要:化疗是三阴性乳腺癌 (TNBC) 的主要治疗方法,TNBC 是一种恶性程度高、预后较差的乳腺癌亚型。虽然化疗药物效果显著,但这些药物缺乏特异性,对癌症和非恶性细胞和组织同样具有毒性。针对 TNBC 的靶向疗法可能会带来更安全、更有效的药物。我们之前设计了一种乳腺癌细胞靶向肽 18-4,它特异性地结合乳腺癌细胞上的细胞表面受体角蛋白 1 (K1)。含有酸敏感腙连接子的肽 18-4 和阿霉素 (Dox) 的缀合物对 TNBC 细胞表现出特定的毒性。在这里,我们报告了在 TNBC 细胞衍生的异种移植小鼠模型中对 K1 靶向肽-Dox 缀合物 (PDC) 的体内评估。与接受 Dox 或生理盐水治疗的小鼠相比,接受该结合物治疗的小鼠的抗肿瘤功效显著提高,脱靶毒性降低。经过六周的治疗后,在第 35 天,与接受 Dox (2.5 mg/kg) 治疗的小鼠相比,接受 PDC (2.5 mg Dox 当量/kg) 治疗的小鼠的肿瘤体积显著缩小 (1.5 倍)。与接受 Dox 治疗的小鼠相比,接受该结合物治疗的小鼠的肿瘤中 Dox 水平显著升高 (1.4 倍),而其他器官中 Dox 水平降低 (1.3-2.2 倍)。15 分钟时采集的血液显示,注射 PDC 的小鼠体内的药物 (PDC 和 Dox) 浓度是注射 Dox 的小鼠体内的药物 (Dox) 浓度的 3.6 倍。研究表明,K1 靶向 PDC 是一种很有前途的治疗 TNBC 的新方法,具有良好的安全性,并且值得进一步研究 K1 靶向结合物作为 TNBC 治疗方法。
新的转铁蛋白受体靶向肽 - 多氧素结合物:合成和体外抗肿瘤活性
摘要:对肿瘤细胞的选择性不佳是抗肿瘤药物阿霉素(DOX)临床应用中的主要缺点。肽 - 药物结合物(PDC)通过用肽配体修饰抗肿瘤药物构建的肽配体对肿瘤细胞中某些过表达的受体具有很高的亲和力,从而越来越多地评估其肿瘤选择性药物递送的可能性。然而,由天然L-配置氨基酸组成的肽配体具有易于酶促降解和生物稳定性不足的缺陷。在这项研究中,设计和合成了两个新的PDC(L T7-SS-DOX和D T7- SS-DOX),通过结合转铁蛋白受体(TFR)肽配体L T7(HAIYPRH)及其retro-Inverso Inverso Analog DT7(Hrpyiah),并通过Dox a Diss a Diss nongulfide ncterulfide nicker inclulffide ncterne合成。与游离DOX相比,两个结合物对TFR过表达的肿瘤细胞表现出靶向的抗增生作用,对TFR低表达的正常细胞的毒性很少。此外,与L T7-SS-Dox相比,D T7-SS-dox结合物具有更高的血清稳定性,更持续减少的药物释放特性和更强的体外抗脂肪性活性。总而言之,抗肿瘤药物与D T7肽配体的偶联可以用作进一步发展稳定和有效的PDC的有前途的策略,并有可能促进TFR靶向的药物递送。
实验动物(小鼠)的基因组编辑
1) Jinek, M., Chylinski, K., Fonfara, I., Hauer, M., Doudna, JA 和 Charpentier, E. (2012): 适应性细菌免疫中的可编程双 RNA 引导 DNA 内切酶。Science, 337, 816- 821。2) Kim, S., Kim, D., Cho, SW, Kim, J. 和 Kim, JS (2014): 通过递送纯化的 Cas9 核糖核蛋白在人类细胞中进行高效 RNA 引导基因组编辑。 Genome Res.,24,1012 — 1019。3) Quadros, RM、Miura, H.、Harms, DW、Akatsuka, H.、Sato, T.、Aida, T.、Redder, R.、Richardson, GP、Inagaki, Y.、Sakai, D.、Buckley, SM、Seshacharyulu, P.、Batra, SK、Behlke, MA、Zeiner, SA、Jacobi, AM、lzu, Y.、Thoreson, WB、Urness, LD、Mansour, SL、Ohtsuka, M. 和 Gurumurthy, CB (2017):Easi-CRISPR:一种使用长 ssDNA 供体和 CRISPR 核糖核蛋白一步生成携带条件和插入等位基因的小鼠的稳健方法。 Genome Biol., 18, 1 — 15。4) Chen, S.、Lee, B.、Lee, AYF、Modzelewski, AJ 和 He, L. (2016): 高效小鼠基因组编辑
基于1,3,5-三嗪类的基于石墨烯和烷基化剂的新型非共价结合物
增加特异性的方法的方法之一和细胞抑制药物的生物相容性是与氧化石墨烯的结合物的创造。石墨烯及其氧化形式 - 氧化石墨烯(GO) - 由于其反应性和发育的表面,可以进行共价和非共价功能化,因此已成为纳米医学领域的新材料,这允许提供药物的固定化。本文致力于一种基于GO的非共价偶联物的生物相容性的合成,鉴定和研究的新方法,以及基于1,3,5-三嗪的烷基化剂。偶联物是血液相容的(在1-200 mg∙l 1中,溶血程度不超过5%),在模型反应中表现出抗氧化活性,与DPPH,降解量降低1.7倍,在GO-1 75 mg 1的最大浓度下降低了1.7倍,并具有1.7倍的浓度,并依赖于75 mg l 1 l 1)。并且还对细胞系A549,PANC-1和HELA表现出细胞毒性。最大细胞毒性显示在HeLa细胞系中(IC 50 = 2.5 L m)。2023由Elsevier B.V.
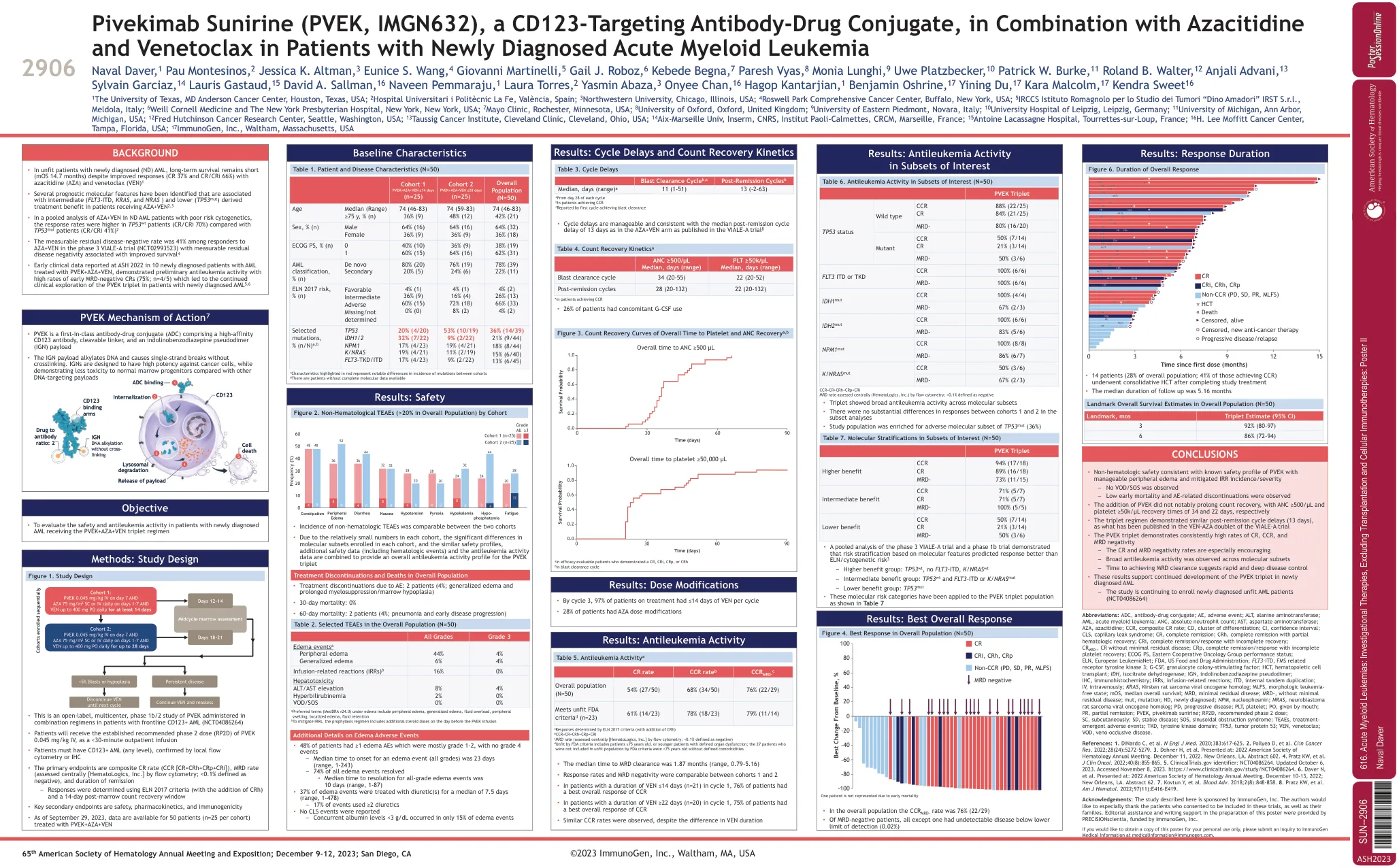
pivekimab sunirine(PVEK,IMGN632),一种CD123靶向抗体 - 药物结合物,与新近D
1美国德克萨斯州休斯敦的德克萨斯大学安德森癌症中心; 2医院Universitari iPolitècnicLaFe,西班牙瓦恩西亚; 3西北大学,美国伊利诺伊州芝加哥; 4罗斯威尔公园综合癌症中心,美国纽约,美国; 5 Irccs iStituto romagnolo per lo Studio dei tumori“ Dino Amadori” Irst S.R.L.,意大利梅尔多拉; 6 Weill Cornell Medicine和美国纽约的纽约长老会医院; 7美国明尼苏达州罗切斯特的梅奥诊所; 8英国牛津大学牛津大学; 9东皮埃蒙特大学,意大利诺瓦拉; 10莱比锡大学医院,德国莱比锡;密歇根大学11号,美国密歇根州安阿伯; 12号弗雷德·哈钦森癌症研究中心,美国华盛顿州西雅图; 13美国俄亥俄州克利夫兰克利夫兰诊所Taussig癌症研究所; 14 AIX-MARSELILL UNIV,INSERM,CNRS,PAOLI-CALMETTES,CRCM,MARSEILLE,法国; 15法国Tourrettes-Sur-Loup的Antoine Lacassagne医院; 16 H. Lee Moffitt癌症中心,美国佛罗里达州坦帕; 17美国马萨诸塞州沃尔瑟姆Immunogen,Inc。