XiaoMi-AI文件搜索系统
World File Search SystemBSC MBCHB FRCP PHD
Palmer教授于2011年被任命为利物浦大学医学肿瘤学的西北癌症研究主席。他的研究兴趣与肝胆(HPB)癌症有关(肝脏,胰腺和胆道)。Palmer教授是利物浦实验癌症医学中心(ECMC)的主任,这是克拉特布里奇癌症中心,利物浦临床试验中心和利物浦大学之间的合作。在2023年,帕尔默教授被任命为与NHS England的第一次获得正确(GIRFT)计划的临床负责人,并审查了胰腺癌患者的服务。
糖尿病治疗2型基于Inkretin激素
抽象糖尿病是一个全球健康问题,由于肥胖患者增加,由于各种并发症而引起的各种并发症,较高的死亡率和2型糖尿病是死亡的主要原因。进行抗糖尿病药物的发展是为了找到不仅降低血糖水平而且有望具有更多作用的新药物,例如能够恢复胰腺β分泌的功能并恢复受干扰的胰岛素受体敏感性。撰写本文献综述旨在讨论激素inkretin在体内的作用,胃抑制肽(GIP)和胰高血糖素样肽-1(GLP-1)在刺激胰岛素分泌中以及这些激素的其他作用/效果,这些激素具有物理上有利可图的和与糖尿病的治疗相吻合生命β细胞,也是其在抑制食欲中的作用。基于在诊所中使用的激素inkretin的一些抗糖尿病药物,包括胰高血糖素,如肽-1受体激动剂(GLP-1 RA)药物,类似于激素Inkretin Endogen Melitus 2型,二吡基肽酶-4抑制剂(DPP4抑制剂),胰高血糖素像肽-1激动剂受体(GLP-1 RA),Inkretin激素
肾脏移植受者中的胰高血糖素样肽-1受体激动剂 - 回顾性单中心研究
objetives:移植后糖尿病的发生率和移植受体中升高的心血管风险升高。胰高血糖素样肽激动剂有可能减轻免疫抑制药物的作用,以解决高血糖和体重增加。这使他们呼吁在该人群中使用,鉴于他们的简历和重新保护的益处。尽管如此,就其在糖尿病肾移植受者(KTR)中的疗效(KTR)方面没有足够的实质证据。方法:这项回顾性研究的目的是评估KTR中胰高血糖素样肽激动剂的有效性和安全性。主要重点是评估它们对各种参数的影响,例如血红蛋白A 1C水平,体重指数(BMI),脂质面板,血红蛋白水平,肾移植物功能(估计的肾小球滤过率[EGFR])和尿蛋白与尿蛋白至关重要的比率。结果:在18个月的中位观察期间,这项研究包括64名肾脏移植患者。基线时EGFR中位数为61.9 mL/min/1.73 m 2,在整个随访过程中保持稳定。中位HBA 1C从7.5降低至7%(95%CI; P <0.002)。还观察到了BMI和脂质面板的显着改善。我们没有观察到中位肌酐和尿蛋白的重大变化:肌酐比率水平。没有副作用证明该药物的中断是合理的。结论:这项研究表明,在KTR中,使用胰高血糖素样肽激动剂是可行且耐受性的,没有观察到显着的副作用。需要进行随后的研究来探索胰高血糖素类肽激动剂是否可以有效地改善这些患者的同种异体移植存活率。
gut-microbiota in-endocrine-health-and ...
内分泌健康受到肠道菌群的严重影响,包括多种机制,包括调节激素的产生,与代谢途径的相互作用以及能量稳态的维持。短链脂肪酸(SCFA),例如乙酸,丙酸酯和丁酸酯,是肠道纤维发酵过程中肠道细菌产生的关键代谢产物。这些SCFA充当信号分子,影响肠道上皮的激素分泌,包括胰高血糖素样肽-1和肽YY。GLP-1增强胰岛素分泌并抑制胰高血糖素的释放,导致葡萄糖稳态,而PYY调节食欲和能量摄入。
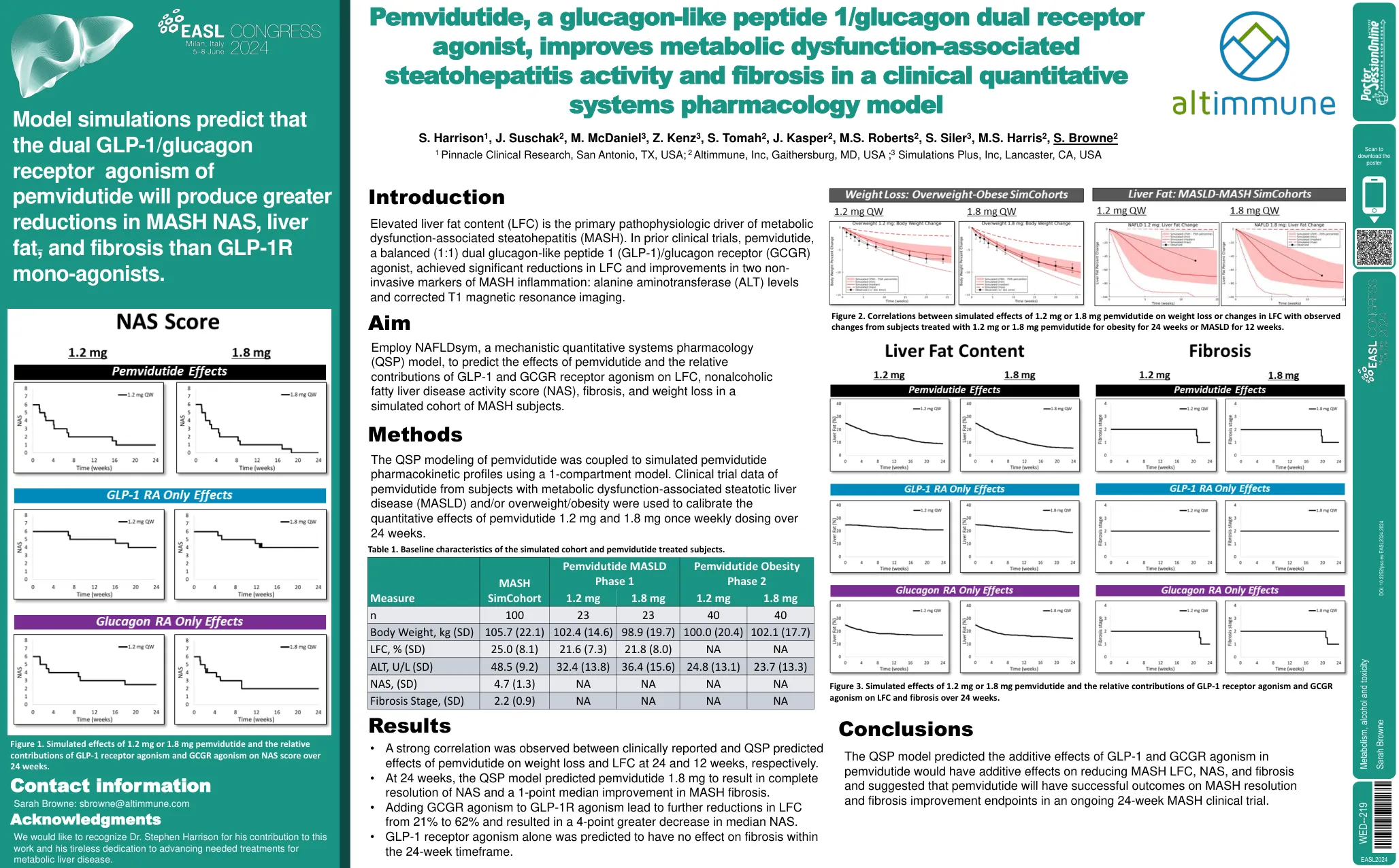
模型模拟预测,Pemvidutide的双重GLP-1/胰高血糖素受体激动剂将在Mash Nas,肝脂肪和FI
•分别在临床报道和QSP预测Pemvidutide对体重减轻和LFC时24和12周之间的影响之间观察到了很强的相关性。•在24周时,QSP模型预测Pemvidutide 1.8 mg可完全分辨NAS和MASH纤维化的1分中位数改善。•将GCGR激动剂添加到GLP-1R激动剂中,导致LFC从21%降低到62%,并导致中位NAS降低4点。•仅在24周时间内,仅凭GLP-1受体激动剂对纤维化没有影响。
致电授予申请-Hepatobiliary Cancers(...
肝胆癌的治疗进展正在为患者带来巨大变化。具有免疫疗法作为治疗方案的骨干的效用,与此类药物的组合疗法已成为中心阶段,为进一步的进步开辟了大门,以优化患者的疗效,安全性和易用性。1这导致了大量试验,评估了双特异性分子在肝脏空间中的作用。1鉴于双特异性代理商的独特MOA和新颖性,在治疗肝脏癌的多学科团队成员中,需要教育。2现在开始教育将减少学习曲线,并为患者的快速采用这些分子铺平道路。提案可能会讨论包括:我们正在寻求提出的提案,以解决有助于解释肝小癌中双特异性分子的基本原理的主题。更具体地说,建议可以详细概述双特异性分子的MOA,从而清楚地解释了它们与当前方案,它们是什么以及没有什么不同。为什么双特异性分子可以有效地治疗肝癌癌。概述了正在探索双特异性分子以治疗肝胆癌的双特异性分子,以及迄今为止可能存在的双特异性分子数据,包括安全性和功效。医学教育活动可清楚地概述这些分子并建立基准理解水平,目前必须从中扩展其他计划。参考需要双特异性分子是肝胆汁空间的新手,因此,我们预计在了解这些分子的独特作用机理以及在患者中使用这种治疗方式时,我们预计会有很大的学习曲线。
自身免疫性维生素B12中心缺乏症中的经黄素蛋白受体抗体
急性糖尿病并发症,包括糖尿病性酮症酸中毒(DKA)和严重的低血糖(2)。这些持续存在的Challenges强调了对胰岛素以外的其他治疗策略的紧迫需求。钠 - 葡萄糖共转移蛋白2(SGLT2)抑制剂药物已革新治疗2型糖尿病,心力衰竭和慢性肾脏疾病。但是,由于DKA风险增加,它们在1型糖尿病中的使用受到限制。在大型3阶段研究中,DKA风险增加了3-4倍(3,4),这一风险仍然是美国食品和药物管理局批准该组SGLT2抑制剂的主要范围(5-7)。鉴于患有1型糖尿病的个体患者的心脏失败和慢性肾脏疾病的明显风险,并且在达到血糖目标方面的普遍困难,因此SGLT2抑制剂的潜在受益很明显。因此,解决DKA风险对于将这些好处扩展到1型糖尿病患者至关重要。问题的根源是胰高血糖素。我们的研究表明,对1型腹泻患者的SGLT2抑制疗法导致空腹胰高血糖素水平增加37%(8)。这种增加的葡萄糖提出了一个双重问题:它不仅增加了内源性葡萄糖的产生(9),从而减少了SGLT2抑制剂的葡萄糖下降作用(10,11),而且还可以增强基因酮产生,尤其是在胰岛素型条件下(12,13)。胰高血糖素受体拮抗剂(GRA)的发展提供了检验我们假设的机会。因此,我们假设将SGLT2抑制与gluc糖抑制作用结合起来可以通过减少内源性葡萄糖产生并通过抑制生酮发生来改善血糖控制。GRA Volagide-mAb是一种完全人类的单克隆抗体,可抑制胰高血糖素受体(GCGR)与胰高血糖素的相互作用,已经显示出令人鼓舞的结果。我们先前证明,Volagidemab作为1型腹膜胰岛素治疗的辅助,可改善血糖控制(HBA 1C,0.5%),并将胰岛素使用降低12%(14)。然而,GRA疗法对酮症发生的影响,尤其是在与SGLT2抑制剂的组合中,仍未得到探索。因此,结合使用辅助性SGLT2抑制剂和GRA治疗的比例很强,目的是最大化葡萄糖
非小细胞肺癌的疫苗治疗
1 玛格丽特公主癌症中心,多伦多,ON M5G 2C1,加拿大;miguel.garcia@uhn.ca 2 巴塞罗那医院肿瘤内科,08036 巴塞罗那,西班牙;tgorria@clinic.cat 3 肝胆免疫病理学实验室,IRCCS 人道主义研究医院,Via Manzoni 56,20089 米兰,意大利;ines.malenica@humanitasresearch.it 4 INSERM UMR 1186,综合肿瘤免疫学和免疫疗法,Gustave Roussy,巴黎萨克雷大学医学院,94805 维尔瑞夫,法国; stephanie.corgnac@gustaveroussy.fr 5 巴塞罗那大学医院病理学系,Villarroel 170,08036 巴塞罗那,西班牙;teixido@clinic.cat 6 转化基因组学和实体肿瘤靶向治疗实验室,IDIBAPS,08036 巴塞罗那,西班牙 7 巴塞罗那大学医学系,08036 巴塞罗那,西班牙 * 通讯地址:lmezquita@clinic.cat
基于单剂量GLP-1的胰腺基因疗法在戒断半氟肽后保持体重减轻,并在肥胖症的鼠模型中降低肝甘油三酸酯
的图从Polonsky等人改编。糖尿病。2022 13:175–1871。1。Nauck等。 mol代谢。 2021 46:101102。 2。 坎贝尔和德鲁克。 细胞代谢。 2013 17:819-837。 3。 Polonsky等。 糖尿病。 2022 13:175–1871。 4。 Weiss等。 患者更喜欢依从性。 2020 14:2337-2345。 5。 Polonsky等。 糖尿病谱。 2021 34:175-183。 6。 Terhune。 路透社。 2023 7月11日。 GLP-1RA =胰高血糖素样肽1受体激动剂Nauck等。mol代谢。2021 46:101102。2。坎贝尔和德鲁克。细胞代谢。2013 17:819-837。 3。 Polonsky等。 糖尿病。 2022 13:175–1871。 4。 Weiss等。 患者更喜欢依从性。 2020 14:2337-2345。 5。 Polonsky等。 糖尿病谱。 2021 34:175-183。 6。 Terhune。 路透社。 2023 7月11日。 GLP-1RA =胰高血糖素样肽1受体激动剂2013 17:819-837。3。Polonsky等。糖尿病。2022 13:175–1871。4。Weiss等。患者更喜欢依从性。2020 14:2337-2345。5。Polonsky等。糖尿病谱。2021 34:175-183。6。Terhune。路透社。2023 7月11日。GLP-1RA =胰高血糖素样肽1受体激动剂