XiaoMi-AI文件搜索系统
World File Search SystemRET 抑制可克服 ER+ 乳腺癌对 CDK4/6 抑制剂和内分泌疗法的耐药性
方法:为了确定与联合内分泌治疗和 CDK4/6i 耐药相关的基因表达改变,我们对两种对该联合治疗有耐药性的 ER+ 乳腺癌细胞模型进行了 RNA 测序。通过 siRNA 介导的 RET 沉默和 FDA/EMA 批准的 RET 选择性抑制剂 selpercatinib 在耐药乳腺癌细胞和患者来源的类器官 (PDO) 中的靶向抑制来评估 RET 的功能作用。使用全局基因表达和通路分析从机制上评估 RET 沉默。通过对接受内分泌治疗的原发性肿瘤进行基因阵列分析,以及对接受联合 CDK4/6i 和内分泌治疗的患者的转移性病变进行免疫组织化学评分,研究了 ER+ 乳腺癌中 RET 表达的临床相关性。
ESR1突变驱动对ER+乳腺癌中CDK4/6抑制剂的抗性
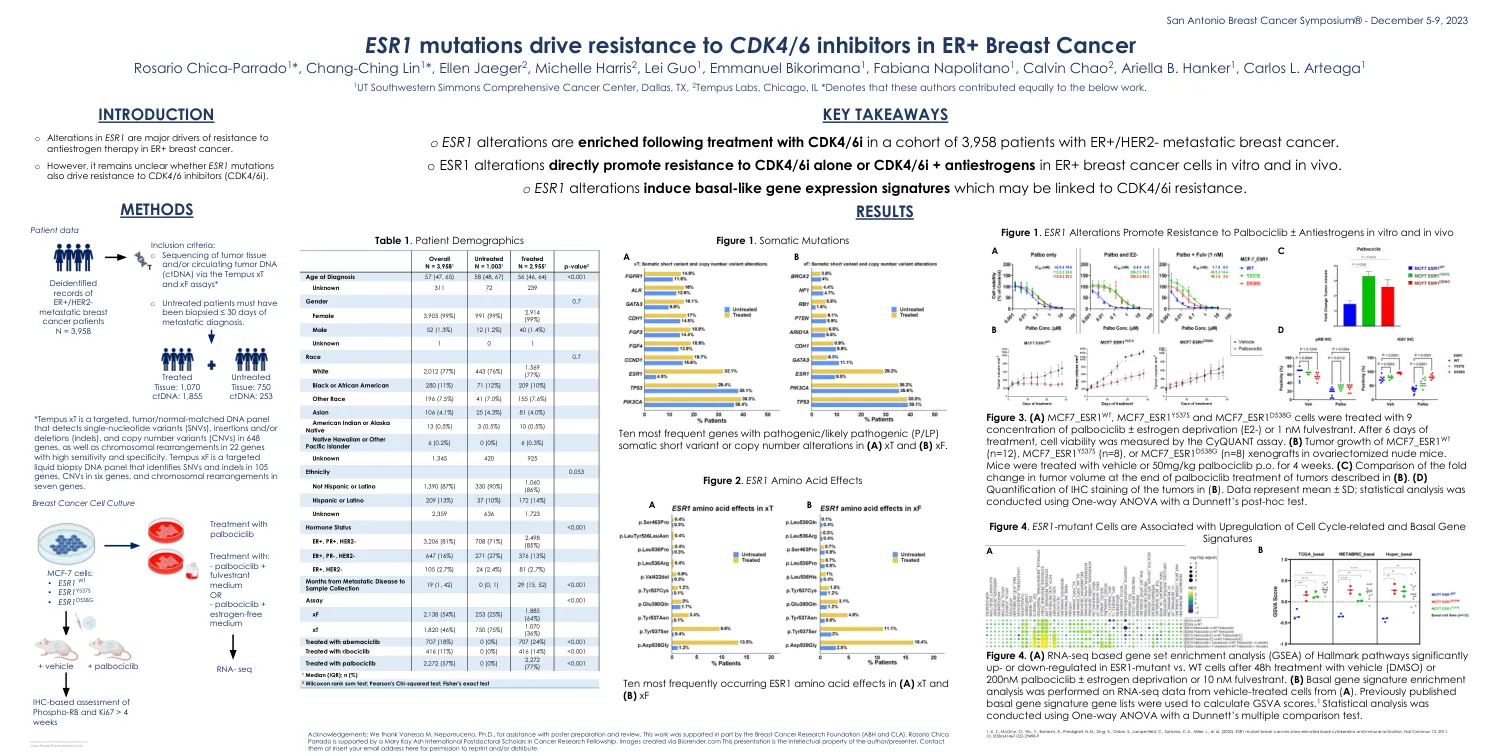
图3。(a)MCF7_ESR1 WT,MCF7_ESR1 Y537S和MCF7_ESR1 D538G细胞用9浓度的palbociclib±雌激素剥夺(E2-)或1 nm fulvesterant处理。治疗6天后,通过曲面测定法测量细胞活力。(b)MCF7_ESR1 WT的肿瘤生长(n = 12),MCF7_ESR1 Y537S(n = 8)或MCF7_ESR1 D538G(N = 8)异种移植物在卵巢肌切除术中。小鼠用车辆或50mg/kg Palbociclib P.O.持续4周。(c)在(b)中描述的肿瘤处理结束时肿瘤体积的折叠变化的比较。(d)(b)中肿瘤的IHC染色定量。数据代表平均值±SD;使用Dunnett的事后测试使用单向方差分析进行统计分析。
caspase-4二聚体和D289自动加工引起白介素-1β-转化酶更新乳腺癌中电流和新的潜在免疫疗法,从长凳到床边
在癌症免疫疗法中已经看到了令人印象深刻的进步。尽管乳腺癌(BC)长期以来一直被认为是非免疫原性的,但治疗BC治疗的免疫疗法现在已成为一种新的有希望的治疗方法,具有巨大的潜力。这得到了各种免疫疗法的大量完整和正在进行的临床前和临床研究的支持。然而,临床肿瘤学和基本癌症研究之间的显着差异会损害对癌症免疫学和免疫疗法的理解,从而阻碍了癌症治疗研究和发育。要以最佳的方式利用累积的可用数据,必须整合在卑诗省免疫疗法及其临床陷阱中发挥作用的两种基本机制。然后,临床试验必须经过精心设计,以适当的常规和免疫治疗策略组合。尽管有重大改进的空间,但此更新的评论详细介绍了迄今为止从长凳到床边可用的免疫治疗工具,希望这将导致重新思考和优化卑诗省患者的护理标准。
乳腺癌 - 个性化的,分子的突破...
• low sensitivity of mammography (up to 93% in fatty breast to 30 % in extremely dense breasts ( D category) • Number of false positive results in fatty breast 11/1000 mammo increases to 24/1000 in dense breast • Screening reduces relative risk of death from BC in fatty breast to 43 % compared to 13 % • Density is independent risk factor for developing breast cancer aside age and genetics ( 4-6 fold in D breasts)
II-III期非小细胞肺癌的围手术期免疫疗法:随机对照试验的荟萃分析基础 L-DOS47升高胰腺癌肿瘤pH并增强对免疫疗法的反应 蒙特卡洛法的进步用于模拟具有碳基填充物的导电聚合物复合材料的电渗透行为 科学期刊 科学期刊 可持续性
结果:最终分析中包括三个RCT(Keynote-671,Nadim II和Aeegean)。PIO group (neoadjuvant platinum-based chemotherapy plus perioperative immunotherapy) exhibited superior ef fi cacy in OS (hazard ratio [HR]: 0.63 [0.49-0.81]), EFS (HR: 0.61 [0.52, 0.72]), objective response rate (risk ratio [RR]: 2.21 [1.91, 2.54]), pathological complete response (RR:4.36 [3.04,6.25]),主要病理反应(RR:2.79 [2.25,3.46]),R0切除率(RR:1.13 [1.00,1.26])和辅助治疗速率(RR:1.08 [1.08 [1.01,1.15])与PP组(NeoAdjuvivant Plasity Plaser Plaser Plaser Planeboers plyoper plyoper plyoper plyoper)相比。在亚组分析中,EFS几乎在所有亚组中都倾向于PIO组。BMI(> 25),T阶段(IV),N阶段(N1-N2)和病理反应(具有病理完全反应)是PIO组的有利因素。在安全评估中,PIO组表现出更高的严重AE(28.96%比23.51%)和AES导致治疗中断(12.84%比5.81%)。同时,尽管总的不良事件,3-5级不良事件和致命的不良事件倾向于有利于PP组,但差异在统计学上并不显着。
Abemaciclib 联合内分泌治疗用于激素受体阳性、HER2 阴性、淋巴结阳性且复发风险较高的早期乳腺癌的辅助治疗
3.1 乳腺癌是英国最常见的癌症。激素受体阳性、HER2 阴性乳腺癌是最常见的亚型,约占所有乳腺癌的 70%。患者专家解释说,激素受体阳性、HER2 阴性、淋巴结阳性的早期乳腺癌复发风险高,对生活质量有相当大的影响。初次诊断令人痛苦,对癌症复发的恐惧是患者及其家人压力和焦虑的常见原因。这是因为需要进一步治疗或可能进展为无法治愈的转移性疾病。对于患有 HER2 阴性疾病的人来说,治疗选择有限,并且伴有不良副作用,使得完成推荐的疗程变得困难。临床专家指出,30% 的早期乳腺癌患者在初次治疗后会复发。他们指出,某些临床和病理风险因素(如阳性淋巴结数量多、肿瘤大或肿瘤等级或生物标志物测量的高细胞增殖)会导致复发风险更高。手术后复发风险高的患者存在大量未满足的需求。患者和临床医生将非常重视靶向治疗以降低复发风险。委员会得出结论,激素受体阳性、HER2 阴性、淋巴结阳性的早期乳腺癌患者及其家属将欢迎一种降低复发风险的新型有效治疗方案。
Sotorasib 在患有 KRAS G12C 突变的肺腺癌和未经治疗的活动性脑转移的患者中表现出颅内活性
一名 61 岁女性患者,因持续疲劳被诊断为右上肺叶转移性腺癌,伴有局部淋巴结转移、多发性肺转移和右额叶脑转移(根据 PET-CT 发现的临床分期:cT3 cN2 cM1c)。肿瘤 DNA 的下一代测序(Ion AmliSeq Colon and Lung Research Panel v2、Ion Torrent 平台、热点区域分析)显示 KRAS p.G12C (c.34G>T) 突变,但没有其他靶向改变。PD-L1 的免疫组织化学染色在肿瘤细胞中不到 1%。一线全身治疗采用顺铂、培美曲塞和帕博利珠单抗,总体获得部分缓解,包括脑转移完全缓解,2018 年 9 月开始使用培美曲塞和帕博利珠单抗维持治疗。2019 年 3 月,由于进行性多发性神经病变,停用培美曲塞。2019 年 6 月,患者肺部出现进展,因咯血而需要止血放射治疗,帕博利珠单抗也停用。单独的脑转移继续缓解。2019 年 11 月,患者肺部再次出现进展,并出现有症状的脑部进展,小脑蚓部出现新的病变,导致导水管受压和连续性脑积水。植入脑室腹腔分流术,小脑蚓部病变用立体定向放射治疗;进行性肺部病变用放射治疗;此外,由于病情稳定,且持续控制疾病超过一年,因此恢复使用派姆单抗治疗。然而,2021 年 2 月,患者小脑已知病变进展(临床意义不大),左脑室周围白质出现新转移,肺部进一步进展。2021 年 3 月开始使用多西他赛,肺部和脑部病变进展,右额叶和颞叶出现新病变,这是四个周期后的最佳反应(见图 1 治疗时间顺序示意图)。2021 年 6 月,开始口服 960 毫克每日 sotorasib 治疗。经过 6 周的 sotorasib 治疗后,不仅肺部,而且未治疗的脑转移瘤都出现了令人印象深刻的治疗反应,这种反应持续了 5 个月(见图 2)。由于全身进展,停止使用 sotorasib 治疗,并于 2021 年 11 月底开始使用吉西他滨治疗。2021 年 12 月初,患者出现症状性脑部进展,行为改变和精神萎靡,并进行了神经外科干预,包括开颅术和肿瘤切除术。吉西他滨的全身治疗持续到 2022 年 2 月,并因疾病进展而停止。患者于 2022 年 3 月接受培美曲塞进一步全身治疗(再次治疗),随后于 2022 年 4 月接受卡铂和紫杉醇治疗。此外,患者于 2022 年 4 月进行了全脑放射治疗。随着病情进一步进展,患者自 2022 年 5 月起接受最佳支持治疗。
双酚A和DDT破坏乳腺中的脂肪细胞功能:对乳腺癌风险和进展的影响
随着乳腺癌发病率在全球范围内继续上升,迫切需要了解有助于其发展的环境因素。肥胖症,包括双酚A(BPA)和二氯二苯基三氯乙烷(DDT),在环境中非常普遍,并且与肥胖和代谢失调有关。BPA和DDT,已知会破坏乳腺上皮细胞中的激素信号传导,还促进脂肪组织中的脂肪生成,脂肪生成和脂肪因子分泌,直接导致肥胖症的发病机理。虽然富含脂肪的乳腺可能特别容易受到环境性肥胖症的影响,但研究研究了肥胖的脂肪细胞的变化,促进乳腺上皮细胞的致癌细胞的变化。在这里,我们回顾了将BPA和DDT与乳腺发育和乳腺癌风险降低的临床前和临床证据。我们讨论了肥胖驱动的机制如何有助于肥胖,包括脂肪生成,脂肪生成和脂肪因子分泌的变化,可以提供促进富含营养的富含营养的环境,从而促进乳房上皮细胞中致癌途径的激活。了解肥胖症在乳腺癌风险和进展中的作用对于旨在最大程度地减少肥胖原子的公共卫生指南,最终降低乳腺癌的发病率并改善女性的结果至关重要。
免疫疗法时代的卵泡衍生甲状腺癌的新兴治疗选择
尽管大多数卵泡衍生的甲状腺癌的分化良好,并且在手术和放射性碘治疗后,甲状腺癌的管理(包括碘难治性疾病)和不良分化/未分化的亚型在治疗后具有出色的预后,更具挑战性。在过去的十年中,对甲状腺癌晚期的遗传驱动因素和免疫环境的了解已导致这些患者的管理取得了重大进展。现在,美国食品药品监督管理局(FDA)批准了许多靶向激酶抑制剂,用于治疗晚期放射碘难治性分化甲状腺癌(DTC)以及甲状腺质癌(ATC)。免疫疗法也已进行了彻底的研究,并在选定病例中表现出了希望。在这篇综述中,我们总结了放射碘耐药DTC和ATC的遗传景观以及细胞和分子基础方面的进展,并讨论了当前的治疗方案以及未来的治疗途径。
大脑思维学院HelixScreen创造了乳腺癌护理的新时代什么是Bose-Einstein冷凝物?冷原子...
Bose-Einstein冷凝物的研究很重要,因为它具有原子理的潜力。可以提高精度的原子激光器和测量仪器。 例如,BEC可用于精确的重力波检测。 bec还具有减速光的能力,并且已经表明,光脉冲甚至可能被困在它们中。 这可能会导致在基于光的技术领域的充分应用,并影响量子计算的世界。 总的来说,在ISS的CAL中研究更长的BEC的能力肯定会带来令人兴奋的机会。可以提高精度的原子激光器和测量仪器。例如,BEC可用于精确的重力波检测。bec还具有减速光的能力,并且已经表明,光脉冲甚至可能被困在它们中。这可能会导致在基于光的技术领域的充分应用,并影响量子计算的世界。总的来说,在ISS的CAL中研究更长的BEC的能力肯定会带来令人兴奋的机会。