XiaoMi-AI文件搜索系统
World File Search SystemEA8143(Prosper RCC)临床试验结果摘要
EA8143/Prosper RCC试验是针对肾癌患者(也称为肾细胞癌[RCC]),其癌症的返回高风险(经常性),并且即将接受肾脏的全部或部分去除。该试验正在测试如果患者在手术前后与单独的手术相比,手术前后的免疫疗法药物nivolumab在手术前和手术后的添加。共有785名患者参加了EA8143/Prosper RCC。
在现实世界中应用声音试验结果
从Dana-Farber Brigham癌症中心手术数据库中确定的作者512名患者从2016年至2022年接受了HR+HER2-乳腺癌,他们符合合理的试验资格标准。SLNB在411(80.5%)中完成,并在98(19.2%)中省略了。一个过程失败。“事实证明,患者人口与合理的试验参与者非常相似,”金博士说。进行了乳房切除术的患者中有88%的SLNB阴性,而在SLNB上患有淋巴结疾病的患者中,有75%的患者只有一个阳性。小于1.0%的阳性淋巴结超过四个。癌症复发率非常低,也与声音试验参与者相似,尽管随访时间较短。
Kazia Therapeutics宣布了II/III期的临床试验结果Kazia Therapeutics宣布了II/III期的临床试验结果
Paxalisib in Glioblastoma GBM AGILE trial data shows clinically meaningful improvement in a prespecified secondary analysis for overall survival in paxalisib-treated, newly diagnosed unmethylated patients with glioblastoma Sydney, July 10, 2024 -- Kazia Therapeutics Limited (NASDAQ: KZIA), an oncology-focused drug development company, is pleased to announce results from GBM-Agile是一项II/III期研究,其中包括对胶质母细胞瘤患者(NCT03522298)的Paxalisib与护理标准(SOC)的评估,这是一种危及生命的脑癌,在这种情况下,紧迫的新疗法需求紧迫。GBM敏捷研究GBM Agile是一项自适应的全球试验,由全球自适应研究联盟(GCAR)(GCAR)赞助,该联盟由世界上一些最重要的临床,翻译和基础科学研究人员组成,该组织由纪念Sloorial Sloiorage Sloorial Kettering Cancer Cancer Centle Cancer and Dana-Farber cancer and Dana cancer Intercute等机构组成。该试验旨在有效筛选和表征胶质母细胞瘤(GBM)患者对新型研究剂的反应。利用复杂的创新设计,将贝叶斯原则应用于主要终点(总生存)(总生存)比较研究开始招募的护理标准(SOC)的患者(也称为累积对照人群)。一般而言,与研究剂(并发对照人群)同时招募的对照患者相比,基于既定的统计模型对二次分析和终点进行评估。累积控制组从2019年7月开始招募(GBM敏捷研究日期)至2022年5月。paxalisib是第三个在研究中完成评估的药物,并在新诊断的未甲基化MGMT启动子状态以及复发性疾病的患者中进行了评估。GBM敏捷Paxalisib结果Kazia首席执行官John Friend博士说:“我们很高兴在整体生存率上表现出3.8个月的改善,大约33%的改善,对于新诊断的未经甲基化的GBM患者,与同意的护理ARM相比,我们很高兴提高了33%的改善。在两项独立研究中具有可比的总生存数据是这种难以治疗胶质母细胞瘤人群的令人信服的结果。我们期待讨论与FDA加速批准途径的可能方法。”总共313名新诊断的未甲基化(NDU)患者和在美国顶级癌症医院接受治疗的经常性患者是在第1阶段与Paxalisib治疗组(60 mg/day)或2021年1月至2022年5月的SOC并发控制组的随机分配的。
利用药物生物活性预测临床试验结果 - ...
摘要 能够估计药物在临床试验中获得批准的概率为优化药物研究工作流程提供了天然优势。临床试验的成功率对成本、开发时间以及严格的监管审批流程的压力有着深远的影响。我们提出了一种机器学习方法,该方法可以使用生物活性、化合物的物理化学性质、靶标相关特征和基于 NLP 的化合物表示以可靠的准确度预测试验结果。生物活性从未被用作预测特征。我们从临床试验中提取了药物-疾病对,并使用多个数据源将靶标映射到该对。实证结果表明,集成学习优于独立训练的小数据 ML 模型。我们报告了从随机森林分类器得出的结果和推论,该分类器的平均准确率为 93%,并且“通过”类的 F1 得分为 0.96。“通过”是指所有临床试验的两个类别(通过/失败)之一,该模型在预测“通过”类别方面表现良好。特征分析表明,生物活性在预测临床试验结果方面发挥着重要作用。我们付出了巨大努力来制作数据集,这是首次将临床试验信息与蛋白质靶标整合在一起。本研究提供了映射这些实体的所有代码,所有数据均来自公开来源。虽然我们的模型在包含生物活性时识别出低位推论,但整合生物活性和靶标信息的代码使研究人员能够访问深度策划和专有的临床试验数据库,从而获得更深入的见解、更好的统计意义以及更好地预测试验失败的能力。
2023 年全年及第四季度临床试验结果附录.pdf
Wainua – ATTR-CM(CARDIO-TTRansform) baxdrostat – 不受控制的高血压(BaxHTN) 呼吸 – 轻度至中度哮喘(LITHOS) 呼吸 – 重度哮喘(KALOS) 呼吸 – 重度哮喘(LOGOS) 呼吸 – 中度哮喘(VATHOS) 呼吸 – COPD(ATHLOS) RESOLUTE) Saphnelo – 中度至重度 SLE(TULIP-SC) Saphnelo – 中度至重度 SLE(AZALEA-SLE) Airsupra – 轻度哮喘(BATURA) tozorakimab – 急性呼吸衰竭(TILIA) Ultomiris – HSCT-TMA(ALXN1210-TM-313) Ultomiris – 儿童。 HSCT-TMA(ALXN1210-TM-314)Ultomiris – CSA-AKI(ARTEMIS)安塞拉米单抗 – AL 淀粉样变性(May Stg. IIIa)(CAEL101-302)安塞拉米单抗 – AL 淀粉样变性(May Stg. IIIb)(CAEL101-301)。
基于精神性的高血压干预:对血压和内皮功能的影响 - feel试验结果
试验方法先前已发表(11),该试验已在Ensaiosclinicos注册。gov.br(RBR-7 M7CT53)。简要地说,感觉是一项开放的随机对照试验,评估了在I和II期高血压中基于灵性的干预措施的使用。该试验得到了联邦戈亚斯大学临床医院的机构审查委员会的批准(注册号:5.487.621),所有患者均提供了书面知情同意书。试验。该试验由HTN参考中心的巴西联邦大学高血压部门协调,并在巴西人心脏病学协会(DEMCA/SBC)的精神和心血管医学系科学支持下进行。
使用数字孪生患者队列和 GenerativeAI 对新药临床试验结果进行预测建模
BioAlg Corp. 摘要 存在临床试验失败的问题,因为每种新药的疗效都应该超过现有治疗方案的疗效,而这随着时间的推移变得越来越具有挑战性。另一个重要问题是治疗对当前疗法产生耐药性的患者。本质上,使用药物组合或标外用药(指征与诊断不符)类似于实验,因为没有足够的数据来确定使用哪种药物或组合。这项工作提出了一种利用基因表达和临床数据对患者进行计算机建模的方法。深度学习和生成对抗网络被用作建模工具。算法的训练数据来自公开可用的数据库,例如 TCGA 和 Drugbank。建模基于患者之间的相似性、药物之间的相似性以及个体器官和患者组织与细胞系之间的相似性的假设,相似性是通过数学计算的。结果,创建了一个患者模型,其中输入由药物及其组合组成,输出提供生存概率值。这些模型数据可以使用生成对抗网络 (GAN) 技术生成任意数量的所需数量,以创建观察组和对照组。因此,可以模拟临床试验、预测其结果,最重要的是,优化试验参数以最大程度地提高成功的可能性。简介许多研究都集中于确定患者是否会超过定义的 OS 或 PFI 的阈值,从而产生分类任务。研究人员试图分类患者对给定疗法的反应是积极还是消极 [1]。一些方法可以预测对特定治疗药物的反应,但仅限于少数化疗药物,通常少于 10 种。其他药物的模型尚未训练 [2]。现有的预测临床试验有效性或临床结果的方法基于不同的方法。然而,结合转录组分析数据的研究有限(1900 项中不到 45 项)。
Kura Oncology 和 Kyowa Kirin 宣布 Ziftomenib 单药治疗注册试验结果呈阳性,并且
– Kura 管理层将于今天美国东部时间下午 4:30 举办虚拟投资者活动 – 圣地亚哥和东京,2025 年 2 月 5 日和 6 日 – Kura Oncology, Inc. (Nasdaq: KURA,“Kura”) 和 Kyowa Kirin Co., Ltd. (TSE: 4151,“Kyowa Kirin”) 今天宣布了 KOMET-001 的积极顶线结果,这是 ziftomenib 的 2 期注册导向试验,ziftomenib 是一种高度选择性、每日一次的口服研究性脑膜炎抑制剂,用于治疗复发/难治性 (R/R) NPM1 突变型 (NPM1-m) 急性髓细胞白血病 (AML) 患者。 KOMET-001 的顶线数据已提交给即将于 2025 年第二季度举行的医学会议进行展示,Kura 有望在 2025 年第二季度向美国食品药品监督管理局 (FDA) 提交 ziftomenib 的新药申请 (NDA)。两家公司宣布将在 2024 年联合将 ziftomenib 商业化,同时还宣布他们计划启动一项单一方案,该方案包含两项独立驱动、随机、双盲、安慰剂对照、注册性 3 期试验,以评估 ziftomenib 联合强化和非强化联合方案对新诊断的 NPM1-m 和 KMT2A 重排 (KMT2A-r) 患者的效果
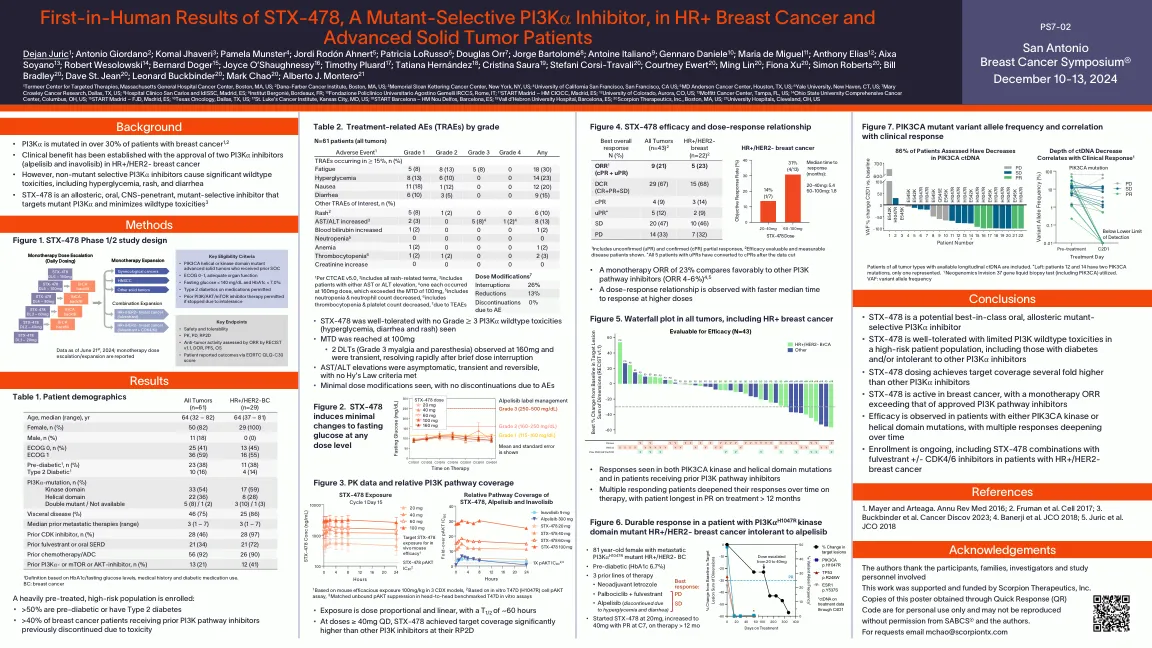
STX-478(一种突变选择性 PI3K α 抑制剂)在 HR+ 乳腺癌中的首次人体试验结果和
1 美国马萨诸塞州波士顿麻省总医院癌症中心 Termeer 靶向治疗中心;2 美国马萨诸塞州波士顿丹娜法伯癌症研究所;3 美国纽约州纽约斯隆凯特琳纪念癌症中心;4 美国加利福尼亚州旧金山加利福尼亚大学;5 美国德克萨斯州休斯顿 MD 安德森癌症中心;6 美国康涅狄格州纽黑文耶鲁大学;7 美国德克萨斯州达拉斯玛丽克劳利癌症研究中心;8 西班牙马德里圣卡洛斯医院和 IdISSC;9 法国波尔多贝尔格尼研究所;10 意大利罗马 Agostino Gemelli IRCCS 大学综合医院基金会;11 西班牙马德里 START – HM CIOCC;12 美国科罗拉多州奥罗拉科罗拉多大学;13 美国佛罗里达州坦帕莫菲特癌症中心; 14 俄亥俄州立大学综合癌症中心,美国俄亥俄州哥伦布市;15 START 马德里 – FJD,西班牙马德里市;16 德克萨斯肿瘤学中心,美国德克萨斯州达拉斯市;17 圣卢克癌症研究所,美国密苏里州堪萨斯城市;18 START 巴塞罗那 – HM Nou Delfos,西班牙巴塞罗那市;19 Vall d'Hebron 大学医院,西班牙巴塞罗那市;20 Scorpion Therapeutics, Inc.,美国马萨诸塞州波士顿市;21 大学医院,美国俄亥俄州克利夫兰市