XiaoMi-AI文件搜索系统
World File Search System肿瘤学 - IWILFIN事先授权政策
可以使用授权的供应商指南来支持医疗必要性和其他覆盖范围确定。c Indiation f ormulary c超大:o verview iwilfin,一种鸟氨酸脱羧酶抑制剂,被指示可降低成人和儿童在高危神经母细胞瘤中复发的风险至少对包括先前的多重,多态性抗性抗体的偏见,包括对先前的抗多态性抗体,这些抗体症是对抗多态性的抗毒剂,免疫疗法。1指南IWILFIN在国家综合癌症网络(NCCN)指南中进行了讨论。NCCN neuroblastoma guidelines (version 2.2024 – July 2, 2024) recommend Iwilfin as continuation therapy in patients with high-risk disease who have had at least a partial response to prior systemic agents and have completed post-consolidation immunotherapy with Unituxin ® (dinutuximab intravenous infusion) [category 2B].2 P Olicy S Tatement提前授权以进行iWilfin的处方福利覆盖范围。在下面指出的持续时间内提供了所有批准。
抗生素和非靶向代谢物残留检测是确保原料奶食品安全的综合方法
摘要:牛奶中的抗生素残留是乳制品加工过程中严重的健康和技术问题。本研究旨在验证治疗后未使用抗菌药物,同时考虑停药期,并评估在确认 HPLC-HRMS(高效液相色谱-高分辨率质谱)Orbitrap 分析后在现场条件下进行筛选测试的可靠性。此外,使用新的 Compound Discoverer 方法研究了预期或非目标代谢物的存在。尽管样本是在第七次挤奶时采集的,但 29% 的样本中仍显示存在抗菌药物,有时还显示其代谢物(恩诺沙星和林可霉素)。此外,在 9% 的样本中,由于存在母体药物和代谢物,因此发现了未申报的治疗。最后,提出了两种新的恩诺沙星代谢物 ENRO-N-甲基乙酰胺和 ENRO-鸟氨酸的推定鉴定。鉴于这一证据,必须牢记,一些具有药理活性的代谢物也可能对消费者和奶酪行业整个牛奶加工过程构成风险。
通过靶向下一代测序检测到的遗传改变及其在神经母细胞瘤中的临床意义
摘要。背景/目标:本研究研究了替莫唑胺(TMZ)和/或检查点激酶抑制剂AZD7762对人神经胶质瘤细胞的影响。材料和方法:胶质瘤细胞用TMZ和/或AZD7762处理24或48小时,然后研究了细胞存活,并研究了各种蛋白质的表达。结果:TMZ和AZD7762诱导的浓度和时间依赖性细胞毒性作用,以及TMZ和AZD7762(TMZ+AZD)的联合引起了胶质瘤细胞中的协同细胞毒性作用(P <0.05)。AZD7762抑制了O 6-甲基鸟氨酸-DNA-甲基转移酶(MGMT)的表达。tmz+AZD增加了磷酸p53(P-p53),p-p38有丝分裂原激活的蛋白激酶,磷酸酶和Tensin同源物的表达;并降低了胶质瘤细胞中p-细胞信号调节激酶1/2的表达和p-信号传感器和转录3的激活剂。结论:TMZ和AZD7762对人神经胶质瘤细胞的合并诱导的协同细胞毒性作用,并且这种作用可能与AZD7762诱导的MGMT表达抑制和多个信号通路的调节有关。
癌症基因和细胞治疗的新时代
用基因治疗治疗人类遗传病的理念早在50多年前就被提出(13)。尽管从理论到临床应用的道路漫长而充满挑战,但基因治疗为多种疾病的治疗提供了新的选择。成功的基因治疗已从直接体内注射病毒载体发展到过继转移基因工程细胞和基因组编辑(14)。1970年,斯坦菲尔德·罗杰斯(Stanfield Rogers)进行了首次人类基因治疗实验,他试图通过注射含有精氨酸酶的乳头瘤病毒来治疗2名高精氨酸血症儿童,但未能取得成功(15)。1999年,杰西·格尔辛格(Jesse Gelsinger)自愿参加费城宾夕法尼亚大学针对罕见遗传病鸟氨酸转氨甲酰酶缺乏症进行的基因治疗试验,但他在试验后不久就去世了(16)。2000年,首次成功的基因治疗试验临床结果发表,涉及严重联合免疫缺陷(SCID)-X1,为基因治疗铺平了道路。
活动位点胰蛋白酶的质谱分析...
摘要:人类接触DNA烷基化剂的特征很差,部分原因是仅量化了有限的特定烷基DNA加合物范围。人类DNA修复蛋白,O 6-甲基鸟氨酸O 6-甲基转移酶(MGMT),不可逆地将烷基从DNA O 6-烷基鸟氨酸(O 6-烷基)转移到受体半胱氨酸上,从(ASP)。重组MGMT与含有不同O 6-烷基,替莫唑胺 - 甲基化小牛胸腺DNA(ME -CT -DNA)或已知O 6-甲基G(O 6- meg)水平的人类结肠直肠DNA或人结直肠DNA的寡脱氧核苷酸(ODN)孵育。用胰蛋白酶消化,并通过基质辅助激光解吸/飞行飞行时间质谱检测和定量ASP。ASP含有S-甲基,S-乙基,S-丙基,S-羟基乙基,S-羧甲基,S-苯甲酰苯基和S-吡啶糖丁基半胱氨酸基团,通过将MGMT与含有相应的O 6-烷基的OD孵育来检测到MGMT。在MGMT与ME-CT-DNA孵育后检测到的含有S-甲基半胱氨酸的ASP的LOQ <0.05 pmol O 6 -meg每mg CT-DNA。将MGMT与人类结直肠DNA孵育,该ASP产生的ASP含有S-甲基半胱氨酸的水平,与先前由HPLC -RadioMumunoAseay确定的O 6 -MEG相关的水平(r 2 = 0.74; P = 0.014)。o 6 -CMG,一种推定的O 6-羟基乙基加合物和其他潜在的未鉴定MGMT底物。4最近在结直肠癌中描述了类似的突变签名,这意味着AA暴露为这种新颖的方法是对人DNA中O 6 -ALKG的鉴定和定量的方法,揭示了人类DNA烷基加合物的存在,尚待充分表征。该方法建立了一个表征人DNA O 6 -Alkg加合体的平台,并且鉴于O 6 -Alkgs的诱变潜力可以提供有关癌症发病机理的机械信息。■简介烷基化剂(AAS)是已知的人类诱变剂和致癌物,其作用在很大程度上是由DNA中烷基加合物形成的介导的。1 - 3在用化学治疗甲基化剂Temozolomide治疗后,在恶性黑色素瘤和胶质母细胞瘤多种形式的患者中观察到的突变景观,替莫唑胺,主要由DNA中O 6-甲基鸟嘌呤(O 6-meg)产生的G -A转变。
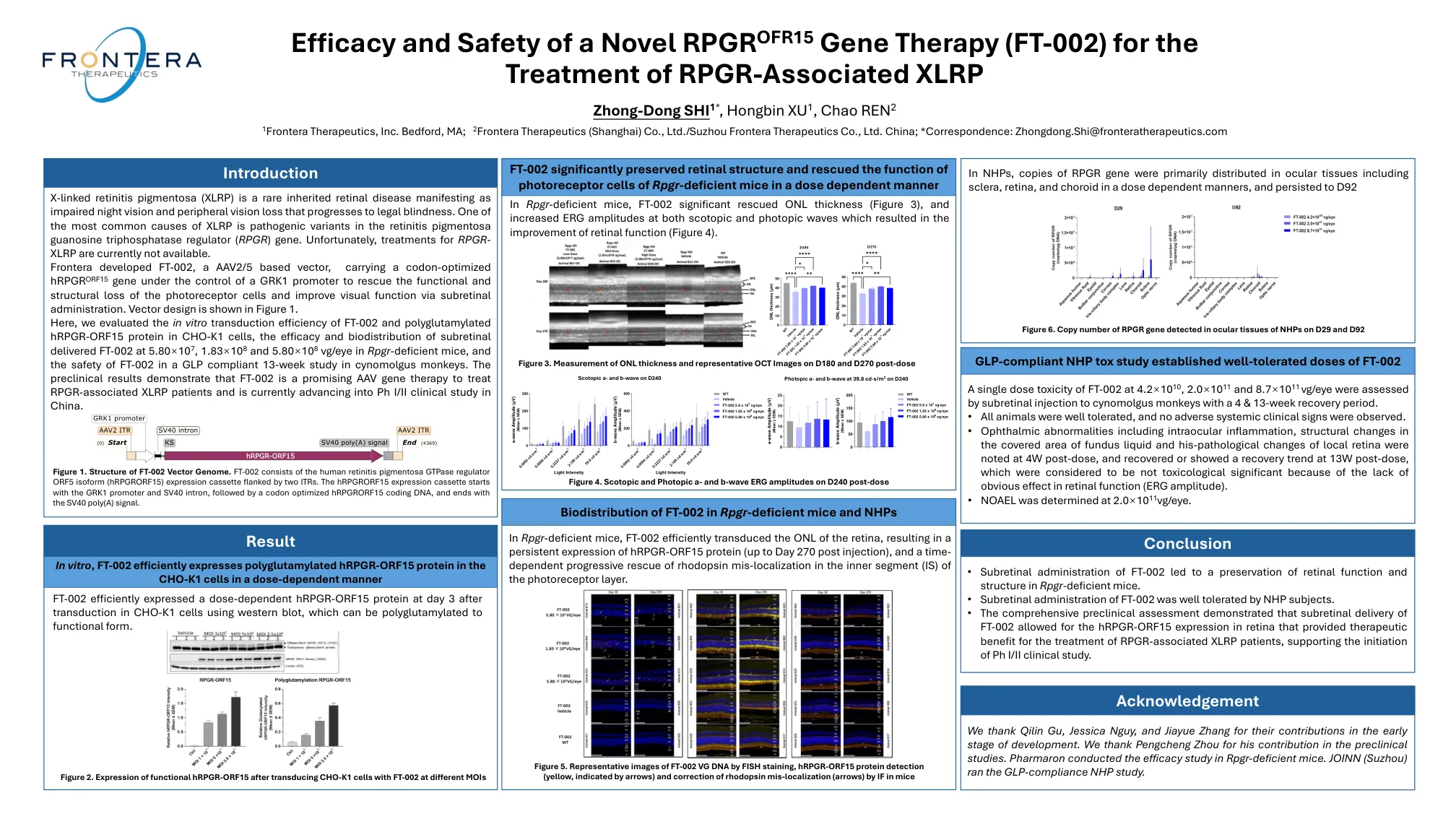
新型RPGroFR15基因疗法的功效和安全性...
X连接的色素性视网膜炎(XLRP)是一种罕见的遗传性视网膜疾病,表现为夜视受损和外围视力丧失,发展为法律失明。XLRP最常见的原因之一是色素性鸟氨酸三磷酸酶调节剂(RPGR)基因中的致病变异。不幸的是,目前尚无RPGR -XLRP的治疗方法。frontera开发了FT-002,这是一种基于AAV2/5的向量,在GRK1启动子的控制下携带密码子优化的HRPGR ORF15基因,以挽救光感受器细胞的功能和结构丧失,并通过下视网膜给药改善视觉功能。向量设计如图1。在这里,我们评估了CHO-K1细胞中FT-002和聚谷氨酰化的HRPGR-ORF15蛋白的体外转导效率,在5.80×10 7,1.83×10 80和5.80×10 8和5.80×10 8 VG/EYSE中,下输送FT-002下输送FT-002的效率和生物分布的效率和生物分布。在一项符合GLP的13周研究中,FT-002在Cynomolgus猴子中。临床前结果表明,FT-002是一种有望治疗与RPGR相关的XLRP患者的有前途的AAV基因疗法,目前正在中国进入PH I/II临床研究。
为...
缩写:基于人O6-烷基鸟氨酸-DNA-DNA-烷基转移酶(夹标签)的小蛋白质标签,簇生定期间隔短的短质体重复序列(CRISPRS)双链破裂(DSB);电子繁殖电荷耦合装置(EMCCD)荧光原位杂交(FISH); Förster共振能量传递点积累用于成像纳米级的topography(fret-paint)高度倾斜和层压光学(HILO)线性分配问题(LAP)发光二极管(LED);晶格灯片(LLS)多阶段关联跟踪(MAT);多种假设跟踪(MHT);均方根位移(MSD)感兴趣的区域(ROI)光活动荧光蛋白(PAFP)纳米级地形(PAINT)概率数据关联(PDA)点分布功能(PSF)定量点积累的纳米级图形(QPAINT)随机跨链接(RCL)RNA RNA CORMASE II(RCL)RNNA PLONASE(RCL)rnNA PORNNA(RCL)概率数据累积(PDA)概率数据均值(PDA)概率数据扩散功能(RCL)RNNA PORNNA(RCL)RNNA PORNNA(RCL)II(RCL)RNNA PORNNA(RCL)概率数据均值积累金属 - 氧化物 - 血症导体(SCMOS)信噪比(SNR)单粒子跟踪(SPT)转录因子(TF)_____________________________________________________________________________________________________________________________________________________
anzchog-stotion-statement-eflornithine-dfmo-use-for- ...
最近已获得美国FDA批准的口服鸟氨酸脱羧酶抑制剂Eflornithine(DFMO),以降低高危神经母细胞瘤复发的风险。dfmo在美国以外不广泛使用,目前尚未在澳大利亚或新西兰获得批准。ANZCHOG实体瘤组承认,虽然DFMO可用于降低HR-NB的风险,但目前,公平的局部DFMO访问已经存在重大障碍。在获得HR-NB的DFMO批准儿童之前,接受了强化诱导化疗,手术,合并疗法,放射治疗和固结后免疫疗法的治疗。所有这些治疗元素均经批准,并广泛用于澳大利亚和新西兰的所有HR-NB患者。儿童肿瘤学组神经细胞瘤生物学研究ANBL00B1(NCT00904241)的最新数据表明,HR-NB儿童的3年免费生存率超过50%。1,2显然需要额外的疗法来减少高危神经母细胞瘤复发并提高生存率。ANZCHOG实体瘤组继续与合作伙伴合作,包括澳大利亚神经母细胞瘤,家庭,倡导者,制药公司和政府,以促进澳大利亚和新西兰的HR-NB的及时,本地,公平,资助的DFMO访问权限,并鼓励当地的注册以及长期访问。ANZCHOG实体瘤组:
ribbontail stingray皮肤采用核心壳光子玻璃超微结构制成蓝色结构颜色
结构性蓝色在动物中很常见,组织纳米结构和物质系统产生它们(尤其是明亮的蓝色),通常基于高度有序的纳米架构。在这项研究中,我们描述了液体尾丁略皮肤的异常明亮,无关紧要的结构蓝色,这是由更无序的散射元素带来的,这些散射元素具有先前未描述的核心 - 壳超微结构,其中涉及nano-seclets封闭圭鸟氨酸纳米纳米弹丸。我们表明,这种皮肤结构充当细胞内光子玻璃,相干散射蓝色,而密切相关的黑素化器的宽带吸收则消除了光子玻璃的典型低色饱和度。我们对黄貂鱼中皮肤超微结构和颜色的表征展示了如何利用无序系统来产生鲜艳的色调,同时说明基于鸟嘌呤的颜色的能力可能在脊椎动物的演化中很早就出现。此外,采用两种不同的光子现象的材料结构功能协会的材料结构功能关联,说明了纳米级体系结构的演变如何在更大尺寸的尺度上具有深远的影响(例如,在视觉生态学和通信中),并为颜色效应的光效率覆盖了基本的指南。
临床试验的结果 - 您可能对
作为NGBMS的一线疗法,Temozolomide的有效性自然受到了特别的关注,并且也在RGBMS中进行了测试。Temozolomide在1999年和2000年的两个II期试验中达到了令人满意的功效和可接受的安全性(10,11)。但是,在2007年II期对CNS肿瘤儿童的试验中,替莫唑胺的客观反应率(ORR)不符合预期(12)。我们认为,这种偏差可能是由于肿瘤病理学的差异。此外,救援试验建议连续剂量强症替莫唑胺方案作为主动选择,而6个月的PFS为23.9%(13)。The methylated O 6 - methylguanine DNA methyltransferase ( MGMT ) promoter was identified as a strong beneficial prognostic biomarker for temozolomide rechallenge in both the RESCUE trial and DIRECTOR trial ( 14 ).此外,II期双臂主管试验表明,接受最后一次替莫唑胺的患者对剂量强化的Temozolomide rechallenge的反应更好。o 6-在临床前研究中,已证实苄鸟氨酸,二硫酸酯和铜被证实为替莫唑胺敏化剂。不幸的是,这些药物并未增强替莫唑胺抗性RGBMS中替莫唑胺的治疗作用(15,16)。抗替莫唑胺抗性神经胶质瘤的最佳策略仍然难以确定,而替莫唑胺的甲基阵利可用于甲基化的MGMT启动子患者。