XiaoMi-AI文件搜索系统
World File Search System一组患有风湿性疾病的 COVID-19 患者的临床病程、严重程度和死亡率
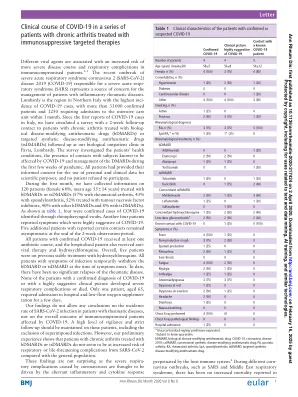
在这项描述性回顾性研究中,我们旨在描述这些患者的严重程度和死亡率相关特征以及免疫调节药物对感染病程的影响。研究对象为 2020 年 2 月 25 日至 2020 年 6 月 8 日期间在拉巴斯大学医院风湿病科就诊的患有 COVID-19 感染和风湿性炎症疾病的患者。共纳入 122 名患者。其中 100 名(82.0%)通过鼻咽拭子确诊。22 名患者(18.0%)表现出相符的症状,且肺部影像学检查结果相符和/或血清学检查呈阳性。患者特征如表 1 所示。单因素分析显示,与住院相关的变量(表 2)包括年龄(5 年间隔;OR 1.34,95% CI 1.17-1.55)、泼尼松剂量 >5 mg/天(OR 2.55,95% CI 1.07-5.59)、慢性肺部疾病(OR 5.34,95% CI 1.47-19.35)和高血压(OR 4.06,95% CI 1.79-9.19)。住院的独立危险因素是甲氨蝶呤(OR 2.06,95% CI 1.01-5.29)和年龄(5 年间隔;OR 1.31,95% CI 1.11-1.48)。未发现与羟氯喹、其他常规抗风湿药物 (cDMARDs)、靶向合成抗风湿药物或生物抗风湿药物 (bDMARDs) 或实验室参数有任何关联。甲氨蝶呤治疗与年龄、性别、糖皮质激素或风湿病亚型无关。14 名患者 (11.5%) 死于呼吸衰竭。9 名患者使用 cDMARDs(单药或联合治疗),1 名使用 bDMARD(利妥昔单抗),4 名仅服用口服糖皮质激素。羟氯喹在死亡率方面没有差异。单变量分析显示,与死亡相关的因素包括年龄(OR 1.60,95% CI 1.20- 2.01)、动脉高血压(OR 12.17,95% CI 2.58-57.38)、肺部疾病(OR 5.36,95% CI 1.60-17.94)和泼尼松剂量>5 mg/天(OR 5.70,95% CI 1.63-19.92)。最近爆发的 COVID-19 引起了人们对炎症性风湿病患者管理的担忧。然而,一些报告表明,通常用于治疗风湿病的治疗方法可能对 COVID-19 有效。 4 在我们的系列研究中,与其他群体相比,因感染严重而需要住院的患者比例较高 (56.6%),这可能是由于合并症患病率较高,尤其是高血压,糖皮质激素的使用率较高或对更严重病例的潜在选择偏见。5 6
评估孟加拉国成年男性MPOX感染的疫苗感知和疫苗接种意图:横断面研究结果
POXVIRIDAE家族的正托病毒属包含称为MPOX(Monkeypox)病毒的封闭的双链DNA病毒。MPOX病毒分为两个遗传进化枝:中非(刚果盆地)进化枝和西非进化枝[1,2]。2022年11月28日,世界卫生组织(WHO)将这种疾病重命名为MPOX,以避免污名和种族主义[3]。mpox是一种人畜共患病,可以通过与灵长类动物和几种啮齿动物物种直接接触到人[1]。1959年,从新加坡到丹麦研究中心的一批生病的猴子导致了MPOX病毒的第一个隔离和鉴定。该病毒是在刚果民主共和国的一个孩子中确定的,但人们认为这是天花,但这是人类中首次疾病的事件[4,5]。然而,当涉及并发症,病例死亡和疤痕的率时,MPOX不如天花[5-7]。有许多MPOX的流行病,这些流行病因人而异[8,9]。通过呼吸液滴传播并与受感染者的病变直接接触正在引起目前的爆发。根据最近的数据,MPOX也可能发生性传播[4,10,11]。在西非的人们和野生动物水库之间经常接触,并且有证据表明传染性攻击率正在上升,MPOX已被确定为日益增长的公共卫生危害[5]。但是,这可能会发生,因为男人经常与野生动物进行狩猎和互动[4,12]。MPOX病毒在病毒入口后通过任何途径(内皮内,鼻咽和口咽和口咽)复制,并随后扩散到附近的淋巴结。根据研究,孵育期持续5到21天,体征和症状持续2到5周。发烧,头痛,肌痛,嗜睡和淋巴结肿胀是疾病之前的一些体征和症状。各种尺寸的皮疹从发烧开始后的1到5天开始,首先在面上,并且可能会或可能不会传播到身体的其他区域[4,5]。在2022年,各大洲的几个国家都有广泛的MPOX爆发,主要影响与男性发生性关系(MSM),Bisexalual和Gay的男人。在西班牙,发现595例MPOX病例中有99%在MSM人群中,其中病变主要影响生殖器,耕地和会阴区域。人类MPOX病例的增加突出了预防策略的价值以及早期筛查和识别[13]。MPOX最近已成为全球健康问题,WHO报告了80,000多个欧洲,西太平洋,东南亚,美洲和东地中海的超过90个国家的已验证和可疑案件。此外,可能无限期地增加的实例数[3,14,15]。对
麻疹(Rubeola) - OEPS -WV.GOV
麻疹概述什么是麻疹?麻疹(rubeola)是由一种高度传染性的帕托氏病毒引起的,该病毒仅具有一种抗原类型。这是一种急性,病毒,全身感染,主要是鼻咽呼吸道上皮的。病毒在呼吸上皮和区域淋巴结中侵入并复制。麻疹的特征是发烧缓慢增加(峰值至105 0 F),然后是暴露后10至12天发生的咳嗽,Coryza或结膜炎;前景持续2-4天(范围1-7天)。koplik斑点在口腔皮疹后1-2天到1-2天之前,在口腔颊(脸颊)粘膜的鲜红色背景上显示为点状蓝白色斑点。它被认为是麻疹和。暴露后14天(范围7-21天)通常会出现刺激性喷发。皮疹从发际线开始,从头到尾向下蔓延到四肢,持续5-6天。皮疹似乎是离散的,但可能会汇合。皮疹以与出现的顺序相同的顺序褪色。麻疹的其他症状和/或并发症可能包括耳朵感染,腹泻,中耳炎,肺炎,肝炎,脑炎和死亡。5岁以下的儿童和20岁以上的成年人更有可能患有麻疹并发症。麻疹也可能导致自发流产,过早出生或如果孕妇在怀孕期间感染的女性。麻疹的治疗方法是什么?没有针对麻疹的特定治疗方法。考虑到患者的临床表现(见上文),实验室结果(请参阅实验室测试部分)和暴露风险,应进行麻疹诊断。可以提供支持性护理以减轻症状并解决并发症。传播与预防麻疹有多常见?麻疹是在2000年正式从美国淘汰的,这意味着该国没有麻疹传播,只有在某人在国外签约麻疹并返回该国并与处于危险的人群接触(未接种或对麻疹的疫苗接触)才能找到新病例。截至2024年4月,19个司法管辖区报告了总共126例麻疹病例:亚利桑那州,加利福尼亚,佛罗里达州,乔治亚州,伊利诺伊州,印第安纳州,路易斯安那州,路易斯安那州,马里兰州,密歇根州,密歇根州,密苏里州,密苏里州,新泽西州,新泽西州,新泽西州,新泽西在2024年报告了7次爆发(定义为3个或更多相关案件)。国际旅行后,西弗吉尼亚州的最后一次报道的麻疹病例是在2024年4月。在2024年之前,在2009年报告了WV的最后一例麻疹。
英国脑膜炎球菌病公共卫生管理指南
脑膜炎奈瑟菌是全球败血症和脑膜炎的主要原因,可导致大量死亡以及幸存者严重的长期后遗症 (1)。六种脑膜炎球菌荚膜群 (A、B、C、W、X 和 Y) 以其多糖荚膜为特征,可导致几乎所有人类侵袭性感染。流行病学因血清群和克隆复合体组合而异。脑膜炎球菌通常定植于鼻咽部,携带率在儿童期增加,在 18 至 20 岁达到峰值,随后下降 (2,3)。携带期可能持续数月 (4)。侵袭性疾病是感染的罕见结果,但从病例到密切接触者的进一步传播很少会导致继发病例和聚集性感染 (5、6、7)。然而,不到 2% 的侵袭性脑膜炎球菌病 (IMD) 病例被认为是与原发性 IMD 病例密切接触所致 ( 8 )。2014 年,在引入常规 MenB 婴儿和 MenACWY 青少年疫苗接种之前,英国所有年龄组的年 IMD 发病率约为每 100,000 人 1.2 人 ( 9 )。以血清杀菌抗体衡量的全身免疫力通常在感染脑膜炎球菌后 14 天内形成 ( 10 )。罕见的是,感染可能会在免疫力形成之前发展为侵袭性疾病。根据实验室获得性感染研究 ( 11 )、已知接触日期的偶尔聚集性感染 ( 12 ) 以及军队新兵携带研究 ( 13 ) 的数据,该潜伏期通常为 3 至 5 天。已确诊的脑膜炎球菌携带者通常不会患上侵袭性疾病 ( 13 )。感染后罹患侵袭性疾病的风险可能因环境和宿主因素而异,但也主要取决于所感染菌株的特性。仅有极小部分携带菌株会导致侵袭性疾病 ( 14 )。针对 C 组脑膜炎球菌 (MenC) 的结合疫苗自 20 世纪 90 年代末开始面世,针对 A、C、W 和 Y 组脑膜炎球菌 (MenACWY) 的四价结合疫苗已在欧洲获得许可近 20 年。2013 年初,一种专门为预防 B 组脑膜炎球菌 (MenB) 引起的疾病而开发的新疫苗在欧洲获得许可(4CMenB,Bexsero®,GSK Biologicals,比利时)。该疫苗不同于之前存在的 MenC 和 MenACWY 结合疫苗,因为它是基于蛋白质的,因此与结合疫苗相比具有不同的作用机制,并且在不同年龄组中具有不同的安全性、反应原性和免疫原性特征 ( 15 )。2017 年,另一种使用二价脂质化 fHbp (rLP2086,Trumenba®;辉瑞) 的 MenB 疫苗在欧洲获得许可。rLP2086 (Trumenba®) 目前获准用于 10 岁及以上的个人。本指导原则包括 MenB 疫苗在 IMD 病例和接触者公共卫生管理中的潜在用途。
检测和鉴定医学重要性细菌
引言葡萄球菌是在环境中抵抗最大的非孢子细菌。在干燥的临床样品中可能存活数月,具有相对耐热性,可以耐受盐浓度升高。然而,尽管存在抗菌素,改善了卫生条件和医院感染控制措施,但这种微生物仍然是人类最重要的病原体之一。健康的个体通过金黄色葡萄球菌从母乳喂养中间歇性地殖民,并且可以在鼻咽中容纳微生物,偶尔在皮肤上,而在阴道中很少。在这些部位,金黄色葡萄球菌可能通过直接接触或气溶胶污染患者的皮肤和粘膜,无生命的物体或其他患者,从而导致致命的感染因毒力或对当前使用的抗菌药物的抗性而导致致命感染。葡萄球菌葡萄球菌引起的感染病例部分抗性抗生素,例如万古霉素,而阴性葡萄球菌凝结酶的报道必须发展出抗性。因此,需要快速有效地识别这些微生物出现的所有情况。链球菌是抗抗生素时代医院感染的最大原因,导致感染和产后妇女死亡。肠球菌的重要性越来越重要,因为由于传统上用于治疗这些感染的抗生素几乎完全抵抗力,引起了医院感染。尽管目前不是医院感染的重要原因,但是即使在免疫能力的患者中,它们也会引起非常严重且经常致命的疾病,并且该药物的快速诊断很重要。最常见的肠球菌是:粪肠球菌(占病例的90%)和肠球菌粪便,患者的殖民能力较大,医院使用的污染表面或设备。它们对称为糖肽的抗生素具有敏感性或可变性,例如万古霉素和二甲苯蛋白酶。目前有天然可抗性的共生菌株可以从住院的患者中隔离,但尚无法引起暴发,但应正确识别。初步鉴定链球菌和葡萄球菌的鉴定基于液体培养基中存在的形态。由于链球菌是通常的长链,葡萄球菌以椰子的形式证明了葡萄卷曲或分组。识别推定始于对RAM血板上的主要接种,该接种应在5%CO²中孵育(蜡烛方法或煤炭2)。葡萄球菌菌落通常更大,凸面,着色范围从白色到黄色,并且可能有溶血。应注意的是,金黄色葡萄球菌中淡黄色的发育仅在室温下长时间孵育(72 h)后才发生。链球菌菌落倾向于较小(untiforms),并且总溶血卤素(β和α溶血)。p riva da c atalase带有细菌环或牙签将可疑菌落的中心收集,并摩擦到玻璃刀片中。将3%过氧化氢下降到此涂片上,并观察到气泡的形成。对于家族微核心素(葡萄球菌),证明通常为正,而对于链球菌家族(链球菌)为阴性。
接受免疫抑制靶向治疗的一系列慢性关节炎患者的 COVID-19 临床病程
不同的病毒因子与免疫功能低下患者病情加重和呼吸系统并发症的风险增加有关。1–3 最近爆发的严重急性呼吸综合征冠状病毒 2 (SARS-CoV-2) 疾病 2019 (COVID-19) 导致严重急性呼吸综合征 (SARS),这引起了对炎症性风湿病患者管理的担忧。伦巴第大区是意大利北部 COVID-19 病例发病率最高的地区,确诊患者超过 33,000 例,1,250 例患者在 1 个月内需要进入重症监护室。自意大利首次报告 COVID-19 病例以来,我们已对在伦巴第大区帕维亚的生物门诊接受生物抗风湿药物 (bDMARDs) 或靶向合成抗风湿药物 (tsDMARDs) 治疗的慢性关节炎患者进行了为期两周的随访调查。调查内容包括患者的健康状况、与已知受 COVID-19 影响的受试者的接触情况以及在疫情爆发的头几周内对 DMARDs 的管理情况。所有患者均已知情同意将个人和临床数据用于科学目的,并且没有患者拒绝参与。在第一个月内,我们收集了 320 名接受 bDMARDs 或 tsDMARDs 治疗的患者(女性占 68%,平均年龄 55±14 岁)的信息(57% 患有类风湿性关节炎,43% 患有脊柱关节炎,52% 接受肿瘤坏死因子抑制剂治疗,40% 接受其他 bDMARDs 治疗,8% 接受 tsDMARDs 治疗)。如表 1 所示,四例是通过鼻咽拭子发现的 COVID-19 确诊病例。另有四名患者报告的症状高度提示是 COVID-19。另外五名报告有某些接触的患者在两周观察期结束时仍无症状。所有确诊的 COVID-19 患者均接受了至少一疗程的抗生素治疗,住院患者还接受了抗病毒治疗和羟氯喹治疗。总体而言,五名患者之前均接受过羟氯喹的稳定治疗。所有出现感染症状的患者在症状出现时均暂时停用 bDMARD 或 tsDMARD。迄今为止,风湿病没有出现明显复发。确诊为 COVID-19 或临床表现高度可疑的患者均未出现严重呼吸道并发症或死亡。只有一名 65 岁患者需要住院并接受几天的低流量吸氧。我们的研究结果无法得出有关风湿病患者 SARS-CoV-2 感染发病率的任何结论,也无法得出有关 COVID-19 免疫功能低下患者的总体结果的任何结论。应对这些患者保持高度警惕并严格随访,包括排除叠加感染。然而,我们的初步经验表明,与普通人群相比,使用 bDMARDs 或 tsDMARDs 治疗的慢性关节炎患者似乎不会因 SARS-CoV-2 而增加呼吸道或危及生命的并发症的风险。这些发现并不令人惊讶,因为冠状病毒引起的严重呼吸道并发症被认为是由异常的炎症和细胞因子反应引起的
感染麻疹的风险增加
2025 年 1 月 31 日背景:新墨西哥州卫生部 (NMDOH) 通知医疗保健提供者,过去两周内德克萨斯州至少确诊了四例麻疹病例,分别来自盖恩斯县 (2) 和哈里斯县 (2)。盖恩斯县与新墨西哥州利县接壤。德克萨斯州卫生服务部正在调查更多疑似麻疹病例以及是否有任何接触发生在新墨西哥州。鉴于州居民经常跨越州界,考虑麻疹暴露风险增加是明智之举。虽然新墨西哥州目前没有确诊病例,但医疗保健提供者应警惕任何年龄的未接种疫苗或接种不足的患者出现发热性皮疹,尤其是那些最近旅行或接触过已知病例(例如德克萨斯州的病例)的患者。重要的是让您的患者及时接种麻疹疫苗,并及时识别、隔离、报告和检测疑似麻疹患者以防止进一步传播至关重要。对临床医生的建议:麻疹的特征是发烧、不适、咳嗽、鼻炎和结膜炎的前驱症状,随后出现斑丘疹。皮疹从头部开始,向下蔓延至全身,通常在接触后约 14 天出现,但范围从接触后 7-21 天不等。麻疹患者在皮疹开始前 4 天到皮疹出现后 4 天具有传染性。麻疹传染性极强,NMDOH 建议不允许疑似麻疹患者(分诊时发烧和出疹)与其他人一起在候诊室。最好先在诊所外对患者进行评估。如果怀疑是麻疹,立即将患者隔离在负压室。如果您的机构没有负压室,请确保患者戴上口罩并安置在有门的私人房间中。疑似麻疹患者所住的任何房间在患者离开后两小时内都不应使用,因为在此期间麻疹病毒仍悬浮在空气中。应指导疑似麻疹患者在出疹后四天内在家中自我隔离。高风险接触者(例如孕妇或免疫功能低下者)可能需要进一步评估。大约五分之一的麻疹病例需要住院治疗。如果怀疑是麻疹,应获取血清样本进行 IgM 检测,并获取咽拭子或鼻咽拭子,置于病毒运输培养基中,进行 PCR 检测。如有任何疑似麻疹病例,请立即通知卫生部门,电话是 1-833-SWNURSE(1-833-796-8773),24/7 全天候服务。目前已有安全且高效的麻疹疫苗,医疗机构应确保所有工作人员都接种了两剂 MMR 疫苗,或有实验室证据表明对麻疹具有免疫力。MMR(麻疹-腮腺炎-风疹)疫苗获准供 12 个月或以上的人群使用;MMRV(麻疹-腮腺炎-风疹-水痘)疫苗获准供 12 个月至 12 岁的人群使用。一剂的平均有效率为 93%,而两剂的平均有效率为 97%。
2020 年 3 月 1 日至 2022 年 4 月 2 日大学教职员工 COVID-19 发病率及疫苗有效性
摘要:背景:大学工作人员与学生和同事频繁接触,并在拥挤的环境中上课,因此需要进行频繁的社交互动。我们的研究旨在评估 2020 年 3 月 1 日(疫情开始)至 2022 年 4 月 2 日期间里雅斯特大学一组工作人员的 COVID-19 感染率和疫苗有效性。方法:里雅斯特大学实施了一系列公共卫生政策,以遏制校园内 SARS-CoV-2 的传播,包括及时追踪接触者、加强所有场所的通风、对污染物进行消毒以及在室内强制佩戴口罩。根据当地公共卫生部门的监测规程,在出现与 COVID-19 相符的症状时,或在与确诊的 COVID-19 病例密切接触后进行接触者追踪时,大学人员会根据要求通过聚合酶链反应 (PCR) 对鼻咽拭子进行 SARS-CoV-2 检测。 SARS-CoV-2 感染的发病率以病例数除以处于风险中的人日数 (pd) 来估计。采用多变量 Cox 比例风险回归模型来调查原发性 COVID-19 感染的风险,控制了许多潜在的混杂因素,并将风险表示为调整后的风险比 (aHR),置信区间 (95% CI) 为 95%。结果:大学教职员工的 SARS-CoV-2 感染率低于同一地区的卫生保健工作者 (HCW)。与未接种疫苗的同事 (6.55 × 10,000 pd) 相比,接种一剂 (7.22 × 10,000 pd) 或两剂 (7.48 × 10,000 pd) 的大学工作人员的 SARS-CoV-2 感染原始发病率更高,而接种加强剂 (1.98 × 1000 pd) 的工作人员的 SARS-CoV-2 感染原始发病率较低。感染风险仅在医学研究生中增加(aHR = 2.16;95% CI:1.04;4.48),尽管这仅限于 Omicron 传播期。在实施全国 COVID-19 疫苗接种运动后,接种加强针的工人在 Omicron 传播期之前(aHR = 0.10;95% CI:0.06;0.16)和之后(aHR = 0.37;95% CI:0.27;0.52)感染 SARS-CoV-2 的可能性均低于未接种疫苗的工人。加强剂的疫苗有效率为 Omicron 疫苗接种前 90% (=(1 − 0.10) × 100),而 Omicron 疫苗接种期间 63% (=(1 − 0.37) × 100),同源免疫(三剂 m-RNA 疫苗)和异源免疫(前两剂 Vaxzevria,然后是第三剂 m-RNA 疫苗)之间没有显着差异。结论:大学教职员工的 SARS-CoV-2 感染率低于 ASUGI 的 HCW,可能是因为按需检测计划不可避免地错过了绝大多数无症状感染。因此,在大学人员中观察到的加强剂量的显着保护作用是指有症状的 SARS-CoV-2 感染。的里雅斯特大学实施的感染预防和控制政策成功平衡了行政人员和教学人员之间的生物风险。
COVID-19改变人类微生物:一种荟萃分析
新型β-核可纳病毒,严重急性呼吸综合征-2(SARS-COV-2)的出现和快速传播引起了全球严重且前所未有的公共健康和社会经济挑战(Waters等,2022)。主要是,COVID-19表示具有可变严重程度的多方面和多器官感染。症状范围从急性呼吸窘迫综合征到肺炎,包括非特异性症状症状,胃肠道症状,心肌功能障碍,多器官衰竭和死亡(Kumar Singh等,2019; Baud等,2019; Baud et al。在大多数情况下,SARS-COV-2感染者是无症状的,要么表现出轻度的症状。然而,大约有5%的感染者(通常是合并症的老年人和/或个人)发展出严重的疾病形式,导致重症监护和死亡(Grasselli等,2020; Wiersinga等,2020)。截至2023年4月,在全球范围内有762,791,152个确认的Covid-19案件,其中有6,897,025例死亡率(Who Coronavirus(coronavirus(covid-19)仪表板)。在与COVID-19感染相关的许多长期作用中,许多研究报道了COVID-19患者的微生物群改变。人类微生物组在宿主健康中起着至关重要的作用(Kumpitsch等,2019),并被认为是额外的器官(Baquero和Nombela,2012年)。这些微生物群落通过复杂而基本的相互作用维持宿主的稳态,从而改善了免疫调节,代谢,器官功能,粘膜屏障完整性以及针对入侵病原体的结构保护(Jandhyala等,2015; Kumpitsch等,2019)。特定的微生物群落与不同的人体组织有关(人类微生物组项目联盟,2012; p flughoeft and versalovic,2012)。扰动(例如COVID-19)可能会导致人类微生物组中的微生物组营养不良,其中有益和/或共生微生物的组成和多样性改变了生长或机会性病原体,从而促进了生长或机会性病原体(Hoque等,2021b; 2021b; Ren等; Ren等,20221; 2022; 2022; 202222222。尤其是,观察到与不健康的宿主相关的微生物中增加的宿主到宿主变异性的观察被称为Anna Karenina原理(AKP),该原则(AKP)源自Tolstoy的Anna Karenina的开场线:“所有幸福的家庭都是所有不幸的家庭;每个不幸福的家庭都是不幸的。”据报道,包括肥胖,牛皮癣,关节炎,炎性肠病(IBD),infuenza,hbv和HIV的不同人类疾病显着改变了人类微生物组(Ling等人(Ling等)(Ling等,2015; Lu et al。 2019; Sencio等人,2021年)。同样,有几份报告表明,在主动感染和恢复状态期间,Covid-19患者的微生物(肠道,鼻咽和口服)的变化,通常以有益的儿童微生物和更高的机会病原体的丰富度来表征,ZUO ZUO ET。 2021a,Jochems等人,2021年;肠道,鼻或口服微生物组的组成和多样性现在被人们普遍认为可以预测COVID-19的预后,进展和严重程度(Mathieu等,2018; Wypych et al。肠道,鼻或口服微生物组的组成和多样性现在被人们普遍认为可以预测COVID-19的预后,进展和严重程度(Mathieu等,2018; Wypych et al。