XiaoMi-AI文件搜索系统
World File Search Systemalirocumab
PCSK9抑制剂 - 新加坡
1.1。在2023年6月的会议上,MOH药物咨询委员会(“委员会”)考虑了用于对原始蛋白转化酶的技术评估提供的证据,该croversisin/kexin/kexin型9型(PCSK9)抑制剂(alirocumab,evolocumab and evolocumab and cansiriran)用于治疗非果糖超固醇和hytremer selliroil(nonypholeter)(nonypholeter)(hytremer)(hytremer)(hytrolyer)(hertyers)(hertyrem norkial)(herterair)(hertyer)heterairiz和herterairizg(herterairiz) (hefh)。evolocumab用于治疗纯合家族性高胆固醇血症(HOFH)的证据。医疗机构(ACE)与公共医疗机构的临床专家和当地患者和志愿组织的患者专家进行了协商。根据注册指示,考虑了每个PCSK9抑制剂的临床和经济证据。
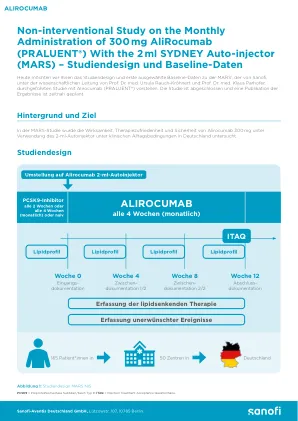
研究设计和基线数据
活性成分:Alirocumab。成分:药物。有效的内容:预充式笔/注射器,1 毫升溶液中含有 75/150 毫克阿利库单抗;预充笔,含有 2 毫升溶液中的 300 毫克阿利库单抗。否则。成分:组氨酸,蔗糖,聚山梨醇酯20,注射用水。适应症:原发性高胆固醇血症和混合性血脂异常:作为饮食b的辅助。患有原发性高胆固醇血症或混合性血脂异常的成人以及儿童和青少年。年龄8岁及以上,患有杂合子家族性高胆固醇血症。 m. 他汀类药物或他汀类药物及其他药物。降脂治疗 b.患有他汀类药物的患者。 LDL-C目标值未达到。或作为单一疗法或组合m. 降脂治疗 b.他汀类药物不耐受患者或如果他汀类药物有禁忌症。现有动脉粥样硬化性心血管疾病:患有现有动脉粥样硬化性心血管疾病的成年人。通过降低 LDL-C 水平以及纠正其他风险因素来降低心血管风险:联合使用。 m. 最大可容忍他汀类药物治疗联合或不联合其他治疗降脂治疗原则或单一疗法。或组合与其他人一起。降脂他汀类药物不耐受患者的治疗原则或当他汀类药物有禁忌症时。禁忌症:超敏反应针对活性成分或其他成分副作用:免疫系统:罕见:超敏反应过敏性血管炎。呼吸道/胸部/内侧圣:常见:临床体征和症状我。的面积上呼吸道。皮肤/皮下组织:常见:瘙痒;罕见:荨麻疹、牛皮癣。湿疹;未知:血管性水肿。一般/投诉一个。管理站点: 通用:React。广告注入站点;未知:流感样疾病仅限处方。营销授权持有人:Sanofi Winthrop Industrie,82 avenue Raspail,94250 Gentilly,法国。当地代表营销授权持有人:Sanofi-Aventis Deutschland GmbH,D-65926 Frankfurt am Main。状态:2023 年 11 月
proprotein转化酶枯草蛋白Kexin 9型抑制剂
•成年人中建立的心血管疾病(CV)疾病,以降低心肌梗塞(MI),中风和冠状动脉血运重建的风险。•原发性高脂血症(包括杂合家族性高胆固醇血症[HEFH]),在成年人中作为饮食的辅助,单独或与其他低密度脂蛋白胆固醇(LDL-C) - 较低的较低的脂肪蛋白(LDL-C) - 较低的疗法相结合,以减少LDL-C。 •HEFH,在≥10岁的小儿患者中,作为饮食和其他LDL-C降低疗法的辅助。•纯合性家族性高胆固醇血症(HOFH),≥10岁的患者,作为饮食和其他低密度脂蛋白(LDL)的辅助 - 降低疗法(例如汀类药物,Ezetimibe,ezetimibe,ldl长椅)以减少LDL-C。尚未在年龄少于10岁的HEFH或HOFH患者的儿科患者中确定Repatha的安全性和有效性。1另一种可用的PCSK9抑制剂是Praluent®(alirocumab皮下注射)。2leqvio®
PCSK9抑制剂在家族性高胆固醇血症中的有效性:可行性分析
高胆固醇血症(FH)。但是,加拿大PCSK9I现实世界中的好处的数据有限。这项研究的目的是1)确定通过PCSK9I实现建议治疗目标的患者的百分比,以及2)估计处方PCSK9I的FH患者中心血管事件的发生率。使用来自艾伯塔省,不列颠哥伦比亚省和安大略省省的行政医疗保健数据,我们将在2015年至2023年之间确定开始使用PCSK9I(Alirocumab或Evolocumab)治疗的患者。PCSK9I与FH的发起人可能会使用公共报销作为FH的指标来确定。将描述PCSK9I启动时的患者特征。我们将确定获得公共药物计划的患者的百分比'推荐治疗目标,即在PCSK9I治疗期间,低密度脂蛋白胆固醇水平至少降低了40%。将估计重大不良心血管事件和血栓性事件的发生率。
PCSK9抑制剂和心血管事件的减少
普罗蛋白转化酶枯草蛋白/Kexin型9(PCSK9)在低密度li- protrotein(LDL)代谢中起重要作用。药理学PCSK9抑制剂已被开发为治疗血脂异常的新方法。本文回顾了涉及PCSK9在脂质代谢中作用以及PCSK9抑制剂对脂质参数和心血管风险的临床影响的证据范围。生化和基因组研究已经确定了PCSK9在PCSK9缺乏症的情况下观察到的PCSK9在脂质代谢中所起的作用。This led to the development of inhibitory monoclonal antibodies (evolocumab, alirocumab) that produce dose-dependent lowering of LDL cholesterol up to 60%, with evidence of regression and stabilization of coronary atherosclerosis (GLAGOV, HUYGENS, PACMAN-AMI) and reduction in cardiovascular risk in large clinical outcomes trials (FOURIER, ODYSSEY结果)。最新的事态发展目睹了PCSK9抑制作用的替代方法,例如RNA干扰(含有),疫苗和基因编辑,这些方法目前正在接受临床评估。PCSK9抑制已成为降低LDL胆固醇的治疗方法的重要组成部分,并在预防策略中起着越来越多的作用。
治疗高脂血症的疗法
摘要:高脂血症是代谢紊乱性疾病之一,是常见的公共卫生问题,其特征是胆固醇、甘油三酯和/或脂蛋白水平升高,是2型糖尿病、非酒精性脂肪肝、心血管疾病等多种疾病的危险因素。目前,治疗高脂血症的主要药物是他汀类药物和抗前蛋白转化酶枯草溶菌素9(PCSK9)的单克隆抗体药物。他汀类药物长期使用的主要限制是副作用难以耐受。Evolocumab和Alirocumab是两种抗PCSK9的单克隆抗体,可有效降低他汀不耐受患者和家族性高胆固醇血症患者的低密度脂蛋白胆固醇(LDL-C),且副作用较少。然而,由于单克隆抗体的半衰期短、成本高,可能导致患者不依从用药,给患者带来巨大的经济负担。鉴于RNA在基因调控中起着关键作用,基于RNA的疗法已成为设计新型抗高脂血症药物的有力蓝图。本文,我们总结了基于RNA的治疗策略以及目前RNA药物在高脂血症治疗中的临床试验。
医疗政策-PCSK9抑制剂
- 普罗蛋白转化酶枯草蛋白/Kexin型(PCSK9)是一种蛋白质,靶向LDL受体降解并降低肝脏从血液中去除循环LDL的能力。循环PCSK9水平升高与低密度脂蛋白胆固醇(LDL-C)的水平升高,因此心血管结局恶化。PCSK9的抑制剂与循环PCSK9结合,并防止其与肝表面上的LDL受体结合并降解,从而导致更多的LDL受体从血液中去除循环的LDL。- FDA已批准的前两种完全人类的单克隆抗体,以治疗患有不当治疗水平的LDL -C患者是reptha(evolocumab)和Praluent(Alirocumab)。两者都通过与循环PCSK9结合并防止其与肝表面上的LDL受体结合并降解,从而导致更多的LDL受体从血液中去除循环的LDL。praluent和repatha已显示出同时汀类药物治疗的患者可降低高达60%的LDL-C,并显示出心血管结局的益处。两种产品均已批准以下指示:
除了他汀类药物,还有降低 LDL 胆固醇和心血管事件的新药理学靶点
血脂异常是动脉粥样硬化性心血管疾病 (ASCVD) 的主要可改变风险因素,其药物治疗仍是一个备受争议的问题,不仅在最合适的脂质水平治疗范围方面,而且在最佳策略和顺序方法(分步治疗与上游治疗)方面也存在争议。目前,血脂异常管理的治疗指南侧重于降低低密度脂蛋白胆固醇 (LDL-C) 的强度,根据患 ASCVD 的风险进行分层。除他汀类药物和依折麦布外,监管机构最近还批准了具有潜在创新作用机制的针对 LDL-C 的不同药物,包括前蛋白转化酶枯草溶菌素/kexin 9 型调节剂(单克隆抗体,如 evolocumab 和 alirocumab;小干扰 RNA 分子,如 inclisiran)、ATP-柠檬酸裂解酶抑制剂(bempedoic acid)、血管生成素样 3 抑制剂(evinacumab)和微粒体甘油三酯转移蛋白抑制剂(lomitapide)。了解它们的药理学方面、效益-风险概况,包括对除降低 LDL-C 以外的硬性心血管终点的影响,以及从患者角度(例如依从性)的潜在优势(本循证审查的重点)对于各医学专业的从业者来说至关重要,以尽量减少治疗惰性并支持临床实践。© 2023 作者。由 Elsevier Inc. 出版。这是一篇根据 CC BY-NC-ND 许可 (http://creativecommons.org/licenses/by-nc-nd/4.0/) 开放获取的文章。
内容索引2024心脏,血管和移植
3-D reconstruction 160 6-minute walk test, 6MWT 111 A round cyst-like structure 144, 151 Ablation 173, 200, 422, 540 Accuracy 67, 448, 454 Acute coronary syndrome 438 Acute kidney injury 475 Acute myocardial infarction 154, 163 Acute myocarditis 154, 163 Acute stroke 284, 293腺苷胁迫测试327青少年131,138有氧训练131,138 alirocumab 169肌萎缩性侧面硬化症417解剖成像532解剖154,163,532 Aneurysm 175,435,435,435,435,435,526 Angiosarcomarcoma532 Angiosarcomarcomarcomafya Anatocarcoma Anatocarcoma Anatocarculation 178,488,488,488,488,488,221,221,221,221,221,221,221,221 Anti-N-methyl-D-aspartate 4 receptor encephalitis 145 Aorta 175, 435, 521, 526 Aortic aneurysm 175, 435, 526 Aortic arch aneurysm 526 Aortic coarctation 382 Aortic disease 175, 521 Aortic stenosis 107, 509 Aortic valve replacement 221, 252, 509 Aortic valve sclerosis 469 AQP4-IgG-seropositive neuromyelitis optica spectrum disorder 145 Arrhythmias 1, 23, 144, 151, 165, 173, 319, 336, 371, 422, 540 Aspergilloma 43 Atherosclerosis3 91 Atherosclerotic cardiovascular disease 169 Athlete 493 Athletic heart syndrome 493 Atrial纤颤173、200、371、411房颤,慢心室反应11
用于多重基因的多功能非病毒传递系统...
心血管疾病仍然是全球范围内导致死亡的主要原因,其中血浆低密度脂蛋白胆固醇 (LDL-C) 水平高(或称高胆固醇血症)和血浆甘油三酯水平高(或称高脂血症)是风险的主要决定因素。[1,2] 降低胆固醇是一个有吸引力的治疗目标,LDL-C 降低 30-40% 与心血管疾病风险同时降低相关。[3] 他汀类药物是目前的标准治疗方法,由于不耐受和增加剂量的副作用,10-20% 的高危患者群体被忽视,这促使人们从遗传学角度寻找替代品。 [3,4] 当前蛋白转化酶枯草溶菌素/kexin 9 型 (PCSK9) 的功能获得性突变被确定为常染色体显性高胆固醇血症的病因,导致患者的 LDL-C 水平升高和早期冠心病 (CHD) 时,人们发现了第一个心脏保护基因靶点。[5] PCSK9 的功能丧失序列变异导致 LDL-C 水平显著降低 (40%) 和 CHD 降低 88%。[6] PCSK9 是一种在肝脏中表达的 LDL 受体 (LDLR) 拮抗剂,因此过表达会导致 LDL 受体减少,并降低血浆中的 LDL-C 清除率。[7] 针对 PCSK9 的单克隆抗体被认为是解决他汀类药物尚未满足的重大需求的潜在解决方案。 [8] 然而,PCSK9 抗体(例如 alirocumab)在临床试验中表现出不良反应,包括注射部位反应、神经认知事件、眼科事件和抗药抗体产生。[9] 小干扰 RNA(siRNA),例如 inclisiran,已被开发用于提供与抗体疗法类似的心脏保护作用。[10] 虽然这些 siRNA 能够显著下调 PCSK9,但与这种基因操作方式相关的高脱靶效应仍然令人担忧。CRISPR/Cas9 介导的基因破坏为更高精度、更低频率的治疗提供了一种替代方案。[11]