XiaoMi-AI文件搜索系统
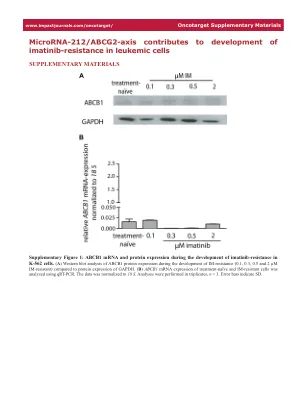
World File Search SystemMicroRNA-212/ABCG2 轴促进白血病细胞产生伊马替尼耐药性
补充图 2:miR-328 依赖性变化导致初治或伊马替尼耐药的 K-562 细胞对伊马替尼的敏感性发生变化,随后分析细胞活力和凋亡。用 25 nM miR 模拟物 pre-miR-328 或 75 nM miR 抑制剂 anti-miR-328 转染 K-562 细胞(初治细胞 (A) 和两种耐药亚系 (0.5 (B)、2 µM (C) IM)),并与 2 µM 伊马替尼孵育 48 小时。在 pre-miR-212 转染和 anti-miR-212 转染后,使用 WST-1 测定法 (上图) 分析细胞活力,使用发光 caspase 9 glo 测定法 (下图) 分析凋亡,以阴性对照转染细胞为标准表示。分析是在三个独立实验中进行的。数据根据各自的阴性对照转染细胞进行标准化。误差线表示 SD,统计分析使用学生 t 检验进行
酪氨酸激酶抑制剂伊马替尼,达沙替尼和尼洛替尼的剂量优化策略用于慢性髓样白血病:从临床试验到
随着酪氨酸激酶抑制剂(TKI)的出现,慢性髓样白血病(CML)的治疗前景明显改变。这种创新可以延长患有CML的患者的长期生存。但是,长期暴露于TKI的伴随着各种不良事件(AE)。后者会影响CML患者的生活质量和依从性,并可能导致严重的疾病进展(甚至死亡)。最近,越来越多的CML患者开始采用剂量优化策略。剂量优化可以在整个治疗的各个阶段考虑,其中包括减少剂量和停用TKIS治疗。通常,在维持分子反应的前提下,TKI剂量的减少被认为是减少AE和改善生活质量的重要措施。此外,对于大约一半的最佳反应和更长的TKI治疗持续时间,TKIS治疗的停用是可行且安全的。本综述主要关注伊马替尼,达沙替尼和尼洛替尼在CML临床试验和现实生活环境中的最新研究。我们将新诊断的患者或最佳反应或改善AE的剂量降低为无治疗缓解的前奏(TFR)或无法停用TKIS治疗的患者的维持治疗。此外,我们还专注于停产TKIS疗法和实现TFR的第二次尝试。
小檗碱及其代谢物的药理学,它是自然界的奥泽米克还是伊马替尼?
背景:小檗碱是一种天然存在的生物碱,被广泛用于多种健康益处,包括体重管理和代谢紊乱。据报道,小檗碱的主要药理作用是通过激活 AMP 活化蛋白激酶,而其其他临床结果缺乏明确的作用机制。因此,本研究使用成熟的 Insilco 工具评估了小檗碱及其两种主要代谢物(小檗红碱和药根碱)在人体中的详细药理学。材料和方法:在 SwissTargetPrediction 服务器中确定了小檗碱及其代谢物的靶标,并使用 AutoDock vina 1.2.0 评估了它们的亲和力。使用 PrankWeb:配体结合位点预测工具评估了最高配体受体组合的结合位点。结果:激酶、酶和 A 家族 GPCR 被确定为小檗碱及其代谢物的三大靶标类别。观察到 ROCK2、PIK3CD、KCNMA1、CSF1R 和 KIT 是小檗碱及其代谢物的高亲和力靶点,亲和力值 <4 uM。小檗碱及其代谢物对所有 AMPK 和脂质/葡萄糖调节靶点(LDLR、DDP4 和 PCSK9)的亲和力均为 >10 uM。小檗碱及其代谢物对 ROCK2 的 IC50 值最小(<1 uM),而其其他高亲和力靶点(PIK3CD、KCNMA1、CSF1R 和 KIT)的 IC50 值 <5 uM。结论:多种多样的蛋白质靶点和观察到的新的亲和力靶点(ROCK2、PIK3CD、KCNMA1、CSF1R 和 KIT)为小檗碱及其代谢物在各种疾病条件下的潜在作用机制和治疗效果提供了有价值的见解,值得在合适的功效分析研究中进行验证。
四名接受伊马替尼治疗的慢性粒细胞白血病儿童接种减毒活疫苗
儿童和青少年慢性粒细胞白血病 (CML) 是一种罕见的恶性肿瘤,可用酪氨酸激酶抑制剂 (TKI) 伊马替尼成功治疗。根据目前的经验,需要多年的治疗,在大多数情况下,需要终身治疗才能控制恶性疾病。伊马替尼在不同年龄组中引起免疫抑制的程度是一个有争议的讨论。根据一般医疗建议,接受伊马替尼治疗的个体禁用活疫苗。然而,最近全球报告的麻疹病例数量有所增加,并且还在继续上升。由于病毒传染性强,需要近乎完美的疫苗接种覆盖率(93% 至 95% 的群体免疫率)才能有效防止麻疹复发——这种情况在许多国家并不现实。当四名患有 CML 的青少年(平均年龄 13 岁,范围 12-15 岁)在接受伊马替尼治疗(平均治疗持续时间 36 个月,范围 11-84)期间被纳入儿童试验 CML-paed II 时,发现他们没有保护性麻疹和/或水痘滴度,我们仔细权衡了在免疫抑制 TKI 药物下接种活疫苗的风险与获得保护的好处。患者同时接种减毒活疫苗 MM-RVAX Pro R ⃝ 和 Varivax R ⃝(患者 #1),Priorix R ⃝ 和 Varilix R ⃝
由于奇马尼马尼的气候变化,农村妇女遇到的心理挑战,津巴布韦
本研究论文研究了由于气候变化而导致津巴布韦农村地区妇女面临的心理挑战。该研究采用定性研究方法,利用案例研究设计来探索Nyanyadzi Ward 8 Chimanimani区的妇女经历。使用目的和便利抽样方法选择了包括关键线人在内的十名参与者,以确保样本中的多样性。通过半结构化访谈收集了数据,这些访谈的开放性问题并补充了笔记。的道德考虑,包括诚实,真实和正直。主题分析被用于分析并介绍收集的数据,并揭示了两个主题; 1)妇女对气候变化的影响的脆弱性和暴露,以及2)由于气候变化而导致的女性遇到的心理挑战。这些发现强调了对整体支持系统和干预措施的迫切需求,这些系统认识并解决了受气候变化影响的农村地区妇女的心理健康。这项研究强调了整合对性别敏感的方法和气候教育计划,以促进农村社区的韧性,性别平等和可持续发展。研究结果对在气候变化适应,性别平等和心理健康领域工作的决策者,从业者和研究人员具有影响。关键词:气候变化,心理健康,韧性,性别规范简介本文提出的建议为实施倡议提供了宝贵的见解和指导,以增强农村妇女权力,增强其心理健康并促进性别响应性的气候行动。
马尼托巴省的人工智能
TheoryMesh 提供软件解决方案,帮助数字化和优化食品供应链。他们当前的平台包括扫描纸质文档的数字化和流程优化。对于农业和食品行业,公司之间交换的大部分信息都是纸质的。TheoryMesh 的软件使用人工智能来确定新扫描文档中包含的信息,然后不断进行训练以改进从这些文档中捕获数据的能力。他们的流程优化软件允许公司创建多步骤流程,然后使用人工智能提供关于如何获得最佳输出的分析和预测分析。对于食品公司来说,这可能包括调整复杂提取过程中的参数或更好地控制输入谷物的特性。
马戛尔尼远征与全球经济
特雷弗:我们的故事从英格兰南部海岸的朴茨茅斯开始。和世界上许多其他重要的贸易城市一样,朴茨茅斯是一个天然的港口。在这里,船只可以免受英吉利海峡恶劣天气或敌船的侵扰。事实上,这是欧洲防御最严密的城市——因为敌人很多。公元三世纪,罗马占领该岛时,他们在这里修建了一座堡垒,以击退撒克逊人的袭击。14 世纪,当英国与法国陷入 100 年的冲突时,法国人至少三次烧毁了该镇。然后,在 15 世纪,亨利八世国王把这里变成了英国第一个主要海军基地。它的码头制造了当时欧洲最大的一些船只,包括亨利八世的旗舰玛丽玫瑰号。02:10
索乐匹尼布(Syk) ITP治疗领域新希望
SYHX1901 JAK/Syk 抑制剂 石药集团 斑块状银屑病 ; 白癜风 / II 期 类风湿性关节炎 ; 系统性红斑狼疮 / I 期 TOP1288 p38 MAPK/Src/Syk 抑制剂 TopiVert 溃疡性结肠炎 II 期 / cevidoplenib Syk 抑制剂 Genosco 免疫性血小板减少症 ; 类风湿性关节炎 II 期 / lanraplenib Syk 抑制剂 吉利德 干燥综合征 ; 狼疮性肾炎 ; 急性髓系白血病 II 期 / mivavotinib Syk/Flt3 抑制剂 Calithera Biosciences 弥漫性大 B 细胞淋巴瘤 II 期 /
道尔顿交易
它们通过可逆的 ATP 竞争机制在细胞内与受体结合发挥作用。5 – 7 对伊马替尼的耐药性促使人们开发新的 TKI,例如尼洛替尼,它的药效大约是伊马替尼的 30 倍,并且具有三氟甲基,可增加与活性位点的范德华 (wdW) 相互作用。8 尼洛替尼可以规避 33 种临床相关的伊马替尼耐药突变中的 32 种。考虑到伊马替尼和尼洛替尼与顺铂联合使用时表现出协同抗肿瘤作用,本研究的关键概念是将 TKI 的抑制作用与顺铂的抗癌特性结合起来,通过设计和合成在一个独特分子中包含 Pt(II) 支架(即顺铂)和 TKI(即尼洛替尼和伊马替尼)的 Pt(IV) 物种。